Generischer Name: Sulfacetamid-Natrium, Schwefel
Darreichungsform: Creme
Medizinisch überprüft von Drugs.com . Zuletzt aktualisiert am Jan 1, 2021.
- Nebenwirkungen
- Dosierung
- Professional
- Wechselwirkungen
- Mehr
Haftungsausschluss: Dieses Medikament wurde von der FDA nicht als sicher und wirksam befunden, und diese Kennzeichnung wurde von der FDA nicht genehmigt. Weitere Informationen zu nicht zugelassenen Medikamenten finden Sie hier.
Nur Rx
NUR ZUR ÄUßERLICHEN ANWENDUNG. NICHT FÜR OPHTHALMISCHEN GEBRAUCH.
BESCHREIBUNG:
Jedes Gramm enthält 100 mg Natriumsulfacetamid und 50 mg kolloidalen Schwefel in einem Vehikel bestehend aus: Benzylalkohol, Cetylalkohol, Dinatrium-EDTA, Duftstoff, Glycerylstearat (und) PEG-100-Stearat, Magnesium-Aluminium-Silikat, PEG-150-Distearat, Phenoxyethanol, Polyethylenglykol 400, gereinigtes Wasser, Natriumlaurylsulfat, Natriumthiosulfat , Stearylalkohol und Xanthangummi.
Natriumsulfacetamid ist ein Sulfonamid mit antibakterieller Aktivität, während Schwefel als Keratolytikum wirkt. Natriumsulfacetamid ist C 8H 9N 2NaO 3S · H 2O mit einem Molekulargewicht von 254,24. Chemisch ist Natriumsulfacetamid N -Acetamid, Mononatriumsalz, Monohydrat. Die Strukturformel lautet:
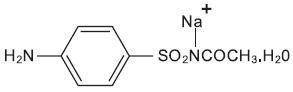
Natriumsulfacetamid ist ein geruchloses, weißes, kristallines Pulver mit einem bitteren Geschmack. Es ist frei löslich in Wasser, schwer löslich in Alkohol, während praktisch unlöslich in Benzol, in Chloroform und in Ether.
KLINISCHE PHARMAKOLOGIE:
Natriumsulfacetamid übt eine bakteriostatische Wirkung gegen Sulfonamid-empfindliche grampositive und gramnegative Mikroorganismen aus, die üblicherweise aus sekundären kutanen pyogenen Infektionen isoliert werden. Es wirkt, indem es die Synthese von Folsäure, die Bakterien für das Wachstum benötigen, durch seine Konkurrenz mit Paraaminobenzoesäure einschränkt. Es liegen keine klinischen Daten zum Grad und zur Rate der systemischen Resorption dieses Produkts bei Anwendung auf Haut oder Kopfhaut vor. Es wurde jedoch über eine signifikante Resorption von Natriumsulfacetamid durch die Haut berichtet.
Die folgenden In-vitro-Daten liegen vor, die klinische Signifikanz ist jedoch unbekannt. Organismen, die eine Anfälligkeit für Natriumsulfacetamid zeigen, sind: Streptokokken, Staphylokokken, E. coli, Klebsiella pneumoniae, Pseudomonas pyocyanea, Salmonellenarten, Proteus vulgaris, Nocardia und Actinomyces.
Die genaue Wirkungsweise von Schwefel bei der Behandlung von Akne ist unbekannt, aber es wurde berichtet, dass es das Wachstum von Propionibacterium acnes und die Bildung von freien Fettsäuren hemmt.
INDIKATIONEN:
Dieses Produkt ist zur topischen Kontrolle von Akne vulgaris, Akne rosacea und seborrhoischer Dermatitis indiziert.
KONTRAINDIKATIONEN:
Dieses Produkt ist bei Personen mit bekannter oder vermuteter Überempfindlichkeit gegen einen der Inhaltsstoffe des Produkts kontraindiziert. Dieses Produkt darf nicht von Patienten mit Nierenerkrankungen angewendet werden.
WARNHINWEISE:
Es ist bekannt, dass Sulfonamide bei überempfindlichen Personen das Stevens-Johnson-Syndrom verursachen. Das Stevens-Johnson-Syndrom wurde auch nach topischer Anwendung von Natriumsulfacetamid berichtet. Fälle von arzneimittelinduziertem systemischem Lupus erythematodes durch topisches Sulfacetamid wurden ebenfalls berichtet. In einem dieser Fälle gab es einen tödlichen Ausgang.
DARF NICHT IN DIE HÄNDE VON KINDERN GELANGEN.
VORSICHTSMAßNAHMEN:
NUR ZUR ÄUßERLICHEN ANWENDUNG. NICHT FÜR OPHTHALMISCHEN GEBRAUCH.
Allgemein: Unempfindliche Organismen, einschließlich Pilze, können sich unter Verwendung dieser Zubereitung vermehren.
Obwohl selten, kann eine Empfindlichkeit gegenüber Natriumsulfacetamid auftreten. Daher ist bei der Verschreibung dieses Arzneimittels bei Patienten, die zu einer Überempfindlichkeit gegen topische Sulfonamide neigen, Vorsicht und sorgfältige Überwachung geboten. Wenn die Verwendung dieses Produkts Anzeichen von Überempfindlichkeit oder anderen unerwünschten Reaktionen hervorruft, stellen Sie die Verwendung des Arzneimittels ein. Die Patienten sollten während der Langzeittherapie sorgfältig auf mögliche lokale Reizungen oder Sensibilisierungen beobachtet werden. Systemische toxische Reaktionen wie Agranulozytose, akute hämolytische Anämie, Purpura hemorrhagica, Drogenfieber, Gelbsucht und Kontaktdermatitis weisen auf eine Überempfindlichkeit gegen Sulfonamide hin. Besondere Vorsicht ist geboten, wenn Bereiche mit entblößter oder abgerissener Haut betroffen sind. Die systemische Resorption topischer Sulfonamide ist nach Anwendung auf große, infizierte, abgeriebene, entblößte oder stark verbrannte Bereiche größer. Unter diesen Umständen könnten möglicherweise Nebenwirkungen auftreten, die durch die systemische Verabreichung dieser Wirkstoffe hervorgerufen werden, und es sollten geeignete Beobachtungen und Laborbestimmungen durchgeführt werden.
Ziel dieser Therapie ist es, eine Abschuppung ohne Reizung zu erreichen, aber Natriumsulfacetamid und Schwefel können Rötung und Schuppung der Epidermis verursachen. Diese Nebenwirkungen sind nicht ungewöhnlich bei der Behandlung von Akne vulgaris, aber die Patienten sollten über die Möglichkeit gewarnt werden.
Informationen für Patienten: Patienten sollten die Anwendung dieses Produkts abbrechen, wenn sich der Zustand verschlechtert oder wenn sich in dem zu behandelnden Bereich oder anderswo ein Hautausschlag entwickelt. Die Verwendung dieses Produkts sollte auch sofort abgebrochen und der Arzt benachrichtigt werden, wenn sich Arthritis, Fieber oder Wunden im Mund entwickeln. Kontakt mit Augen, Lippen und Schleimhäuten vermeiden.
Wechselwirkungen mit anderen Arzneimitteln: Dieses Produkt ist mit Silberpräparaten nicht kompatibel.
Karzinogenese, Mutagenese und Beeinträchtigung der Fertilität: Langzeit-Tierstudien zum karzinogenen Potenzial dieses Produkts wurden bisher nicht durchgeführt. Studien zur Fortpflanzung und Fruchtbarkeit wurden ebenfalls nicht durchgeführt. Chromosomale Nichtdisjunktion wurde in der Hefe Saccharomyces cerevisiae nach Anwendung von Natriumsulfacetamid berichtet. Die Bedeutung dieses Befundes für die topische Anwendung von Natriumsulfacetamid beim Menschen ist unbekannt.
Trächtigkeit: Kategorie C. Mit diesem Tierarzneimittel wurden keine Reproduktionsstudien an Tieren durchgeführt. Es ist auch nicht bekannt, ob dieses Produkt die Fortpflanzungsfähigkeit beeinträchtigen oder den Fötus schädigen kann, wenn es einer schwangeren Frau verabreicht wird. Dieses Produkt sollte von einer schwangeren Frau nur verwendet werden, wenn dies eindeutig erforderlich ist oder wenn der potenzielle Nutzen die potenziellen Gefahren für den Fötus überwiegt.
Stillende Mütter: Es ist nicht bekannt, ob dieses Arzneimittel in die Muttermilch übergeht. Da viele Arzneimittel in die Muttermilch übergehen, ist Vorsicht geboten, wenn dieses Arzneimittel einer stillenden Frau verabreicht wird.
Pädiatrische Anwendung: Sicherheit und Wirksamkeit bei Kindern unter 12 Jahren sind nicht erwiesen.
NEBENWIRKUNGEN:
Berichte über Reizung und Überempfindlichkeit gegen Natriumsulfacetamid sind gelegentlich. Die folgenden Nebenwirkungen, die nach Verabreichung von sterilem ophthalmischem Natriumsulfacetamid berichtet wurden, sind bemerkenswert: Fälle von Stevens-Johnson-Syndrom und Fälle von lokaler Überempfindlichkeit, die sich zu einem Syndrom entwickelten, das einem systemischen Lupus erythematodes ähnelt; In einem Fall wurde ein tödlicher Ausgang berichtet (siehe WARNHINWEISE).
ÜBERDOSIERUNG:
Die orale LD 50 von Sulfacetamid bei Mäusen beträgt 16,5 g / kg. Im Falle einer Überdosierung sollte sofort mit der Notfallbehandlung begonnen werden.
Symptome: Überdosierung kann Übelkeit und Erbrechen verursachen. Eine große orale Überdosierung kann aufgrund der Ausfällung von Sulfakristallen in den Nierentubuli und im Harntrakt zu Hämaturie, Kristallurie und Nierenstillstand führen. Wenden Sie sich zur Behandlung an Ihr örtliches Giftinformationszentrum oder Ihren Arzt.
DOSIERUNG UND ANWENDUNG:
Betroffene Stellen reinigen. Tragen Sie eine dünne Schicht auf die betroffenen Stellen mit Licht massieren, 1 bis 3 mal täglich oder wie von einem Arzt verordnet.
LAGERUNG:
Lagerung bei 20 °C bis 25 °C (68 °F bis 77 °F), zulässige Abweichungen zwischen 15 °C und 30 °C (zwischen 59 °F und 86 °F). Eine kurze Exposition gegenüber Temperaturen von bis zu 40 ° C (104 ° F) kann toleriert werden, sofern die mittlere kinetische Temperatur 25 ° C (77 ° F) nicht überschreitet.
HINWEIS: Vor Frost und übermäßiger Hitze schützen. Das Produkt kann bei Lagerung leicht nachdunkeln. Leichte Verfärbungen beeinträchtigen die Wirksamkeit oder Sicherheit des Produkts nicht. Flasche fest verschlossen halten.
Gelegentlich kann eine leichte Verfärbung des Gewebes auftreten, wenn eine übermäßige Menge des Produkts verwendet wird und mit weißen Stoffen in Kontakt kommt. Diese Verfärbung stellt jedoch kein Problem dar, da sie durch gewöhnliches Waschen ohne Bleichmittel leicht entfernt werden kann.
WIE GELIEFERT:
Dieses Produkt wird in den folgenden Größen geliefert:
2 oz. (57 g) Flaschen, NDC 0178-0470-02
Um ein schwerwiegendes unerwünschtes Ereignis zu melden oder Produktinformationen zu erhalten, rufen Sie 1-800-298-1087 an.
Hergestellt für:
MISSION PHARMACAL UNTERNEHMEN
San Antonio, TX 78230 1355
| AVAR-E Sulfacetamid-Natrium, Schwefelcreme |
||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||
Etikettierer – Mission Pharmacal Company (008117095)
Mehr über Avar-E (sulfacetamide sodium / sulfur))
- Nebenwirkungen
- Dosierungsinformationen
- Wechselwirkungen mit anderen Arzneimitteln
- Preise & Gutscheine
- Arzneimittelklasse: topische Antibiotika
Professionelle Ressourcen
- Verschreibungsinformationen
Andere Marken Sulfacleanse 8/4, Plexion, Sumaxin, Rosanil Reiniger, … +23 mehr
Andere Formulierungen
- Avar
- … +4 mehr
Verwandte Behandlungsleitfäden
- Akne
- Rosacea
- Seborrhoische Dermatitis
Medizinischer Haftungsausschluss