Pankreaszysten stellen eine kleine, aber zunehmend erkannte Entität von Pankreasanomalien dar. Etwa 70% der zystischen Läsionen der Bauchspeicheldrüse werden zufällig entdeckt. Die am häufigsten auftretenden neoplastischen Pankreaszysten umfassen intraduktales papilläres muzinöses Neoplasma (IPMN), seröses Zystadenom (SCA), muzinöses zystisches Neoplasma mit Ovarialstroma (MCN) und solides pseudopapilläres epitheliales Neoplasma. IPMN wird weiter in Abzweigkanal (BD), Hauptkanal und kombinierte Formen unterteilt. Zusammen bilden diese 90% der prämalignen Pankreastumoren, hauptsächlich zystische Tumoren. Im Gegensatz dazu haben Pseudozyste, echte Epithelzyste, lymphoepitheliale Zyste und muzinöse nicht-neoplastische Zyste kein malignes Potenzial.
Malignität tritt nur bei muzinösen Zysten auf. SCA gilt als nichtmaligne Läsion, und es wurde nicht festgestellt, dass bösartige seröse Tumoren, die in der Literatur berichtet wurden, die WHO-Kriterien für SCN erfüllen. IPMN kann von niedrigeren zu höheren Dysplasiegraden und letztendlich zum pankreasduktalen Adenokarzinom (PDAC) fortschreiten. IPMNs, an denen der Hauptkanal beteiligt ist, weisen eine höhere Malignitätsrate auf als diejenigen in den Zweigen, wobei das Malignitätsrisiko auf 62% geschätzt wird; Das Malignitätsrisiko von MCNs beträgt weniger als 15%. Andere, seltenere zystische Läsionen, wie solides pseudopapilläres epitheliales Neoplasma und zystischer neuroendokriner Pankreastumor (cPNET), weisen tendenziell Merkmale auf, die auf eine spezifische Diagnose hindeuten und normalerweise zu einer chirurgischen Entfernung führen.
Um die Häufigkeit zufälliger Pankreaszysten bei asymptomatischen Personen zu untersuchen, führte Kromrey eine Magnetresonanz-Cholangiopankreatographie-Untersuchung (MRCP) bei 1077 Teilnehmern durch, die an einer populationsbasierten Kohortenstudie teilnahmen. Von der ursprünglichen Gruppe wurden 676 Personen 5 Jahre später einer Wiederholungsuntersuchung unterzogen. Zum Zeitpunkt der Erstuntersuchung hatten 49% mindestens eine Zyste mit einem Durchmesser von ≥2 mm. Die Inzidenz neuer Zysten während der Nachbeobachtungszeit betrug 2,6% pro Jahr. Zystenpräsenz war stark mit dem Alter verbunden; Im Alter von 75 Jahren hatten 75% der Teilnehmer eine oder mehrere Zysten. Die Unterscheidung zwischen gutartigen und prämalignen oder malignen Pankreaszysten ist von hoher Bedeutung, um unnötige Eingriffe wie radiologische Nachuntersuchungen oder chirurgische Resektionen zu vermeiden.
Muzinöses zystisches Neoplasma mit Ovarialstroma (MCN)
MCNs treten häufig bei Frauen mittleren Alters auf, sind normalerweise gut definiert und befinden sich überwiegend im Pankreasschwanz (>90%). Im Vergleich zu serösen zystischen Tumoren sind MCNs größer (> 20 mm Durchmesser) und weniger zahlreich (normalerweise < 6). Das biologische Verhalten von MCNs ist variabel, und verschiedene histologische Muster koexistieren häufig im selben Tumor. Die Tumoren können vollständig gutartig sein, ebenso wie muzinöse Zystadenome oder intraduktale papilläre muzinöse Adenome. Einige Tumoren sind grenzwertig und zeigen zelluläre Dysplasie, während andere offen bösartig sind. Malignes Zystadenokarzinom und intramedulläres muzinöses Karzinom können weiter unterteilt werden in nichtinvasive und invasive Typen.
(Die radiologischen Eigenschaften von MCNs sind in den folgenden Bildern dargestellt.)
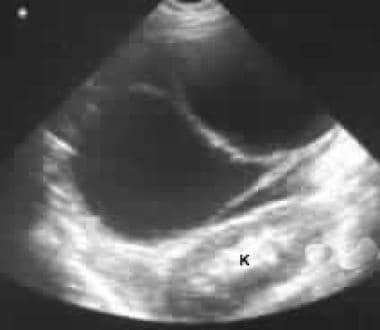 Sonogramm durch das linke Hypochondrium zeigt eine große septierte Masse vor der Niere (K).
Sonogramm durch das linke Hypochondrium zeigt eine große septierte Masse vor der Niere (K). 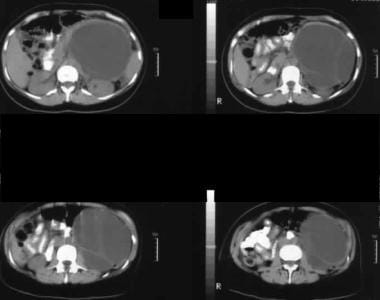 Nicht erweiterte axiale CT-Scans. Bild 1 zeigt eine große septierte Masse im linken Hypochondrium. Beachten Sie die glatte Außenkontur, die typisch für ein muzinöses zystisches Neoplasma ist.
Nicht erweiterte axiale CT-Scans. Bild 1 zeigt eine große septierte Masse im linken Hypochondrium. Beachten Sie die glatte Außenkontur, die typisch für ein muzinöses zystisches Neoplasma ist. Intraduktales papilläres muzinöses Neoplasma (IPMN)
Auf der Grundlage der Beteiligung des Pankreasganges werden IPMNs entweder als Hauptgang-IPMN, Seitenast-IPMN oder Mischvariante IPMN klassifiziert, an der sowohl der Pankreasgang als auch die Seitenäste beteiligt sind. Hauptgang IPMNs haben oft Darm-Typ Epithel, und Seitenast IPMNs haben in der Regel Magen-Typ Epithel. Obwohl alle morphologischen Varianten von IPMN zu Krebs fortschreiten können, invasives Adenokarzinom Mit Ursprung in IPMNs vom Magen-Typ ist mit einer signifikant schlechteren Überlebensrate verbunden als bei anderen Arten von IPMNs. Die Bildgebungsmerkmale sind jedoch nicht spezifisch für die Differenzierung der verschiedenen histologischen Varianten von IPMNs.
Seitenzweig-IPMNs werden häufig bei älteren Männern nachgewiesen und befinden sich häufiger im proximalen Pankreas (Kopf- und Uncinatfortsatz). Ein wichtiges Unterscheidungsmerkmal zwischen MCN und IPMN ist die Visualisierung der pankreatischen duktalen Kommunikation. Wenn ein klarer Kommunikationskanal mit dem Pankreasgang sichtbar gemacht wird, ist die Diagnose von Seitenast-IPMN fast sicher, da SCAs und MCNs nicht mit dem Pankreasduktalsystem kommunizieren.
Trotz der geringen Inzidenz der Aggressivität muzinöser zystischer Läsionen von 3 cm und kleiner ist die Inzidenz nicht niedrig genug, um die Läsionen vollständig zu verwerfen, und eine sorgfältige Überprüfung der Bildgebungsmerkmale ist erforderlich. Darüber hinaus benötigen Patienten, deren Zustand für das chirurgische Management nicht geeignet ist, häufig häufige Bewertungen für das Wachstum und die Änderung der Bildgebungsmerkmale.
(IPMNs sind in den folgenden Bildern zu sehen.)
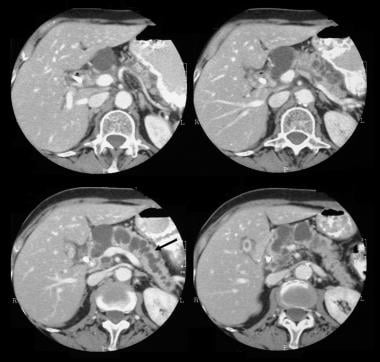 Pankreatischer intraduktaler papillärer Schleimhauttumor (IPMT). Kontrastverstärkte axiale CT-Scans durch die Bauchspeicheldrüse zeigen einen 5,5 cm großen zystischen Tumor im Pankreaskopf. Beachten Sie die stromaufwärtige, grobe Dilatation des Pankreasganges. Der akzessorische Pankreasgang ist ebenfalls erweitert.
Pankreatischer intraduktaler papillärer Schleimhauttumor (IPMT). Kontrastverstärkte axiale CT-Scans durch die Bauchspeicheldrüse zeigen einen 5,5 cm großen zystischen Tumor im Pankreaskopf. Beachten Sie die stromaufwärtige, grobe Dilatation des Pankreasganges. Der akzessorische Pankreasgang ist ebenfalls erweitert. 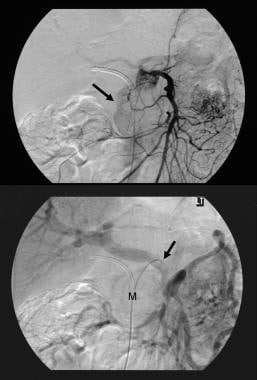 intraduktaler papillärer Schleimhauttumor der Bauchspeicheldrüse (IPMT). (Oben) Das obere Mesenterialangiogramm zeigt die Kapillarvaskularität in der Masse im Pankreaskopf während der arteriellen Phase. (Unten) Das Pfortaderphasenbild zeigt die Verschiebung der Pfortaderäste und die Umhüllung der Verbindung der oberen Mesenterialvene und der Pfortader. M bezeichnet die Pankreasmasse.
intraduktaler papillärer Schleimhauttumor der Bauchspeicheldrüse (IPMT). (Oben) Das obere Mesenterialangiogramm zeigt die Kapillarvaskularität in der Masse im Pankreaskopf während der arteriellen Phase. (Unten) Das Pfortaderphasenbild zeigt die Verschiebung der Pfortaderäste und die Umhüllung der Verbindung der oberen Mesenterialvene und der Pfortader. M bezeichnet die Pankreasmasse. 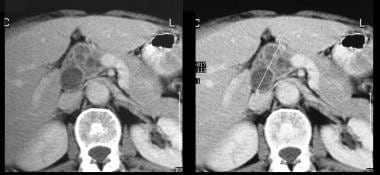 intraduktaler papillärer Schleimhauttumor der Bauchspeicheldrüse (IPMT). Kontrastverstärkte axiale CT-Scans durch die Bauchspeicheldrüse zeigen einen multiseptären Tumor im Pankreaskopf.
intraduktaler papillärer Schleimhauttumor der Bauchspeicheldrüse (IPMT). Kontrastverstärkte axiale CT-Scans durch die Bauchspeicheldrüse zeigen einen multiseptären Tumor im Pankreaskopf. 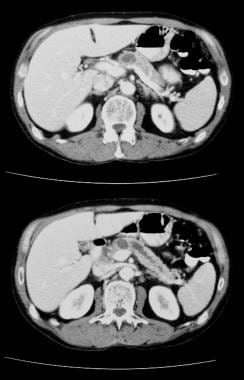 intraduktaler papillärer Schleimhauttumor der Bauchspeicheldrüse (IPMT). Kontrastverstärkte CT-Scans durch die Bauchspeicheldrüse zeigen eine starke Erweiterung des Pankreasganges. Bei der Operation wurde IPMT bestätigt.
intraduktaler papillärer Schleimhauttumor der Bauchspeicheldrüse (IPMT). Kontrastverstärkte CT-Scans durch die Bauchspeicheldrüse zeigen eine starke Erweiterung des Pankreasganges. Bei der Operation wurde IPMT bestätigt. Seröse Zystadenome
Seröse Zystadenome (mikrozystische Adenome) (siehe Bilder unten) sind die zweithäufigsten zystischen Tumoren der Bauchspeicheldrüse. Das klinische Erscheinungsbild seröser Zystadenome ähnelt dem von muzinösen zystischen Pankreastumoren.
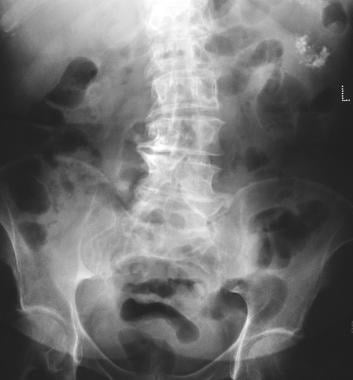 Pankreas-mikrozystisches Adenom. Das Röntgenbild zeigt eine Tumorverkalkung in einem mikrozystischen Adenom (linker oberer Quadrant). Die Verkalkung im mikrozystischen Adenom stellt sich als zentraler Cluster dar, der in einer Sunburst- oder Sternanordnung angeordnet ist. Die zentrale Verkalkung wird mit CT besser beurteilt als mit Radiographie.
Pankreas-mikrozystisches Adenom. Das Röntgenbild zeigt eine Tumorverkalkung in einem mikrozystischen Adenom (linker oberer Quadrant). Die Verkalkung im mikrozystischen Adenom stellt sich als zentraler Cluster dar, der in einer Sunburst- oder Sternanordnung angeordnet ist. Die zentrale Verkalkung wird mit CT besser beurteilt als mit Radiographie. 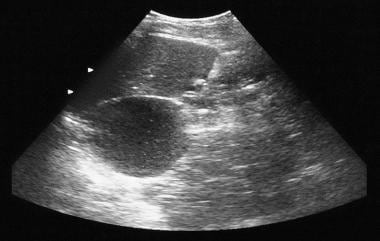 pankreatisches mikrozystisches Adenom. Das Sonogramm zeigt eine zystische Masse im Bereich des Pankreasschwanzes.
pankreatisches mikrozystisches Adenom. Das Sonogramm zeigt eine zystische Masse im Bereich des Pankreasschwanzes. 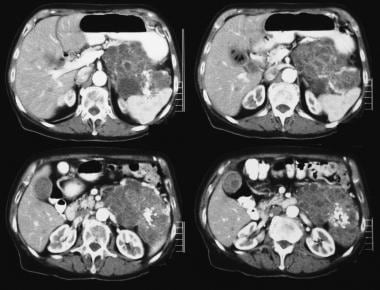 Pankreatisches mikrozystisches Adenom. Kontrastverstärkte axiale CT-Scans zeigen einen hypervaskulären Tumor im Pankreasschwanz mit Sunburst-Verkalkung. Beachten Sie die Swiss-Cheese-Verbesserung.
Pankreatisches mikrozystisches Adenom. Kontrastverstärkte axiale CT-Scans zeigen einen hypervaskulären Tumor im Pankreasschwanz mit Sunburst-Verkalkung. Beachten Sie die Swiss-Cheese-Verbesserung. Aufgrund der zunehmenden Verwendung der Querschnittsbildgebung werden viele dieser Tumoren als zufälliger, asymptomatischer Befund nachgewiesen.
Auf Querschnittsbildern erscheinen seröse Zystadenome als zahlreiche winzige Zysten, die durch empfindliche fibröse Septen getrennt sind, die ihnen ein wabenartiges Aussehen verleihen. Die Zysten sind mit klarer, wässriger Flüssigkeit gefüllt und oft um eine zentrale Sternnarbe herum angeordnet, die verkalkt sein kann. Bei CT-Scans ist die zentrale Sunburst-Verkalkung in einer schwammigen Masse pathognomonisch für diesen Tumor, aber dieser Befund tritt nur bei 10% der Patienten auf.
Die endoskopische Sonographie (EUS) ermöglicht eine bessere Auflösung der Wabenstruktur als die CT. Manchmal können die Zysten groß sein, ein Merkmal, das es schwierig macht, diese Zysten von MCNs zu unterscheiden.
Hypervaskularität kann auf Angiogrammen nachgewiesen werden, und einige Tumoren treten mit intraabdominalen Blutungen auf.
Differentialdiagnosen
Pankreaspseudozysten- oder Pankreasflüssigkeitsansammlungen
Flüssigkeitsansammlungen treten in bis zu 50% der Fälle einer akuten Pankreatitis auf. Pseudozysten werden normalerweise als schalltote Flüssigkeitsräume auf Sonogrammen gesehen, aber sie können interne Echos zeigen, wenn sie nekrotisches Gewebe oder Gerinnsel enthalten.
Bildgebende Befunde, die auf eine Diagnose einer Pseudozyste anstelle eines zystischen Neoplasmas hindeuten, umfassen Folgendes: Fehlen von Septen, Lokulationen, festen Bestandteilen oder Zystenwandverkalkungen bei Computertomographien (CT); Hypovaskularität bei Angiogrammen; und Kommunikation zwischen der Zyste und den Pankreasgängen bei der endoskopischen retrograden Cholangiopankreatographie (ERCP). Die meisten Pseudozysten sind extrapankreatisch, während pankreatische zystische Neoplasmen intrapankreatisch sind.
Pankreasabszess
Pankreasabszess ist in der Regel sekundär zu einer Infektion einer Pseudozyste, aber in seltenen Fällen kann es als Folge der direkten Ausbreitung von Nieren- oder Dickdarm-Infektion auftreten. Typischerweise tritt ein Pankreasabszess 2-4 Wochen nach einer akuten Pankreatitis auf.
Auf Bildern können diese Abszesse Pseudozysten ähnlich erscheinen. Im Allgemeinen hängt das Aussehen von ihrem Alter ab. In der akuten Phase können die Veränderungen subtil sein, wobei nur der Verlust der normalen Pankreaskontur mit einer Auslöschung der Pankreaskontur und der peripankreatischen Gefäß- und anderen Weichteilräume verbunden ist. Diese Veränderungen können von denen bei schwerer akuter Pankreatitis nicht zu unterscheiden sein. Im subakuten und chronischen Stadium, wenn eine zentrale Nekrose auftritt, wird normalerweise eine echoreiche oder komplexe zystische Masse gesehen. Ein Trümmerspiegel kann im abhängigen Teil des Abszesses beobachtet werden. In der subakuten oder chronischen Phase ist die Durchgangsübertragung normalerweise gut, außer wenn Gas im Abszess vorhanden ist. In Gegenwart von Gas kann der Abszess echogen werden und Schatten bilden.
Die Wände des subakuten und chronischen Pankreasabszesses weisen variable Merkmale auf. Die Wände können dick, unregelmäßig und gut definiert sein, oder der Abszess kann überhaupt keine definierbare Wand haben. Die sonographischen Befunde sind unspezifisch, aber im entsprechenden klinischen Umfeld kann eine Diagnose eines Abszesses vorgeschlagen und mittels perkutaner Aspiration oder CT bestätigt werden.
Parasitäre Zysten
Echinococcus granulosis-Zysten und Multilocularis-Zysten der Bauchspeicheldrüse wurden beschrieben, obwohl eine Pankreasbeteiligung außergewöhnlich selten ist. E. Granulosezysten können unilokular, multilokular oder komplex zystisch sein.
Bei der Bildgebung allein ist die Differenzierung dieser und anderer zystischer Massen schwierig. Serologische Tests können in der entsprechenden klinischen Umgebung nützlich sein. E. multilocularis Zysten zeigen ein echogenes infiltratives Muster. Diese Diagnose sollte in endemischen Regionen gestellt werden, wenn ein solches Muster beobachtet wird.
Feste und papilläre epitheliale Pankreastumoren
Feste und papilläre epitheliale Neoplasien der Bauchspeicheldrüse können fest oder zystisch sein. Dies sind seltene Tumoren, die oft mit Mucin-sekretierenden Tumoren oder nicht funktionierenden Adenomen verwechselt werden.
Feste und papilläre epitheliale Pankreastumoren befinden sich am häufigsten im Pankreasschwanz. Sie sind große, gut eingekapselte Massen mit Bereichen von Blutungen und Nekrosen. Auf Sonogrammen erscheinen sie als heterogene, runde, feste Massen mit einem zystischen nekrotischen Zentrum und dystrophischer Verkalkung, die Schatten bilden können.
Dysontogene Zysten
Dysontogene Zysten sind hamartomatöse Zysten, die häufig mit Nierenzysten, Kleinhirnangiomen und Enzephalozelen assoziiert sind. Die Bildgebung zeigt eine große, dünnwandige Zyste mit einer Maulbeerkonfiguration.
Pseudoaneurysmen
Pseudoaneurysmen sind normalerweise nicht wirklich intrapankreatisch und können mit einer Pankreaszyste verwechselt werden. Diese Aneurysmen sind eine Komplikation der Pankreatitis bei 3,5-10% der Patienten. Die Dopplersonographie kann einen turbulenten arteriellen Fluss innerhalb eines Pseudoaneurysmas zeigen, während die Farbfluss-Dopplersonographie einen bidirektionalen Fluss und eine Wirbelung innerhalb der schalltoten Masse zeigt. Die Doppler-Bildgebung kann eine vorläufige Identifizierung der Arterie ermöglichen, die das Pseudoaneurysma speist.
Retroperitoneales Neurofibrom oder Schwannom
Diese Tumoren können echoreiche oder echoarme / zystische Läsionen mit sporadischen inneren Echos sein. Dies ist ein häufiges Merkmal bei größeren Tumoren, bei denen zystische Degeneration und Blutung aufgetreten sind. Die Tumoren sind retroperitoneal, können aber Pankreasmassen nachahmen.
Pankreassarkom
Das Pankreassarkom ist ein seltener Tumor der mesenchymalen Stützstrukturen der Bauchspeicheldrüse. Es ist eine relativ sonoluzente Masse und kann mit einer Flüssigkeitsansammlung oder Pseudozyste verwechselt werden. Sonographische Ergebnisse können normal sein, oder Sonogramme können eine retroperitoneale Masse zeigen, die im Vergleich zu den umgebenden Geweben relativ sonoluzent ist. Daher kann diese Läsion mit einer zystischen Pankreasmasse verwechselt werden.
Pankreaslymphom
Primäres Pankreaslymphom ist selten. Das klinische Erscheinungsbild ist dem des Pankreaskarzinoms nicht unähnlich. Sonographie kann eine homogene, sonolucent oder komplexe Masse aufdecken. Diese Massen sind normalerweise echoarm und können zystische Läsionen nachahmen. Da die Prognose eines Pankreaslymphoms günstig ist, ist seine Differenzierung von einem Karzinom entscheidend. Die Korrelation von sonographischen, CT- und angiographischen Befunden kann zu einer korrekten Diagnose führen. Wenn jedoch Zweifel bestehen, kann eine sonographiegesteuerte Biopsie die wahre Natur der Masse aufdecken.
Pankreas-Azinuszellkarzinom
Pankreaszellkarzinome (PACCs) machen etwa 1% der exokrinen Pankreastumoren aus. PACC ist ein epitheliales Neoplasma mit Anzeichen einer Azinusdifferenzierung. Patienten mit Azinuszellkarzinom haben eine bessere Prognose als Patienten mit Adenokarzinomen vom Duktaltyp, aber eine schlechtere Prognose als Patienten mit endokrinen Tumoren der Bauchspeicheldrüse. Auf CT, PACC wurde auf verschiedene Arten beschrieben, einschließlich als schlecht definierte dichte Masse; als gut definierte Masse mit zentraler Nekrose; und als zystische Masse, umgeben von einer dicken hypervaskulären Wand.
Bevorzugte Untersuchung
Die MRT ist die bevorzugte Technik zur Diagnose von zystischen Pankreastumoren. MRTs sind in der Regel hilfreich bei der Unterscheidung zwischen Pseudozysten und zystischen Neoplasmen. Die Magnetresonanz-Cholangiopankreatographie (MRCP) kann die Anatomie der Gallen- und Pankreasgänge nichtinvasiv darstellen und hilft bei der Diagnose von intraduktalen Tumoren.
Die Sonographie ist im Allgemeinen die erste Technik bei einem Patienten mit epigastrischen Symptomen. Dies ist eine ausgezeichnete Modalität für die Diagnose von zystischen Pankreasmassen. Die Sonographie bietet auch die Möglichkeit für geführte Eingriffe wie Aspiration und Biopsie. Die Dopplersonographie bietet einen zusätzlichen Vorteil bei der Beurteilung von hypervaskulären Tumoren und Gefäßthrombosen / -verschlüssen im Zusammenhang mit Pankreastumoren. Die echoverstärkte Dopplersonographie weist eine hohe Empfindlichkeit und Spezifität bei der Differentialdiagnose von Pankreastumoren auf.
In zweideutigen Fällen oder in Fällen, in denen ein hoher Verdacht auf Malignität besteht, liefert EUS-FNA die beste diagnostische Ausbeute, da es die Gewinnung von zytologischen Proben und zystischer Flüssigkeit für die Analyse verschiedener Tumormarker ermöglicht.
Gelegentlich kann die Art der Zyste trotz vollständiger Beurteilung einer zystischen Masse unbestimmt bleiben. Obwohl teuer und invasiv, tragen die laparoskopische Sonographie, die Biopsie der Zystenwand und die Analyse des zystischen Aspirats signifikant zur Differentialdiagnose von pankreaszystischen Läsionen bei.
CT zeigt Tumorverkalkung und ist eine ausgezeichnete Modalität für den Nachweis von lokalen und Fernmetastasen. Obwohl CT und MRT nicht verwendet werden können, um den Muzingehalt vom Pankreassaft zu unterscheiden, sind die Kommunikation zwischen der zystischen Läsion und der erweiterten MPD und eine prall gefüllte Papille mit einer durchsichtigen Öffnung Merkmale der IPMT. Die innere Architektur von muzinösen Tumoren wird bei MRT-Scans mindestens genauso gut dargestellt wie bei CT-Scans, mit Ausnahme der Verkalkung innerhalb der Läsion (die MRT nur begrenzt aufdecken kann).
Spiral- und / oder Multisektions-CT sind hervorragende Techniken zur Bildgebung der Bauchspeicheldrüse, die eine hervorragende räumliche Auflösung und anatomische Details bieten. Mit dünner Kollimation und arteriellen und venösen Phasen sowie multiplanaren und / oder 3-dimensionalen (3D) Rekonstruktionen werden hervorragende Details der Gefäßanatomie dargestellt; Die meisten Zentren verwenden heute selten Angiographie zur Beurteilung von Pankreastumoren.
Einfache Röntgenaufnahmen werden häufig erhalten, um nach Pankreasverkalkungen zu suchen. Obere GI-Barium-Studien können im Zusammenhang mit epigastrischen Schmerzen durchgeführt werden. Bei Pankreastumoren können Bariumstudien eine extrinsische Verschiebung des Magens und des Zwölffingerdarms zeigen.
Einschränkungen der Techniken
Die MRT ist nicht allgemein verfügbar, teuer und stellt ein Problem für Patienten mit Klaustrophobie dar. Die Genauigkeit der MRT oder MRCP bei der Diagnose des Zystentyps beträgt 40-50% und beträgt 55-76% bei der Bestimmung von gutartigen vs. bösartigen Tumoren.
Viszerales Gas, Patientenhabitus und Bedienerabhängigkeit begrenzen den Wert der Sonographie. Die laparoskopische Sonographie ist invasiv. Die EUS-Bildgebung kann gutartige nicht zuverlässig von malignen IPMNs unterscheiden, und es ist unklar, ob Bildgebungsmerkmale von muzinösen Läsionen mit erhöhtem malignen Potenzial sind ausreichend prädiktiv, um das klinische Management zu beeinflussen. Wenn die chirurgische Histologie als Referenzstandard verwendet wird, liegt die diagnostische Genauigkeit der EUS-Bildgebung zwischen 40 und 96%. Eine einzige prospektive Studie zeigte, dass die Sensitivität (56%) und Spezifität (45%) der EUS-Morphologie allein zur Unterscheidung von muzinösen Zysten (muzinöse zystische Neoplasmen und IPMNs) von nicht-muzinösen Zysten gering waren, was zu einer schlechten Gesamtgenauigkeit führte (51%).
Einfache Röntgenaufnahmen und Bariumuntersuchungen des oberen GI sind unspezifisch, und ähnliche Befunde können bei einer Vielzahl von Pathologien auftreten. CT trägt eine erhebliche Belastung durch ionisierende Strahlung und verwendet jodiertes Kontrastmittel mit einem Risiko für Anaphylaxie und Nephrotoxizität.
Querschnittsstudien, einschließlich Ultraschall, CT und MRT, können nicht zur Unterscheidung zwischen muzinösem Zystadenom und Zystadenokarzinom verwendet werden, es sei denn, der Tumor ist metastasiert oder in benachbarte Organe eingedrungen. Angiographie ist unspezifisch und invasiv. Es erfordert auch jodiertes Kontrastmittel mit dem Risiko von Anaphylaxie und Nephrotoxizität.
Follow-up-Bildgebung
Die ACG-Richtlinien empfehlen, Kandidaten mit asymptomatischen Zysten, von denen angenommen wird, dass sie IPMNs oder MCNs sind, eine Zystenüberwachung anzubieten. Alle chirurgisch resezierten IPMNs erfordern eine postoperative Überwachung, resezierte MCNs ohne Bauchspeicheldrüsenkrebs jedoch nicht. MRCP ist die bevorzugte Modalität für die Überwachung; EUS kann auch das primäre Überwachungsinstrument sein, wenn MRT-Scans kontraindiziert sind. In Ermangelung von Merkmalen, die eine verstärkte Überwachung oder Überweisung zur weiteren Bewertung rechtfertigen, leitet die Zystengröße die Überwachungsintervalle für vermutete IPMNs und MCNs an.
Richtlinien
Richtlinien für die Diagnose und Behandlung von Pankreaszysten wurden von folgenden Organisationen veröffentlicht:
-
American College für Gastroenterologie (ACG)
-
Europäische Studiengruppe für zystische Tumoren der Bauchspeicheldrüse
-
Amerikanisches College für Radiologie (ACR)
Die ACG-Richtlinien von 2018 empfehlen die Magnetresonanztomographie (MRT) oder die Magnetresonanz-Cholangiopankreatographie (MRCP) als bevorzugte Diagnosemodalität aufgrund ihrer Nichtinvasivität, ihres Strahlungsmangels und ihrer größeren Genauigkeit bei der Beurteilung der Kommunikation zwischen dem Pankreasgang und der Zyste (was ein Merkmal von IPMNs mit Seitenzweigen ist). Pankreas-Protokoll-Computertomographie (CT) oder endoskopischer Ultraschall (EUS) wurden als „ausgezeichnete Alternativen“ angesehen, wenn die MRT kontraindiziert ist. Die EUS-Feinnadelaspiration (FNA) und die Zystenflüssigkeitsanalyse sollten bei Zysten in Betracht gezogen werden, bei denen die Diagnose unklar ist und bei denen die Ergebnisse wahrscheinlich das Management verändern.
Analyse der Zystenflüssigkeit CEA kann in Betracht gezogen werden, um IPMNs und MCNs von anderen Zystentypen zu unterscheiden, aber es kann nicht verwendet werden, um IPMNs und MCNs mit hochgradiger Dysplasie oder Bauchspeicheldrüsenkrebs zu identifizieren. IPMNs oder MCNs mit einem der folgenden Merkmale sollten einer EUS mit oder ohne FNA unterzogen und / oder zur weiteren Bewertung an eine multidisziplinäre Gruppe überwiesen werden :
-
Eines der folgenden Symptome oder Anzeichen: Gelbsucht sekundär zur Zyste, akute Pankreatitis sekundär zur Zyste, signifikant erhöhte Serum-CA 19-9
-
Einer der folgenden bildgebenden Befunde: das Vorhandensein eines Wandknotens oder einer festen Komponente entweder innerhalb der Zyste oder im Pankreasparenchym, Erweiterung des Hauptpankreasganges von > 5 mm, eine fokale Erweiterung des Pankreasganges, die für die IPMN des Hauptganges oder eine obstruktive Läsion von Bedeutung ist, oder muzinproduzierende Zysten mit einem Durchmesser von ≥3 cm
-
Das Vorhandensein von hochgradiger Dysplasie oder Bauchspeicheldrüsenkrebs in der Zytologie
Die europäischen Richtlinien von 2018 empfehlen auch die MRT als bevorzugte Methode zur Diagnose von pankreaszystischen Neoplasmen (PCN). Die multimodale Bildgebung sollte in Fällen in Betracht gezogen werden, in denen die Identifizierung von Verkalkungen wichtig ist, für das Tumorstadium oder für die Diagnose postoperativer rezidivierender Erkrankungen. Die Genauigkeit zur Identifizierung des spezifischen PCN-Typs, zur Unterscheidung kleiner PCN von nicht-neoplastischen oder nicht-epithelialen Zysten oder zur Verbindung mit dem duktalen System bleibt jedoch relativ gering. CT sollte in den folgenden klinischen Situationen in Betracht gezogen werden :
-
Zum Nachweis von parenchymaler, muraler oder zentraler Verkalkung und insbesondere zur Unterscheidung von Pseudozysten im Zusammenhang mit chronischer Pankreatitis von pankreatischen zystischen Neoplasmen
-
Wenn der Verdacht auf Malignität oder begleitenden Bauchspeicheldrüsenkrebs besteht und eine Beurteilung der Gefäßbeteiligung, der Peritonealerkrankung oder der Metastasierung erforderlich ist.
-
Bei Verdacht auf postoperatives Wiederauftreten von Bauchspeicheldrüsenkrebs.
Die europäischen Richtlinien finden EUS hilfreich bei der Identifizierung von PCN mit Merkmalen, die für die chirurgische Resektion in Betracht gezogen werden sollten. Ähnlich wie MRT und CT hat EUS eine geringe Genauigkeit zur Identifizierung des genauen PCN-Typs. EUS-FNA verbessert die diagnostische Genauigkeit bei der Unterscheidung von muzinöser und nichtmuzinöser PCN sowie von maligner und benigner PCN in Fällen, in denen CT- oder MRT-Befunde unklar sind. Zusätzliche Empfehlungen für die Verwendung von EUS-FNA umfassen Folgendes:
-
EUS-FNA sollte nur durchgeführt werden, wenn erwartet wird, dass die Ergebnisse das klinische Management ändern
-
EUS-FNA sollte nicht durchgeführt werden, wenn die Diagnose bereits durch Querschnittsbildgebung gestellt wurde oder wenn eine eindeutige Indikation für eine Operation vorliegt
-
Relative Kontraindikationen für EUS-FNA in PCN ist ein Abstand von >10 mm zwischen der Zyste und dem Wandler, das Vorhandensein eines hohen Blutungsrisikos aufgrund einer Blutungsstörung oder die Verwendung von dualen Thrombozytenaggregationshemmern