EINLEITUNG
Arzneimitteleluierende Stents (DES) sind im Vergleich zu Bare-Metal-Stents (BMS) mit signifikant niedrigeren Raten der Revaskularisation von Zielläsionen verbunden. Eine langfristige duale Thrombozytenaggregationshemmertherapie (DAPT) ist jedoch ausnahmslos erforderlich, um eine späte Stentthrombose im Zusammenhang mit einer verzögerten Heilung zu vermeiden und die häufige Anwendung von DES bei Patienten mit hohem Blutungsrisiko zu verhindern. Seit vielen Jahren empfehlen Richtlinien einen Zeitraum von mindestens 12 Monaten DAPT basierend auf der Leistung von DES der ersten Generation.1 Vor kurzem haben europäische Richtlinien empfohlen 6 Monate DAPT für stabile Patienten (Evidenzgrad B).2 DES-Studien und -Register der neuen Generation haben im Vergleich zu DES der ersten Generation oder sogar BMS niedrigere Thromboseraten gezeigt.3-7 Eine retrospektive Analyse von DES-Studien der neuen Generation berichtete, dass ein frühzeitiges Absetzen oder Unterbrechen der DAPT über 1 bis 3 Monate nach der Implantation hinaus das Risiko nicht zu erhöhen schien.8,9
In mehreren Studien wurden unterschiedliche DAPT-Dauern verglichen (3-6 Monate vs. 12-24 Monate).10-16 Einzel- und eine gepoolte Analyse von 4 dieser Studien haben gezeigt, dass kürzere DAPT-Therapien ähnliche Raten von ischämischen Ereignissen zeigen und gleichzeitig die Inzidenz von Blutungsereignissen verringern.10-17
Dennoch schränken bestimmte Vorbehalte die weit verbreitete Anwendbarkeit dieser Studien ein, einschließlich des retrospektiven Designs von Analysen und der damit verbundenen Verzerrungen, einige mit kleinen Stichprobengrößen, eingeschränkter Einhaltung von Protokollen und der häufigen Verwendung veralteter DES. Zum Beispiel ist bekannt, dass die in diesen Studien verwendete Version des Zotarolimus-eluierenden Stents einen relativ hohen Grad an spätem Lumenverlust aufweist, was ihm den Ruf einbrachte, ein Stent zu sein, dessen Verhalten irgendwo zwischen einem BMS und dem DES der neueren Generation liegt. Diese Studien umfassten auch BMS und DES der ersten Generation.
Wir präsentieren ein multizentrisches prospektives Register zur Bewertung der Sicherheit eines 6-monatigen DAPT-Ansatzes bei Patienten, die ein DES der ersten Generation erhalten, im Vergleich zu den Ergebnissen einer übereinstimmenden Serie von Patienten, die 12 Monate DAPT erhalten.
METHODEN
Das multizentrische, prospektive ESTROFA-DAPT-Register umfasst 18 Zentren in ganz Spanien. Diese Analyse ist Teil des ESTROFA-Projekt- und Studiennetzwerks und wurde von der spanischen Arbeitsgruppe für interventionelle Kardiologie der Spanischen Gesellschaft für Kardiologie unterstützt. In jedem Zentrum wurde den Patienten DAPT mit Acetylsalicylsäure und Clopidogrel für 6 Monate nach der DES-Implantation gemäß den folgenden Kriterien verschrieben:
- •
Eine klinische Indikation für eine perkutane Intervention mit einem DES der nicht ersten Generation in einem der folgenden klinischen Umgebungen: a) stille Ischämie; b) stabile Angina pectoris; c) instabile Angina pectoris ohne Troponinerhöhung; d) Patienten mit Myokardinfarkt ohne ST–Segmenterhöhung oder ST-Segmenterhöhung ohne geschätztes geringes Blutungsrisiko bei langfristiger DAPT, die jedoch immer noch als Kandidaten für eine Behandlung mit DES angesehen werden (dh Patienten > 75 Jahre, Patienten mit Magengeschwüren in der Vorgeschichte ohne Blutung, mittelschweres chronisches Nierenversagen oder mittelschwere Lebererkrankung und Patienten mit elektiver nicht kardialer Operation > 6 Monate).
- •
In Bezug auf das Verfahren wurden linke Hauptkoronarläsionen sowie Bifurkationen, die mit 2 Stents behandelt wurden, oder Patienten, die mehr als 3 Stents benötigten, ausgeschlossen. Patienten mit einer späten DES-Thrombose in der Vorgeschichte wurden ebenfalls ausgeschlossen.
Die Entscheidung, diese Einschlusskriterien auszuwählen, basierte auf den folgenden Sicherheitsbedenken: a) Die Anwendung von DAPT für 12 Monate nach einem akuten Koronarsyndrom (ACS) wird durch Evidenz gestützt und in verschiedenen klinischen Leitlinien und Konsensdokumenten empfohlen.1,2,18-21 Es konnten nur Patienten mit ACS mit geringem Risiko und einem bestimmten Blutungsrisiko eingeschlossen werden. b) Die Studie hatte ein sicherheitsorientiertes Protokoll; Daher wurde die Einbeziehung von Patienten mit einem höheren Risiko für Stentthrombosen (> 3 Stents, Bifurkationen mit 2-Stent-Techniken und frühere späte Thrombosen mit DES) und Patienten mit einem hohen Sterberisiko bei einem thrombotischen Ereignis (Stents in der linken Hauptarterie) ausgeschlossen.
Tatsächlich zeigten diese Untergruppen (ACS, multiple Läsionen und komplexe Läsionen) einen Trend, nach einer längeren DAPT-Periode mehr Nutzen zu erzielen als die Untergruppen mit stabiler Angina pectoris oder einzelnen Läsionen in der PRODIGY-Studie.10
Alle klinischen, angiographischen und prozeduralen Ausgangsdaten wurden in einer gemeinsamen Datenbank berichtet, die speziell für diese Studie entwickelt wurde. Informationen zur klinischen Nachsorge wurden ebenfalls übermittelt, und diese Daten wurden regelmäßig während der Überprüfung der Registrierung und der Krankenhausdatenbank sowie durch Patientenkontakt aktualisiert. Die Überprüfung der DAPT für den ≤ 6-monatigen DAPT-Zeitraum war erforderlich und wurde durch Patientenkontakt bestätigt. Die endgültige Entscheidung für die Veranstaltung wurde im Koordinierungszentrum (Hospital Universitario Marqués de Valdecilla) von 2 blinden Ermittlern (Dr. De la Torre und García Camarero) getroffen.
Um diese Kohorte mit der 12-monatigen DAPT-Kohorte zu vergleichen, überprüften wir die ESTROFA-2-Studiendatenbank, die bereits 2010 veröffentlicht wurde.22 Dies war ein multizentrisches, prospektives Register zur Beurteilung der Thromboseinzidenz nach DES-Implantation der zweiten Generation, an der 4768 Patienten teilnahmen; unter diesen wurden 4354 mit 12 Monaten DAPT behandelt. Unter Verwendung beider Registerdatenbanken (ESTROFA-DAPT und ESTROFA-2) wurde eine Propensity-Score-Analyse durchgeführt, um 2 vergleichbare Kohorten von Patienten zu erhalten, die entweder mit einer 6-monatigen oder einer 12-monatigen DAPT behandelt wurden.
Diese 2 Register wurden, obwohl sie in unterschiedlichen Zeiträumen durchgeführt wurden, nach einer ähnlichen Methodik erstellt. Das Steuerungs- und Koordinierungsteam war das gleiche und die webbasierten klinischen Aufzeichnungsformulare hatten das gleiche Format; Die meisten in ESTROFA-DAPT aktiven Zentren rekrutierten auch Patienten in ESTROFA-2 (13 der 18 Zentren). Schließlich waren die Hauptermittler, die an der Analyse der beiden Registrierungsdatenbanken beteiligt waren, dieselben. Die Ereignisentscheidung wurde mit vorab festgelegten Ereignisdefinitionen durchgeführt, und es wurden nach Bedarf zusätzliche Informationen angefordert, um eine ordnungsgemäße endgültige Entscheidung zu erzielen.
Endpunkte und Definitionen
Der primäre Endpunkt der Studie war das 12-monatige ereignisfreie Überleben (Herztod, Myokardinfarkt, Revaskularisation und schwere Blutungen) in beiden DAPT-Behandlungsgruppen. Sekundäre Endpunkte waren Tod aller Ursachen, Herztod, nicht tödlicher Myokardinfarkt, koronare Revaskularisation, definitive Stentthrombose, definite oder wahrscheinliche Stentthrombose, definite oder wahrscheinliche Stentthrombose im Zeitraum von 6 bis 12 Monaten nach der indexierten perkutanen Koronarintervention und schwere Blutungsereignisse.
Die spezifischen Definitionen schwerwiegender unerwünschter kardiovaskulärer Ereignisse waren wie folgt. Myokardinfarkt wurde als typischer Anstieg und allmählicher Abfall (Troponin) oder als schnellerer Anstieg und Abfall (Kreatinkinase-MB) biochemischer Marker definiert, die mit Myokardnekrose in Verbindung mit mindestens 1 der folgenden Faktoren übereinstimmen: ischämische Symptome, die Entwicklung pathologischer Q-Wellen im Elektrokardiogramm, Veränderungen im Elektrokardiogramm, die auf Ischämie hinweisen (ST-Segmenterhöhung oder -depression), oder pathologische Ergebnisse im Einklang mit akutem Myokardinfarkt. Revaskularisation wurde definiert als jede Art von klinisch indizierter perkutaner oder chirurgischer koronarer Revaskularisation. Eine definitive oder wahrscheinliche Stentthrombose wurde gemäß den Definitionen des Akademischen Forschungskonsortiums in Betracht gezogen.23 Blutungsereignisse wurden nach den Kriterien des Bleeding Academic Research Consortium (BARC) kategorisiert.24
Statistische Analyse
Basierend auf früheren Daten von ESTROFA-2 in der Untergruppe aus diesem Register mit einem ähnlichen Profil wie in ESTROFA-DAPT wurde für beide Gruppen eine primäre Endpunktrate von 6, 5% bis 7, 0% angenommen. Daher würde bei einer Leistung von 80% und einem 1-seitigen Typ-I-Fehler von 5% eine Stichprobengröße von 1200 Patienten in jeder Gruppe zeigen Nichtunterlegenheit zwischen den 2 Gruppen für den primären Endpunkt mit einer festen Nichtunterlegenheitsmarge von 2, 5%, die mit übereinstimmt Nichtunterlegenheitsmargen, die in zeitgenössischen Studien mit DES und in einer Studie zum Vergleich verschiedener DAPT-Perioden verwendet wurden.13 Wenn die Obergrenze des 95% -Konfidenzintervalls des Behandlungsunterschieds (Kurz- vs. Langzeit-DAPT) weniger als 2 betrug.5% würde die Nullhypothese abgelehnt, was bedeuten würde, dass die Kurzzeitgruppe der Langzeitgruppe in Bezug auf den primären Endpunkt nach 12 Monaten nicht unterlegen war.
Kontinuierliche Variablen werden als Mittelwert ± Standardabweichung dargestellt. Kategoriale Variablen werden in Prozent ausgedrückt. Kontinuierliche Variablen wurden mit dem Student-t-Test verglichen, wenn sie einer Normalverteilung folgten, und mit Wilcoxon-Tests, wenn sie dies nicht taten (Beurteilung der Art der Verteilung durch den Kolmogorov-Smirnov-Test). Die kategorialen Variablen wurden je nach Bedarf mit dem Chi-Quadrat-Test oder dem exakten Fischer-Test verglichen. Kaplan-Meier-Kurven für das ereignisfreie Überleben wurden für jede in der Analyse berücksichtigte Gruppe oder Untergruppe erhalten und durch den Log-Rank-Test verglichen. Interaktionstests wurden durchgeführt, um Untergruppen zu identifizieren, die unter den 2 verschiedenen DAPT-Perioden unterschiedliche Risiken für eine Stentthrombose darstellen.
Es wurden zwei Maßnahmen durchgeführt, um vergleichbare Patientenserien aus diesen 2 Registern auszuwählen. Zunächst wandten wir die Ausschlusskriterien von ESTROFA-DAPT auf die ESTROFA-2-Datenbank an, sodass Patienten mit behandelten linken Hauptkranzgefäßläsionen, mit 2 Stents behandelten Bifurkationen, Patienten mit mehr als 3 implantierten Stents und Patienten mit einer Vorgeschichte einer späten DES-Thrombose von der Analyse ausgeschlossen wurden. Zweitens haben wir einen Propensity Score Matching-Prozess durchgeführt. Alle in den Tabellen 1 und 2 aufgeführten Variablen wurden als Kovariaten eingegeben, um die Neigungswerte abzuleiten. Der benutzerdefinierte Dialog „psmatching“ wurde in Verbindung mit SPSS Version 19 verwendet. Das Programm „psmatching“ führt alle Analysen in R über das SPSS R-Plugin (Version 2.10.1) durch. Dieses Verfahren umfasste 3 Stufen: a) Die Neigungswerte wurden unter Verwendung der logistischen Regression geschätzt, bei der die Verschreibung eines 6-monatigen DAPT-Regimes wurde als Ergebnisvariable und alle Kovariaten als Prädiktoren verwendet. b) Die Patienten wurden mit einem einfachen 1: 1-Nearest-Neighbor-Matching abgeglichen, das auf einem „gierigen“ Matching-Algorithmus basiert, der die Beobachtungen in der 6-Monats-DAPT-Gruppe nach ihrem geschätzten Neigungswert sortierte. Dieser Algorithmus passte dann jede Einheit sequentiell an eine Einheit in der 12-Monats-DAPT-Gruppe mit dem nächstgelegenen Neigungswert an. Um schlechte Übereinstimmungen auszuschließen, haben wir einen Messschieber von 0,2 der Standardabweichung des Logit des Propensity Scores auferlegt. Wir haben Einheiten außerhalb des Bereichs der gemeinsamen Unterstützung außer Acht gelassen (definiert als die Region der Verteilungen der geschätzten Neigungswerte in den 6-Monats- und 12-Monats-DAPT-Gruppen, für die Einheiten in beiden Gruppen beobachtet wurden). Dies wurde getan, um das Gleichgewicht der Kovariaten zu verbessern. c) Eine Reihe von Modelladäquanzprüfungen wurde durchgeführt, um zu überprüfen, ob durch das Matching-Verfahren ein angemessenes Gleichgewicht der Kovariaten erreicht wurde. Dies geschah durch Berechnung des globalen Ungleichgewichtsmaßes und durch die Erstellung von 5 Diagnoseplots: histogramme der Neigungswerte in beiden Gruppen vor und nach dem Matching, ein Punktdiagramm der individuellen Neigungswerte von Einheiten in der Kontroll- und Behandlungsgruppe, entweder abgestimmt oder nicht, Histogramme der standardisierten Unterschiede aller Terme (Kovariaten, quadratischer Term, Wechselwirkungen) vor und nach dem Matching, ein Punktdiagramm, das die Größe der standardisierten Unterschiede vor und nach dem Matching für jede Kovariate anzeigt, und ein Liniendiagramm der standardisierten mittleren Unterschiede vor und nach dem Matching. Ein Chi-Quadrat-Test für das Gesamtungleichgewicht wird bereitgestellt. Diese Teststatistik, die sich auf die T2-Statistik des bekannten Hoteliers bezieht, bewertet gleichzeitig, ob eine Variable oder eine lineare Kombination von Variablen nach dem Abgleich signifikant unausgeglichen ist. Der Test untersuchte alle Kovariaten, die zur Schätzung des Propensity Scores verwendet wurden. Standardisierte Unterschiede wurden für alle Kovariaten vor und nach dem Matching berechnet, um das Gleichgewicht nach dem Matching zu bewerten. Ein standardisierter Unterschied
Klinische Merkmale in übereinstimmenden Gruppen
| 6- monat DAPT (n = 1286) | 12- monat DAPT (n = 1286) | P | ASD (%) | |
|---|---|---|---|---|
| Alter, Jahre | 67.3 ± 11 | 67.1 ± 11 | .6 | 4.4 |
| Frauen | 304 (23.5) | 300 (23.3) | .9 | 1.1 |
| Raucher | 270 (21.0) | 286 (22.2) | .5 | 4.3 |
| Hypertonie | 849 (66) | 836 (65) | .6 | 3.5 |
| Dyslipidämie | 769 (59.8) | 751 (58.4) | .5 | 3.3 |
| Diabetes mellitus | 526 (40.9) | 502 (39.0) | .3 | 5.7 |
| Eingeschränkte Nierenfunktion* | 103 (8.0) | 99 (7.7) | .8 | 1.8 |
| Vorherige MI | 279 (21.7) | 270 (20.9) | .7 | 2.6 |
| Vorherige PCI | 370 (28.8) | 355 (27.6) | .4 | 5.6 |
| Vorherige CABG | 63 (4.9) | 71 (5.5) | .5 | 4.9 |
| LVEF, % | 56 ± 12.5 | 56.2 ± 12.5 | .8 | 2.1 |
| Stabile Angina | 591 (45.9) | 581 (45.1) | .7 | 2.5 |
| Instabile Angina | 342 (26.6) | 351 (27.3) | .4 | 5.6 |
| Nicht-ST-Segment-Elevation MI | 140 (10.8) | 150 (11.6) | .3 | 6.7 |
| ST-Segment-Höhe MI | 54 (4.2) | 59 (4.6) | .5 | 4.2 |
| Stille Ischämie | 159 (12.3) | 145 (11.3) | .3 | 6.6 |
ASD, absolute standardisierte Differenz; CABG, Koronararterien-Bypass-Transplantat; DAPT, duale Thrombozytenaggregationshemmer; LVEF, linksventrikuläre Ejektionsfraktion; MI, Myokardinfarkt; PCI, perkutane Koronarintervention.
Sofern nicht anders angegeben, werden die Daten als Nr. (%) oder Mittelwert ± Standardabweichung.
Eine eingeschränkte Nierenfunktion wurde definiert als Serumkreatinin > 1,5 mg/dl.
Verfahrensmerkmale in übereinstimmenden Gruppen
| 6- monat DAPT (n = 1286) | 12- monat DAPT (n = 1286) | P | ASD (%) | |
|---|---|---|---|---|
| Nein. von implantierten Stents | 1.17 ± 0.40 | 1.19 ± 0.40 | .2 | 7.2 |
| Stent länge, mm | 21.0 ± 8.0 | 21.2 ± 8.4 | .5 | 4.5 |
| Durchmesser des Stents, mm | 2.90 ± 0.40 | 2.91 ± 0.40 | .5 | 3.4 |
| In-stent restenosis | 96 (7.4) | 82 (6.3) | .3 | 6.7 |
| Bifurcation | 198 (15.4) | 217 (16.8) | .3 | 7.1 |
| Chronic total occlusions | 90 (7.0) | 72 (5.6) | .2 | 7.7 |
| LAD involvement | 602 (46.8) | 605 (47.0) | .9 | 0.9 |
| IVUS guidance | 71 (5.5) | 78 (6.0) | .6 | 3.5 |
| EES | 688 (53.5) | 646 (50.2) | .1 | 7.8 |
| Acetylsalicylic acid + clopidogrel | 1286 (100) | 1286 (100) | 1 | 0 |
ASD, absolute standardized difference; DAPT, dual antiplatelet therapy; EES, everolimus-eluting stent; IVUS, intravascular ultrasound; LAD, left anterior descending artery.
Sofern nicht anders angegeben, werden Daten als Nr. (%) oder Mittelwert ± Standardabweichung.
Ein P-Wert
ERGEBNISSE
Wie im Studienflussdiagramm (Abbildung 1) gezeigt, erhielten wir aus den ursprünglichen ESTROFA-2- und ESTROFA-DAPT-Kohorten und nach Durchführung des Propensity Score Matchings 2 Gruppen von jeweils 1268 Patienten: die 6-Monats-DAPT- und 12-Monats-DAPT-Gruppen. Die klinischen und verfahrenstechnischen Merkmale der 2 Gruppen sind in den Tabellen 1 und 2 dargestellt. Die geschätzten standardisierten Postmatching-Unterschiede für alle Kovariaten werden bereitgestellt. Alle waren
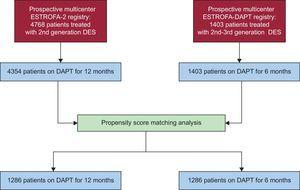
Flussdiagramm studieren. DAPT, duale Thrombozytenaggregationshemmer; DES, arzneimitteleluierende Stents.
In Bezug auf die DES-Verteilung war das am häufigsten verwendete DES in beiden Gruppen der Everolimus-eluierende Stent (53,5% in der 6-Monats-DAPT-Gruppe gegenüber 50,2% in der 12-Monats-DAPT-Gruppe; P = .1). Der Zotarolimus-eluierende Stent wurde in 28.8% der 6-Monats-DAPT-Gruppe gegenüber 49,8% in der 12-Monats-Gruppe; zeitgleich mit den Marken Resolute® und Endeavor®. Der Biolimus-eluierende Stent wurde in 12,7% der 6-monatigen DAPT-Gruppe verwendet.
In der 6-Monats- und der 12-Monats-DAPT-Gruppe gingen keine Patienten an Follow-up verloren und die Therapietreue betrug 97% bzw. 95%. Dies bedeutet, dass nur 3% in der 6-monatigen DAPT-Gruppe die Doppeltherapie über 6 Monate hinaus verlängerten und nur 5% in der 12-monatigen DAPT-Gruppe die Doppeltherapie über das erste Jahr hinaus verlängerten.
Klinische Ereignisse nach 12 Monaten sind in Tabelle 3 dargestellt. Es wurden keine signifikanten Unterschiede zwischen den Gruppen für den primären Endpunkt (Hazard Ratio = 0,75; 95% -Konfidenzintervall, 0,54-1,05 für 6-Monats-vs. 12-Monats-DAPT) oder einen der betrachteten Endpunkte beobachtet, was einen P = ergab .001 für Nichtunterlegenheit. Es gab nicht nur eine ähnliche Inzidenz von ischämischen Ereignissen in der 6-Monats- und 12-Monats-DAPT-Gruppe, sondern auch die Inzidenz von bestimmten und bestimmten oder wahrscheinlichen Thrombosen war in der 6-Monats-Gruppe numerisch niedriger (Abbildungen 2 und 3). Schwere Blutungsereignisse waren in der 12-monatigen DAPT-Gruppe numerisch häufiger, unterschieden sich jedoch nicht signifikant von der 6-monatigen DAPT-Gruppe. Die Inzidenz klinischer Ereignisse im Zeitraum von 6 bis 12 Monaten ist in Tabelle 4 dargestellt, während die Patienten in der 6-Monats- bzw. 12-Monats-DAPT-Gruppe keine DAPT / keine DAPT erhielten. In diesem Zeitraum wurden keine Unterschiede zwischen den Gruppen beobachtet.
Ergebnisse nach 12 Monaten Follow-up
| 6- monat DAPT (n = 1286) | 12- monat DAPT (n = 1286) | P | |
|---|---|---|---|
| Primärer Endpunkt | |||
| Herztod, Myokardinfarkt, Revaskularisation oder BARC ≥ 3 Blutung | 65 (5.0) | 85 (6.6) | .09 |
| Sekundäre Endpunkte | |||
| Tod aller Ursachen | 21 (1.6) | 24 (1.9) | .4 |
| Herztod | 11 (0.9) | 13 (1.0) | .9 |
| Myokardinfarkt | 10 (0.85) | 13 (1.00) | .8 |
| Revaskularisation | 41 (3.2) | 55 (4.3) | .1 |
| Definitive Thrombose | 3 (0.24) | 5 (0.40) | .5 |
| Definitive und wahrscheinliche Thrombose | 6 (0.5) | 9 (0.7) | .4 |
| BARC ≥ 3 Blutungsereignisse | 10 (0.8) | 18 (1.4) | .2 |
BARC, Blutungen Academic Research Consortium; DAPT, dual Thrombozytenaggregationshemmer.
Die Daten werden als Nr. (%).
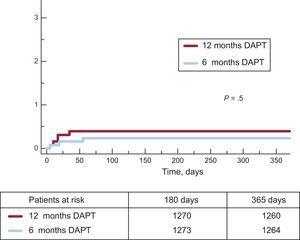
Kumulative Inzidenz einer definitiven Stentthrombose in beiden Gruppen. DAPT: duale Thrombozytenaggregationshemmer-Therapie.
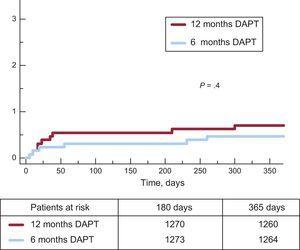
Kumulative Inzidenz einer definitiven oder wahrscheinlichen Stentthrombose in beiden Gruppen. DAPT, duale Thrombozytenaggregationshemmer.
Ergebnisse von 6 bis 12 Monaten
| 6- monat DAPT (n = 1272)* | 12- monat DAPT (n = 1270)* | P | |
|---|---|---|---|
| Primärer Endpunkt | |||
| Herztod, Myokardinfarkt, Revaskularisation oder BARC ≥ 3 Blutung | 38 (2.9) | 54 (4.2) | .1 |
| Sekundäre Endpunkte | |||
| Tod aller Ursachen | 7 (0.55) | 8 (0.60) | .8 |
| Herztod | 3 (0.23) | 4 (0.31) | .8 |
| Myokardinfarkt | 3 (0.23) | 5 (0.40) | .8 |
| Revaskularisation | 32 (2.5) | 44 (3.5) | .2 |
| Definitive Thrombose | 0 (0.0) | 0 (0.0) | |
| Definitive und wahrscheinliche Thrombose | 2 (0.15) | 2 (0.15) | .9 |
| BARC ≥ 3 Blutungsereignisse | 2 (0.15) | 5 (0.40) | .5 |
BARC, Blutungen Academic Research Consortium; DAPT, dual Thrombozytenaggregationshemmer.
Die Daten werden als Nr. (%).
Anzahl der lebenden Patienten nach 6 Monaten Follow-up.
Subgruppenanalysen ergaben keine signifikanten Wechselwirkungen. Bemerkenswert ist, dass in der Untergruppe der Patienten mit oder ohne Myokardinfarkt mit ST-Segmenterhöhung, die 15% der Patienten in der 6-Monats-DAPT-Gruppe und 16,2% in der 12-Monats-DAPT-Gruppe umfasste, der primäre Endpunkt in 7,7% bzw. 8,1% erreicht wurde (P = .8).
DISKUSSION
Die Ergebnisse dieser Studie legen nahe, dass bei ausgewählten Patienten (die etwa 40% der mit DES behandelten Patienten ausmachen) ein 6-monatiges DAPT-Regime aus Sicht der ischämischen Ereignisraten genauso sicher zu sein scheint wie ein 12-monatiges DAPT-Regime.
Die Verwendung von DES reduziert signifikant die Notwendigkeit einer wiederholten koronaren Revaskularisation. DES der neueren Generation, insbesondere Everolimus-eluierende Stents, sind im Vergleich zu DES der ersten Generation oder sogar mit BMS mit einer Verringerung der Thromboseraten verbunden.3-7 Daher besteht eine wesentliche Einschränkung für die Verwendung von DES in der Notwendigkeit eines längerfristigen DAPT-Regimes im Gegensatz zum 1-monatigen DAPT-Regime nach BMS Implantation. Langfristige DAPT ist mit einem höheren Blutungsrisiko und höheren Kosten verbunden. Diese Einschränkungen erklären, warum in einigen Umgebungen ohne offensichtliche Einschränkungen der DES-Anwendung bis zu 15% bis 20% der Patienten nicht von DES zu profitieren scheinen, insbesondere in der älteren Bevölkerung.
In mehreren Studien wurde ein kurzer Zeitraum von 3 bis 6 Monaten mit einem längeren Zeitraum von 12 bis 24 Monaten verglichen.10-16 Eine gepoolte Analyse der ersten 4 Studien veröffentlichte Hinweise auf das Fehlen eines signifikanten Unterschieds bei ischämischen Ereignissen zwischen den kürzeren und längeren Zeiträumen, aber die Inzidenz von Blutungen war im längeren Zeitraum höher.17 Vor kurzem wurden drei weitere Studien vorgestellt, die sich mit kurzen und langen DAPT-Perioden befassen.14-16 Die SECURITY-Studie14 verglich 6-monatige mit 12-monatiger DAPT bei 1399 Niedrigrisikopatienten, die mit DES der zweiten Generation bei stabiler oder instabiler Angina pectoris behandelt wurden (Infarkt als Indikation für eine perkutane Koronarintervention wurde ausgeschlossen). Bei keinem der klinischen Endpunkte wurden nach 12 Monaten Unterschiede beobachtet. Die Haupteinschränkung war die Stichprobengröße, die geringe Einhaltung des Protokolls (34% der Patienten, die 6 Monaten zugewiesen wurden, setzten die DAPT nach 6 Monaten fort) und die Einbeziehung von anatomisch risikoreichen Patienten. In der ITALIC-Studie wurden 15 1894 Patienten mit nachgewiesener Nichtresistenz gegen Acetylsalicylsäure nach Implantation eines Xience® auf 6-monatige vs. 24-monatige DAPT randomisiert. stents. Bei keinem der klinischen Endpunkte, einschließlich Blutungskomplikationen, wurden Unterschiede festgestellt. Schließlich war die ISAR-SAFE-Studie 16, die noch nicht veröffentlicht wurde, für die Rekrutierung von 6000 Patienten geplant, wurde jedoch nach Einbeziehung von 4000 Patienten unterbrochen. Diese wurden randomisiert auf 6-Monats- oder 12-Monats-DAPT nach Implantation von DES (89% neue Generation). Auch hier wurden in keinem der Wirksamkeits- oder Sicherheitsendpunkte Unterschiede beobachtet.
Diese Studien weisen jedoch einige Einschränkungen auf. Da es sich um klinische Studien handelt, ist ihre klinische Repräsentativität begrenzt, die Einhaltung des Protokolls war unzureichend,10,14 DES der ersten Generation wurden verwendet,10,11,16 sowie BMS,10 Die Acetylsalicylsäureresistenz wurde vorgetestet,15 und die erste Version von Zotarolimus-eluierenden Stents mit einem späten Lumenverlust nahe dem von BMS wurden weit verbreitet oder sogar ausschließlich verwendet.10,12,13
Die große DAPT-Versuche25 bewertete eine DAPT-Periode von mehr als 12 Monaten nach der DES-Implantation. In dieser Studie wurden Patienten mit einem ereignislosen Zeitraum von 12 Monaten nach perkutaner Koronarintervention randomisiert zum Absetzen von DAPT zu diesem Zeitpunkt oder zu einem längeren Zeitraum von DAPT (bis zu 30 Monate). Patienten, die mit DES der ersten und zweiten Generation behandelt wurden, wurden eingeschlossen. Die längere DAPT-Periode (30 Monate) führte zu einer Abnahme der kardialen unerwünschten Ereignisse, aber zu einer Zunahme der Blutung im Vergleich zum 12-Monats-Zeitraum. Der DES-Typ erreichte jedoch die Interaktion für den Endpunkt (Hazard Ratio = 0,52 für den Paclitaxel-eluierenden Stent und Hazard Ratio = 0.89 für den Everolimus-eluierenden Stent mit P = .048 für die Interaktion).
Die klinischen Register zur Beurteilung des Thromboserisikos nach frühzeitigem DAPT-Entzug sind auch durch ihr retrospektives Design begrenzt.8,9 Verschiedene Vorurteile sind bemerkenswert, da der Abbruch der Behandlung nach sorgfältiger Abwägung des Thromboserisikos hätte entschieden werden können. Es fehlt an großen prospektiven Registern aus der Praxis, die kürzere DAPT-Zeiträume bewerten.
Schließlich ist ein wichtiges Merkmal, das die Anwendbarkeit eines kürzeren DAPT-Regimes einschränkt, dass Patienten in der Einstellung eines instabilen koronaren Ereignisses (die meisten Patienten, die sich heutzutage einer perkutanen Koronarintervention unterziehen) Profitieren Sie von einer 12-monatigen DAPT im Vergleich zu einer 1-monatigen Behandlungsperiode.18,19 Wir wissen jedoch nicht, ob dieser Nutzen erhalten bleibt, wenn ein 12-Monats-Regime mit einem 6-Monats-Regime verglichen wird. Daher bleibt die Diskussion offen und angemessen gestaltete prospektive Studien und / oder Register mit DES der aktuellen Generation sind gerechtfertigt.
Nach diesen Überlegungen haben wir versucht, dieses multizentrische prospektive ESTROFA-DAPT-Register zu entwerfen Bewertung eines 6-monatigen DAPT-Regimes. Die Einschlusskriterien wurden ausgewählt, um hauptsächlich Patienten mit stabiler koronarer Herzkrankheit einzubeziehen. In Bezug auf instabile Patienten schlossen wir nur solche mit instabiler Angina pectoris und ohne Anstieg der kardialen Marker ein. Wir schlossen auch Patienten mit Myokardinfarkt mit ST-Segmenterhöhung oder Myokardinfarkt ohne ST—Segmenterhöhung mit einem Blutungsrisiko ein, das nicht unbedingt die Notwendigkeit einer DES zugunsten einer BMS-Option ausschloss. Diese Algorithmen wurden jedoch nicht entwickelt oder standardisiert, um das Blutungsrisiko im Rahmen einer langfristigen DAPT vorherzusagen. Daher lag es im Ermessen der Ermittler, das Gleichgewicht zwischen Restenose und Blutungsrisiko zu berücksichtigen. In Bezug auf das Verfahren wurden Patienten mit Stents für linke Hauptkoronarläsionen sowie Bifurkationen, die mit einer 2-Stent-Strategie behandelt wurden, oder Patienten, die mehr als 3 Stents benötigten, ausgeschlossen, da in diesen Fällen ein erheblich höheres Risiko für eine Stentthrombose bestand10.
Um die Ergebnisse unserer Serie von 6-Monats- und 12-Monats-DAPT-Kohorten effektiv vergleichen zu können, verwendeten wir die 12-Monats-DAPT-Kohorte aus der ESTROFA-2-Studiendatenbank.22 Dieses zuvor veröffentlichte Register umfasste 4768 prospektiv eingeschriebene Patienten, die mit DES der zweiten Generation behandelt wurden, und darunter 4354 (91%), die mit einem 12-monatigen DAPT-Regime gemäß den zu diesem Zeitpunkt geltenden Richtlinien behandelt wurden.
Es wurden zwei Schritte befolgt, um vergleichbare Patientenserien aus diesen Registern zu erhalten. Zunächst wurden Patienten in ESTROFA-2, die Ausschlusskriterien für ESTROFA-DAPT aufwiesen, ausgeschlossen (insbesondere Patienten mit behandelten linken Hauptkoronarläsionen, Bifurkationen, die mit 2 Stents behandelt wurden, Patienten mit mehr als 3 implantierten Stents und Patienten mit einer späten DES-Thrombose in der Vorgeschichte). Zweitens wurde ein Propensity Score Matching-Prozess durchgeführt.
Schließlich wurden 2 vergleichbare Gruppen über alle klinischen und prozeduralen Merkmale hinweg in die Ergebnisanalyse einbezogen. In beiden Registern wurden nur DES der nicht ersten Generation mit einem ähnlichen Anteil für Everolimus-eluierende Stents aufgenommen. Das Zotarolimus-eluierende Stentmodell unterschied sich jedoch, wobei Endeavor® bei 12-monatiger DAPT (ESTROFA-2) und Resolute® bei 6-monatiger DAPT (ESTROFA-DAPT) verwendet wurde. Der Endeavor®-Stent, die erste Version von Zotarolimus-eluierenden Stents, zeigte einen späten Lumenverlust nahe dem von BMS (0,6 mm), während der Resolute®-Stent einen späten Lumenverlust von etwa 0,15 mm aufwies. Tatsächlich fanden die RESET- und OPTIMIZE-Studien keinen Unterschied zwischen 3-monatiger und 12-monatiger DAPT bei Verwendung des Endeavor®-Stents.12,13 Daher hätte dieser Differenzfaktor die Ergebnisse in der 6-Monats-DAPT-Gruppe negativ beeinflussen können, dies scheint jedoch nicht der Fall gewesen zu sein. Daher unterstützt dieser Unterschied die Ergebnisse des 6-Monats-DAPT-Ansatzes.
Einschränkungen
Eine wichtige Einschränkung unserer Studie ist der Mangel an Randomisierung. Register bringen das Problem der Verzerrung mit sich, die auf bekannte und unbekannte Störfaktoren zurückzuführen ist, die nach sorgfältiger statistischer Anpassung mit übereinstimmenden Analysen wie dem Propensity Score nicht immer berücksichtigt werden.
Obwohl randomisierte Studien das am besten geeignete Design für den Vergleich von Behandlungen sind, sind Register angesichts der allgemein anerkannten Vorbehalte randomisierter Studien nach wie vor eine wichtige Wissens- und Informationsquelle, z. B. kostenbegrenzende Stichprobengrößen, restriktive Einbeziehung über Ausschlusskriterien hinaus, nicht unabhängige Forschung oder kein „vollständiges“ Patientenmanagement und Follow-up.
Eine zweite Einschränkung ist die relativ geringe Stichprobengröße verschiedener Untergruppen, insbesondere der ACS-Untergruppe, die keine festen Rückschlüsse auf die kurzfristige DAPT-Sicherheit in diesen Einstellungen zulässt. Eine weitere Einschränkung ist die Art der Patientenauswahl. Wie in den „Methoden“ beschrieben, war die Studie hauptsächlich sicherheitsorientiert. Diejenigen Untergruppen mit einem nachgewiesenen Nutzen nach 12-monatiger DAPT (Patienten mit ACS ohne hohes Blutungsrisiko)18,19 und diejenigen mit einem höheren Thromboserisiko und einem Trend zum Nutzen bei längerer DAPT in Studien wurden systematisch ausgeschlossen.10
Eine wichtige Überlegung sind die unterschiedlichen Zeiträume für die Rekrutierung in beiden Registern. Der potenzielle Einfluss dieser Zeitlücke hätte jedoch durch die folgenden Faktoren abgeschwächt werden können: a) DES der neuen Generation wurden nur in beiden Registern verwendet; b) Nur mit Clopidogrel behandelte Patienten wurden in die Analyse einbezogen. Im neueren ESTROFA-DAPT-Register wurden die Patienten basierend auf den Einschlusskriterien nicht nach Protokoll mit neuen Thrombozytenaggregationshemmern behandelt (Patienten unter stabilen klinischen Bedingungen oder nach ACS, jedoch mit mäßig hohem Blutungsrisiko); c) Die Methodik beider Register war ziemlich ähnlich, wie zuvor im Abschnitt „Methoden“ erwähnt.
SCHLUSSFOLGERUNGEN
Eine 6-monatige DAPT-Periode nach Implantation von DES der neuen Generation scheint einer 12-monatigen DAPT-Therapie im klinischen und angiographischen Kontext, der in dieser multizentrischen Studie untersucht wurde, nicht unterlegen zu sein.
FINANZIERUNG
Diese Studie wurde von der spanischen Arbeitsgruppe für interventionelle Kardiologie für webbasierte Fallberichtsformulare (CRF) der Spanischen Gesellschaft für Kardiologie finanziert.
INTERESSENKONFLIKTE
Keine deklariert.