oppimistavoitteet
- aineenvaihdunta
- katabolinen reaktio
- anabolinen reaktio
- entsyymi
- substraatti
- Apoentsyymi
- Haloentsyymi
- kofaktori (koentsyymi)
- entsyymipitoisuus
- substraattipitoisuus
- lämpötila
- pH
- suolapitoisuus
elääkseen, kasvaakseen ja lisääntyäkseen mikro-organismit käyvät läpi erilaisia kemiallisia muutoksia. Ne muuttavat ravinteita, jotta ne pääsevät soluun, ja ne muuttavat niitä, kun ne tulevat soluun, syntetisoidakseen solun osia ja saadakseen energiaa. Aineenvaihdunnalla tarkoitetaan kaikkia solun järjestyneitä kemiallisia reaktioita. Reaktioita, joissa kemialliset yhdisteet hajoavat, kutsutaan katabolisiksi reaktioiksi, kun taas reaktioita, joissa kemiallisia yhdisteitä syntetisoidaan, kutsutaan anabolisiksi reaktioiksi. Kaikki nämä reaktiot ovat entsyymien valvonnassa.

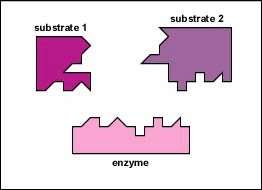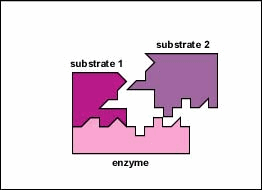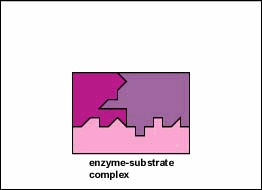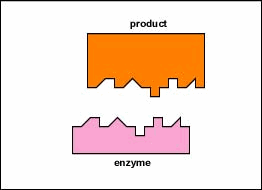
entsyymit ovat solussa pieninä määrinä esiintyviä aineita, jotka toimivat nopeuttamaan tai katalysoimaan kemiallisia reaktioita. Entsyymin pinnalla on yleensä pieni rako, joka toimii aktiivisena kohtana tai katalyyttinä, johon yksi tai kaksi spesifistä substraattia pystyy sitoutumaan. (Kaikkea, mihin entsyymi normaalisti yhdistyy, kutsutaan substraatiksi.) Substraatin sitoutuminen entsyymiin saa taipuisan entsyymin muuttamaan hieman muotoaan indusoidun sovituksen kautta muodostaen tempore-välituotteen, jota kutsutaan entsyymi-substraattikompleksiksi (Kuva \(\PageIndex{1}\)).
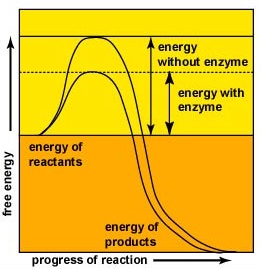
entsyymit nopeuttavat kemiallisten reaktioiden nopeutta, koska ne alentavat aktivointienergiaa, energiaa, joka on syötettävä, jotta molekyylit voivat reagoida keskenään (Kuva \(\PageIndex{2}\)). Entsyymit alentavat aktivoitumisenergiaa muodostamalla entsyymi-substraattikompleksin, joka mahdollistaa entsyymireaktion tuotteiden muodostamisen ja vapautumisen (Kuva \(\PageIndex{3}\)).
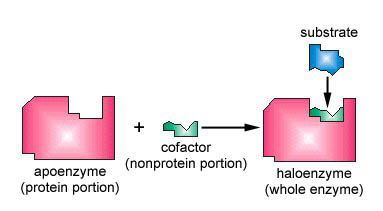
monet entsyymit tarvitsevat nonproteiinikofaktorin avustamaan niitä reaktiossaan. Tällöin entsyymin proteiiniosa, jota kutsutaan apoentsyymiksi, yhdistyy kofaktorin kanssa muodostaen koko entsyymin tai haloentsyymin (Kuva \(\PageIndex{3}\)). Jotkut kofaktorit ovat ioneja, kuten Ca++, Mg++ ja K+; muut kofaktorit ovat orgaanisia molekyylejä eli koentsyymejä, jotka toimivat kemiallisten ryhmien tai elektronien kantajina. Nad+, NADP+, FAD ja koentsyymi A (CoA) ovat esimerkkejä koentsyymeistä.
entsyymien ominaisuudet
kemiallisesti entsyymit ovat yleensä pallomaisia proteiineja. (Jotkut ribotsyymeiksi kutsutut RNA-molekyylit voivat olla myös entsyymejä. Näitä on yleensä solujen ydinalueella ja ne katalysoivat RNA-molekyylien pilkkoutumista). Entsyymit ovat katalyyttejä, jotka hajottavat tai syntetisoivat monimutkaisempia kemiallisia yhdisteitä. Niiden avulla kemialliset reaktiot voivat tapahtua riittävän nopeasti ylläpitääkseen elämää. Entsyymit nopeuttavat kemiallisten reaktioiden nopeutta, koska ne alentavat aktivointienergiaa, energiaa, jota molekyylien on syötettävä, jotta ne voivat reagoida keskenään. Kaikkea, mihin entsyymi tavallisesti yhdistyy, kutsutaan substraatiksi. Entsyymit ovat hyvin tehokkaita. Entsyymi voi tyypillisesti katalysoida 1-10 000 substraattimolekyyliä sekunnissa. Entsyymejä on solussa vain pieniä määriä, koska ne eivät muutu reaktioidensa aikana. ja ne ovat erittäin spesifisiä alustalleen. Yleensä kullekin spesifiselle kemialliselle reaktiolle on olemassa yksi spesifinen entsyymi.
Entsyymiaktiivisuuteen
Entsyymiaktiivisuuteen vaikuttavat useat tekijät, mm.:
- entsyymipitoisuus: Olettaen, että substraattia on riittävästi, entsyymipitoisuuden lisääminen nostaa entsyymin reaktionopeutta.
- substraatin pitoisuus: kun entsyymipitoisuus on vakio ja substraattien pitoisuus pienempi, substraattipitoisuus on rajoittava tekijä. Substraattipitoisuuden kasvaessa entsyymin reaktionopeus kasvaa. Hyvin suurilla substraattipitoisuuksilla entsyymit kuitenkin kyllästyvät substraattiin eikä substraatin suurempi pitoisuus lisää reaktionopeutta.
- lämpötila: Jokaisella entsyymillä on optimaalinen lämpötila, jossa se toimii parhaiten. Korkeampi lämpötila johtaa yleensä entsyymiaktiivisuuden lisääntymiseen. Lämpötilan noustessa molekyylien liike kasvaa, mikä johtaa useampiin molekyylien törmäyksiin. Jos lämpötila kuitenkin nousee tietyn pisteen yläpuolelle, lämpö denaturoi entsyymin, jolloin se menettää kolmiulotteisen funktionaalisen muotonsa denaturoimalla vetysidoksensa. Kylmä lämpötila taas hidastaa entsyymien toimintaa vähentämällä molekyylien liikettä.
- pH: Jokaisella entsyymillä on optimaalinen pH, joka auttaa säilyttämään kolmiulotteisen muotonsa. PH: n muutokset voivat denaturoida entsyymejä muuttamalla entsyymin varausta. Tämä muuttaa entsyymin ionisidoksia, jotka vaikuttavat sen toiminnalliseen muotoon.
- suolapitoisuus: kullakin entsyymillä on optimaalinen suolapitoisuus. Suolapitoisuuden muutokset voivat myös denaturoida entsyymejä.
jotkin bakteerien entsyymien väliset suhteet sekä desinfiointiaineiden ja äärilämpötilojen käyttö bakteerien torjunnassa.
- monet desinfiointiaineet, kuten kloori, jodi, jodoforit, merkuriaalit, hopeanitraatti, formaldehydi ja etyleenioksidi, inaktivoivat bakteerien entsyymejä ja siten estävät aineenvaihduntaa.
- korkeat lämpötilat, kuten autoklavointi, kiehuminen ja pastörointi, denatuuriproteiinit ja entsyymit.
- kylmät lämpötilat, kuten jäähdytys ja jäätyminen, hidastavat tai pysäyttävät entsyymireaktioita.
Yhteenveto
- entsyymit ovat pieniä määriä solussa esiintyviä aineita, jotka toimivat nopeuttamaan tai katalysoimaan kemiallisia reaktioita niin, että ne tapahtuvat riittävän nopeasti ylläpitääkseen elämää.
- entsyymin pinnalla on tyypillisesti pieni rako, joka toimii aktiivisena tai katalyyttisenä kohtana, johon yksi tai kaksi spesifistä substraattia pystyy sitoutumaan.
- kaikkea, mihin entsyymi tavallisesti yhdistyy, kutsutaan substraatiksi.
- substraatin sitoutuminen entsyymiin saa taipuisan entsyymin muuttamaan hieman muotoaan indusoiduksi fit-prosessiksi kutsutun prosessin kautta muodostaen väliaikaisen välivaiheen, jota kutsutaan entsyymi-substraattikompleksiksi.
- entsyymit nopeuttavat kemiallisten reaktioiden nopeutta, koska ne alentavat aktivaatioenergiaa, energiaa, jota molekyylien on syötettävä, jotta ne voivat reagoida keskenään.
- monet entsyymit tarvitsevat nonproteiinikofaktorin avustamaan niitä reaktiossaan. Tällöin apoentsyymiksi kutsuttu entsyymin proteiiniosa yhdistyy kofaktorin kanssa muodostaen koko entsyymin eli haloentsyymin.
- jotkut kofaktorit ovat ioneja, kuten Ca++, Mg++ ja K+; muut kofaktorit ovat orgaanisia molekyylejä, joita kutsutaan koentsyymeiksi, jotka toimivat kemiallisten ryhmien tai elektronien kantajina. Nad+, NADP+, FAD ja koentsyymi A (CoA) ovat esimerkkejä koentsyymeistä.
- kemiallisesti entsyymit ovat yleensä pallomaisia proteiineja. Jotkut ribotsyymeiksi kutsutut RNA-molekyylit voivat olla myös entsyymejä, jotka yleensä toimivat hajottamaan RNA-molekyylejä.
- entsyymejä on solussa vain pieniä määriä, koska ne eivät muutu reaktioissaan ja ovat erittäin spesifisiä substraatilleen.
- entsyymin aktiivisuuteen vaikuttavat useat tekijät, kuten entsyymipitoisuus, substraatin pitoisuus, lämpötila, pH ja suolapitoisuus.
maksajat ja käyttöön otetut määrät
-
Gary Kaiser (COMMUNITY COLLEGE of BALTIMORE COUNTY, CATONSVILLE CAMPUS)