Objectifs d’apprentissage
- Définir ou décrire les éléments suivants:
- métabolisme
- réaction catabolique
- réaction anabolique
- enzyme
- substrat
- apoenzyme
- haloenzyme
- cofacteur (coenzyme)
- Indiquez comment les enzymes sont capables d’accélérer le taux de réactions chimiques.
- Décrire brièvement une réaction enzyme-substrat généralisée, énoncer la fonction du site actif d’une enzyme et décrire comment une enzyme est capable d’accélérer les réactions chimiques.
- Énoncent quatre caractéristiques des enzymes.
- Indiquez comment les éléments suivants affectent la vitesse d’une réaction enzymatique.
- concentration enzymatique
- concentration en substrat
- température
- pH
- concentration en sel
- Indiquez comment des produits chimiques tels que le chlore, l’iode, les iodophores, les mercuriaux et l’oxyde d’éthylène inhibent ou tuent les bactéries.
- Indiquez comment les températures élevées et basses exercent leur effet sur les bactéries.
Pour vivre, grandir et se reproduire, les micro-organismes subissent une variété de changements chimiques. Ils modifient les nutriments pour qu’ils puissent entrer dans la cellule et ils les changent une fois qu’ils entrent afin de synthétiser des parties cellulaires et d’obtenir de l’énergie. Le métabolisme fait référence à toutes les réactions chimiques organisées dans une cellule. Les réactions dans lesquelles des composés chimiques sont décomposés sont appelées réactions cataboliques tandis que les réactions dans lesquelles des composés chimiques sont synthétisés sont appelées réactions anaboliques. Toutes ces réactions sont sous le contrôle des enzymes.

Les enzymes sont des substances présentes dans la cellule en petites quantités qui fonctionnent pour accélérer ou catalyser les réactions chimiques. À la surface de l’enzyme se trouve généralement une petite crevasse qui fonctionne comme un site actif ou un site catalytique auquel un ou deux substrats spécifiques sont capables de se lier. (Tout ce avec quoi une enzyme se combine normalement est appelé substrat.) La liaison du substrat à l’enzyme fait que l’enzyme flexible change légèrement de forme par un processus appelé ajustement induit pour former un intermédiaire temporé appelé complexe enzyme-substrat (Figure \(\PageIndex{1}\)).
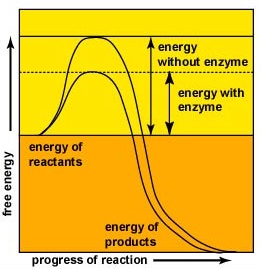
Les enzymes accélèrent la vitesse des réactions chimiques car elles abaissent l’énergie d’activation, l’énergie qui doit être fournie pour que les molécules réagissent entre elles (Figure \(\PageIndex{2}\)). Les enzymes abaissent l’énergie d’activation en formant un complexe enzyme-substrat permettant la formation et la libération de produits de la réaction enzymatique (Figure \(\PageIndex{3}\)).
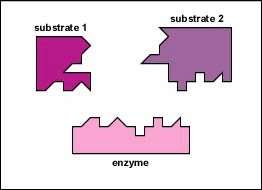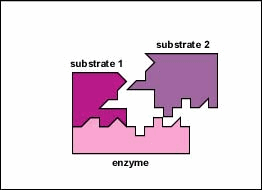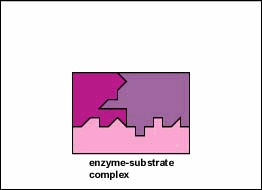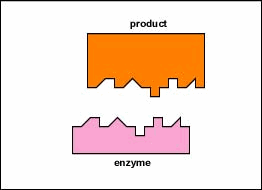
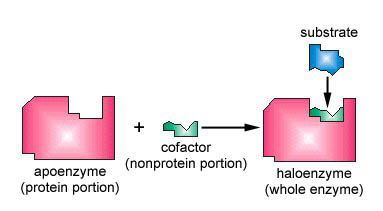
De nombreuses enzymes ont besoin d’un cofacteur non protéique pour les aider dans leur réaction. Dans ce cas, la partie protéique de l’enzyme, appelée apoenzyme, se combine avec le cofacteur pour former l’enzyme entière ou l’halogénoenzyme (Figure \(\PageIndex{3}\)). Certains cofacteurs sont des ions tels que Ca++, Mg++ et K+; d’autres cofacteurs sont des molécules organiques appelées coenzymes qui servent de supports pour des groupes chimiques ou des électrons. NAD+, NADP+, FAD et coenzyme A (CoA) sont des exemples de coenzymes.
Caractéristiques des enzymes
Chimiquement, les enzymes sont généralement des protéines globulaires. (Certaines molécules d’ARN appelées ribozymes peuvent également être des enzymes. Ceux-ci se trouvent généralement dans la région nucléaire des cellules et catalysent la division des molécules d’ARN). Les enzymes sont des catalyseurs qui décomposent ou synthétisent des composés chimiques plus complexes. Ils permettent aux réactions chimiques de se produire assez rapidement pour soutenir la vie. Les enzymes accélèrent la vitesse des réactions chimiques car elles diminuent l’énergie d’activation, l’énergie qui doit être fournie pour que les molécules réagissent entre elles. Tout ce avec quoi une enzyme se combine normalement est appelé substrat. Les enzymes sont très efficaces. Une enzyme peut généralement catalyser entre 1 et 10 000 molécules de substrat par seconde. Les enzymes ne sont présentes qu’en petites quantités dans la cellule car elles ne sont pas altérées lors de leurs réactions. et ils sont très spécifiques pour leur substrat. Il existe généralement une enzyme spécifique pour chaque réaction chimique spécifique.
Activité enzymatique
L’activité enzymatique est affectée par un certain nombre de facteurs, notamment:
- La concentration de l’enzyme: En supposant qu’une concentration suffisante de substrat soit disponible, l’augmentation de la concentration enzymatique augmentera la vitesse de réaction enzymatique.
- La concentration du substrat: À une concentration enzymatique constante et à des concentrations plus faibles de substrats, la concentration du substrat est le facteur limitant. À mesure que la concentration en substrat augmente, la vitesse de réaction enzymatique augmente. Cependant, à des concentrations de substrat très élevées, les enzymes deviennent saturées de substrat et une concentration plus élevée de substrat n’augmente pas la vitesse de réaction.
- La température: Chaque enzyme a une température optimale à laquelle elle fonctionne le mieux. Une température plus élevée entraîne généralement une augmentation de l’activité enzymatique. À mesure que la température augmente, le mouvement moléculaire augmente, ce qui entraîne plus de collisions moléculaires. Cependant, si la température dépasse un certain point, la chaleur dénaturera l’enzyme, lui faisant perdre sa forme fonctionnelle tridimensionnelle en dénaturant ses liaisons hydrogène. La température froide, en revanche, ralentit l’activité enzymatique en diminuant le mouvement moléculaire.
- Le pH: Chaque enzyme a un pH optimal qui aide à maintenir sa forme tridimensionnelle. Les changements de pH peuvent dénaturer les enzymes en modifiant la charge de l’enzyme. Cela modifie les liaisons ioniques de l’enzyme qui contribuent à sa forme fonctionnelle.
- La concentration en sel: Chaque enzyme a une concentration en sel optimale. Des changements dans la concentration en sel peuvent également dénaturer les enzymes.
Certaines relations entre les enzymes bactériennes et l’utilisation de désinfectants et les températures extrêmes pour contrôler les bactéries.
- De nombreux désinfectants, tels que le chlore, l’iode, les iodophores, les mercuriels, le nitrate d’argent, le formaldéhyde et l’oxyde d’éthylène, inactivent les enzymes bactériennes et bloquent ainsi le métabolisme.
- Températures élevées, telles que l’autoclavage, l’ébullition et la pasteurisation, la dénature des protéines et des enzymes.
- Les températures froides, telles que la réfrigération et la congélation, ralentissent ou arrêtent les réactions enzymatiques.
Résumé
- Les enzymes sont des substances présentes dans la cellule en petites quantités qui fonctionnent pour accélérer ou catalyser les réactions chimiques afin qu’elles se produisent suffisamment rapidement pour soutenir la vie.
- À la surface de l’enzyme se trouve généralement une petite crevasse qui fonctionne comme un site actif ou un site catalytique auquel un ou deux substrats spécifiques peuvent se lier.
- Tout ce avec quoi une enzyme se combine normalement est appelé substrat.
- La liaison du substrat à l’enzyme amène l’enzyme flexible à changer légèrement de forme par un processus appelé ajustement induit pour former un intermédiaire temporaire appelé complexe enzyme-substrat.
- Les enzymes accélèrent la vitesse des réactions chimiques car elles abaissent l’énergie d’activation, l’énergie qui doit être fournie pour que les molécules réagissent entre elles.
- De nombreuses enzymes ont besoin d’un cofacteur non protéique pour les aider dans leur réaction. Dans ce cas, la partie protéique de l’enzyme, appelée apoenzyme, se combine avec le cofacteur pour former l’enzyme entière ou l’haloenzyme.
- Certains cofacteurs sont des ions tels que Ca++, Mg++ et K +; d’autres cofacteurs sont des molécules organiques appelées coenzymes qui servent de supports pour des groupes chimiques ou des électrons. NAD+, NADP+, FAD et coenzyme A (CoA) sont des exemples de coenzymes.
- Chimiquement, les enzymes sont généralement des protéines globulaires. Certaines molécules d’ARN appelées ribozymes peuvent également être des enzymes, fonctionnant généralement pour cliver les molécules d’ARN.
- Les enzymes ne sont présentes qu’en petites quantités dans la cellule car elles ne sont pas altérées au cours de leurs réactions et sont très spécifiques de leur substrat.
- L’activité enzymatique est affectée par un certain nombre de facteurs, notamment la concentration de l’enzyme, la concentration du substrat, la température, le pH et la concentration en sel.
Contributeurs et Attributions
-
Dr. Gary Kaiser (COLLÈGE COMMUNAUTAIRE DU COMTÉ DE BALTIMORE, CAMPUS DE CATONSVILLE)