Nom générique: sulfacétamide sodique, soufre
Forme posologique: crème
Revue médicale par Drugs.com . Dernière mise à jour le 1er janvier 2021.
- Effets secondaires
- Dosage
- Professionnel
- Interactions
- Plus
Avertissement: Ce médicament n’a pas été jugé sûr et efficace par la FDA, et cet étiquetage n’a pas été approuvé par la FDA. Pour plus d’informations sur les médicaments non approuvés, cliquez ici.
Rx Uniquement
POUR USAGE EXTERNE UNIQUEMENT. PAS POUR USAGE OPHTALMIQUE.
DESCRIPTION:
Chaque gramme contient 100 mg de sulfacétamide de sodium et 50 mg de soufre colloïdal dans un véhicule constitué de: alcool benzylique, alcool cétylique, EDTA disodique, parfum, stéarate de glycéryle (et) stéarate de PEG-100, silicate de magnésium et d’aluminium, distéarate de PEG-150, phénoxyéthanol, polyéthylène glycol 400, eau purifiée, laurylsulfate de sodium, sodium thiosulfate, alcool stéarylique et gomme xanthane.
Le sulfacétamide de sodium est un sulfonamide à activité antibactérienne tandis que le soufre agit comme agent kératolytique. Le sulfacétamide de sodium est C 8H 9N 2NaO 3S * H 2O avec un poids moléculaire de 254,24. Chimiquement, le sulfacétamide de sodium est le N- acétamide, sel monosodique, monohydraté. La formule structurelle est:
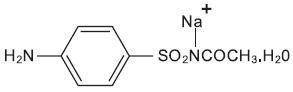
Le sulfacétamide de sodium est une poudre cristalline blanche inodore au goût amer. Il est librement soluble dans l’eau, peu soluble dans l’alcool, alors qu’il est pratiquement insoluble dans le benzène, le chloroforme et l’éther.
PHARMACOLOGIE CLINIQUE:
Le sulfacétamide de sodium exerce un effet bactériostatique contre les microorganismes sensibles aux sulfamides à Gram positif et à Gram négatif couramment isolés des infections pyogènes cutanées secondaires. Il agit en limitant la synthèse de l’acide folique requise par les bactéries pour la croissance, par sa concurrence avec l’acide para-aminobenzoïque. Il n’existe pas de données cliniques disponibles sur le degré et le taux d’absorption systémique de ce produit lorsqu’il est appliqué sur la peau ou le cuir chevelu. Cependant, une absorption significative du sulfacétamide de sodium par la peau a été rapportée.
Les données in vitro suivantes sont disponibles mais la signification clinique est inconnue. Les organismes sensibles au sulfacétamide sodique sont les suivants: Streptocoques, Staphylocoques, E. coli, Klebsiella pneumoniae, Pseudomonas pyocyanea, espèces de Salmonelles, Proteus vulgaris, Nocardia et Actinomyces.
Le mode d’action exact du soufre dans le traitement de l’acné est inconnu, mais il a été rapporté qu’il inhibe la croissance de Propionibacterium acnes et la formation d’acides gras libres.
INDICATIONS:
Ce produit est indiqué pour le contrôle topique de l’acné vulgaire, de l’acné rosacée et de la dermatite séborrhéique.
CONTRE-INDICATIONS:
Ce produit est contre-indiqué chez les personnes présentant une hypersensibilité connue ou soupçonnée à l’un des ingrédients du produit. Ce produit ne doit pas être utilisé par les patients atteints d’une maladie rénale.
MISES EN GARDE:
Les sulfamides sont connus pour provoquer le syndrome de Stevens-Johnson chez les personnes hypersensibles. Le syndrome de Stevens-Johnson a également été rapporté suite à l’utilisation de sulfacétamide de sodium par voie topique. Des cas de lupus érythémateux disséminé d’origine médicamenteuse à partir de sulfacétamide topique ont également été rapportés. Dans l’un de ces cas, il y a eu une issue fatale.
TENIR HORS DE LA PORTÉE DES ENFANTS.
PRÉCAUTIONS:
POUR USAGE EXTERNE UNIQUEMENT. PAS POUR USAGE OPHTALMIQUE.
Généralités: Les organismes non sensibles, y compris les champignons, peuvent proliférer avec l’utilisation de cette préparation.
Bien que rare, une sensibilité au sulfacétamide de sodium peut survenir. Par conséquent, la prudence et une surveillance attentive doivent être observées lors de la prescription de ce médicament pour les patients qui peuvent être sujets à une hypersensibilité aux sulfamides topiques. Si l’utilisation de ce produit produit des signes d’hypersensibilité ou d’autres réactions indésirables, arrêtez l’utilisation de la préparation. Les patients doivent être soigneusement observés pour une éventuelle irritation ou sensibilisation locale pendant le traitement à long terme. Les réactions toxiques systémiques telles que l’agranulocytose, l’anémie hémolytique aiguë, le purpura hémorragique, la fièvre médicamenteuse, la jaunisse et la dermatite de contact indiquent une hypersensibilité aux sulfamides. Une prudence particulière doit être utilisée si des zones de peau dénudée ou abrasée sont impliquées. L’absorption systémique des sulfamides topiques est plus importante après l’application sur de grandes zones infectées, abrasées, dénudées ou gravement brûlées. Dans ces circonstances, l’un des effets indésirables produits par l’administration systémique de ces agents pourrait potentiellement se produire, et des observations et des déterminations de laboratoire appropriées devraient être effectuées.
Le but de cette thérapie est d’obtenir une desquamation sans irritation, mais le sulfacétamide de sodium et le soufre peuvent provoquer une rougeur et une desquamation de l’épiderme. Ces effets secondaires ne sont pas inhabituels dans le traitement de l’acné vulgaire, mais les patients doivent être avertis de la possibilité.
Information pour les patients: Les patients doivent cesser l’utilisation de ce produit si l’état s’aggrave ou si une éruption cutanée se développe dans la zone traitée ou ailleurs. L’utilisation de ce produit doit également être interrompue rapidement et le médecin averti en cas d’arthrite, de fièvre ou de plaies dans la bouche. Évitez le contact avec les yeux, les lèvres et les muqueuses.
Interactions médicamenteuses: Ce produit est incompatible avec les préparations à base d’argent.
Carcinogenèse, Mutagénèse et Altération de la fertilité : Aucune étude à long terme sur le potentiel carcinogène chez l’animal n’a été réalisée sur ce produit à ce jour. Des études sur la reproduction et la fertilité n’ont pas non plus été réalisées. Une non-disjonction chromosomique a été rapportée chez la levure Saccharomyces cerevisiae, après application de sulfacétamide de sodium. La signification de cette découverte pour l’utilisation topique du sulfacétamide de sodium chez l’homme est inconnue.
Grossesse : Catégorie C. Aucune étude de reproduction animale n’a été menée avec ce produit. On ne sait pas non plus si ce produit peut affecter la capacité de reproduction ou causer des dommages fœtaux lorsqu’il est administré à une femme enceinte. Ce produit ne doit être utilisé par une femme enceinte que si cela est clairement nécessaire ou lorsque les avantages potentiels l’emportent sur les dangers potentiels pour le fœtus.
Mères allaitantes: On ne sait pas si ce médicament est excrété dans le lait maternel. Étant donné que de nombreux médicaments sont excrétés dans le lait maternel, il convient de faire preuve de prudence lorsque ce produit est administré à une femme qui allaite.
Utilisation pédiatrique: L’innocuité et l’efficacité chez les enfants de moins de 12 ans n’ont pas été établies.
EFFETS INDÉSIRABLES:
Les rapports d’irritation et d’hypersensibilité au sulfacétamide de sodium sont peu fréquents. Les effets indésirables suivants, rapportés après administration de sulfacétamide de sodium ophtalmique stérile, sont à noter: cas de syndrome de Stevens-Johnson et cas d’hypersensibilité locale qui ont évolué vers un syndrome ressemblant à un lupus érythémateux disséminé; dans un cas, une issue fatale a été rapportée (voir MISES en GARDE).
SURDOSAGE:
La DL 50 orale du sulfacétamide chez la souris est de 16,5 g/kg. En cas de surdosage, un traitement d’urgence doit être commencé immédiatement.
Manifestations: Un surdosage peut provoquer des nausées et des vomissements. Un surdosage oral important peut provoquer une hématurie, une cristallurie et un arrêt rénal en raison de la précipitation de cristaux de sulfamides dans les tubules rénaux et les voies urinaires. Pour le traitement, contactez votre centre antipoison local ou votre médecin.
POSOLOGIE ET ADMINISTRATION:
Nettoyer les zones touchées. Appliquez une fine couche sur les zones touchées en massant légèrement, 1 à 3 fois par jour ou selon les directives d’un médecin.
STOCKAGE:
Conserver entre 20 ° C et 25 ° C (68 ° F à 77 ° F), excursions autorisées entre 15 ° C et 30 ° C (entre 59 ° F et 86 ° F). Une brève exposition à des températures allant jusqu’à 40 ° C (104 ° F) peut être tolérée à condition que la température cinétique moyenne ne dépasse pas 25 ° C (77 ° F); cependant, une telle exposition doit être minimisée.
AVIS: Protéger du gel et de la chaleur excessive. Le produit peut avoir tendance à s’assombrir légèrement au stockage. Une légère décoloration n’altère pas l’efficacité ou la sécurité du produit. Gardez la bouteille bien fermée.
De temps en temps, une légère décoloration du tissu peut se produire lorsqu’une quantité excessive du produit est utilisée et entre en contact avec des tissus blancs. Cette décoloration ne pose cependant aucun problème, car elle est facilement éliminée par blanchiment ordinaire sans blanchiment.
COMMENT FOURNI:
Ce produit est fourni dans la (les) taille(s) suivante(s):
2 oz. (57 g) bouteilles, NDC 0178-0470-02
Pour signaler un événement indésirable grave ou obtenir des renseignements sur le produit, composez le 1-800-298-1087.
Fabriqué pour:
MISSION PHARMACAL COMPANY
San Antonio, TX 78230 1355
| AVAR-E sulfacétamide sodique, crème au soufre |
||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||
Étiqueteuse – Mission Pharmacal Company (008117095)
En savoir plus sur Avar-E (sulfacétamide sodique / sulfur topique)
- Effets secondaires
- Informations posologiques
- Interactions médicamenteuses
- Prix & Coupons
- Classe de médicaments: antibiotiques topiques
Ressources professionnelles
- Informations sur la prescription
Autres marques Sulfacleanse 8/4, Le Plexion, la Sumaxine, le nettoyant au Rosanil, … +23 plus
Autres formulations
- Avar
- … + 4 plus
Guides de traitement connexes
- Acné
- Rosacée
- Dermatite séborrhéique
Avertissement médical