Reazione: Idratazione di alchini
Come con gli alcheni,l’idratazione (aggiunta di acqua) agli alchini richiede un acido forte, solitamente acido solforico, ed è facilitata dal solfato mercurico. Tuttavia, a differenza delle aggiunte ai doppi legami che danno prodotti alcolici, l’aggiunta di acqua agli alchini dà prodotti chetonici ( ad eccezione dell’acetilene che produce acetaldeide ). La spiegazione di questa deviazione sta nella tautomerizzazione enol-cheto, illustrata dalla seguente equazione. Il prodotto iniziale dall’aggiunta di acqua ad un alchino è un enolo (un composto avente un sostituente idrossile attaccato ad un doppio legame), e questo si riorganizza immediatamente al tautomero cheto più stabile.
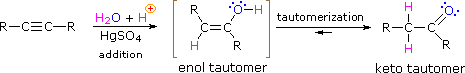
I tautomeri sono definiti come isomeri costituzionali interconversi rapidamente, solitamente distinti da una diversa posizione di legame per un atomo di idrogeno labile (colorato in rosso qui) e un doppio legame situato in modo diverso. L’equilibrio tra i tautomeri non è solo rapido in condizioni normali, ma spesso favorisce fortemente uno degli isomeri ( l’acetone, ad esempio, è il 99,999% del tautomero cheto ). Anche in tali equilibri unilaterali, la prova della presenza del tautomero minore deriva dal comportamento chimico del composto. Gli equilibri tautomerici sono catalizzati da tracce di acidi o basi che sono generalmente presenti nella maggior parte dei campioni chimici. I tre esempi riportati di seguito illustrano queste reazioni per diverse sostituzioni del triplo legame. La fase di tautomerizzazione è indicata da una freccia rossa. Per gli alchini terminali l’aggiunta di acqua segue la regola di Markovnikov, come nel secondo esempio seguente, e il prodotto finale è un metilchetone ( ad eccezione dell’acetilene, mostrato nel primo esempio ). Per gli alchini interni (il triplo legame è all’interno di una catena più lunga ) l’aggiunta di acqua non è regioselettiva. Se il triplo legame non si trova simmetricamente (cioè se R & R ‘ nella terza equazione non sono uguali) si formeranno due chetoni isomerici.
HC≡CH + H2O + HgSO4 & H2SO4 –> –> H3C-CH=O
RC≡CH + H2O + HgSO4 & H2SO4 –> –> RC(=O)CH3
RC≡CR’ + H2O + HgSO4 & H2SO4 –> –> RCH2-C(=O)R’ + RC(=O)-CH2R’
Con l’aggiunta di acqua, alchini può essere idratata per formare enols che spontaneamente tautomerize di chetoni. La reazione è catalizzata da ioni di mercurio. Segue la regola di Markovnikov: Gli alchini terminali danno metilchetoni
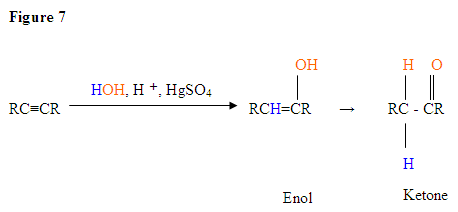
- Il primo passo è una reazione acido / base in cui gli elettroni π del triplo legame agiscono come una base di Lewis e attaccano il protone protendendo quindi il carbonio con il maggior numero di sostituenti di idrogeno.
- Il secondo passo è l’attacco della molecola d’acqua nucleofila sul carbocation elettrofilo, che crea uno ox ossonio.
- Successivamente si deprotona da una base, generando un alcol chiamato enolo, che poi si tautomerizza in un chetone.
- Il tautomerismo è uno spostamento simultaneo del protone e del doppio legame, che va dalla forma enol alla forma isomero cheto come mostrato sopra nella Figura 7.
Ora diamo un’occhiata ad alcune reazioni di idratazione.
L’idratazione dell’alchino terminale produce metilchetoni
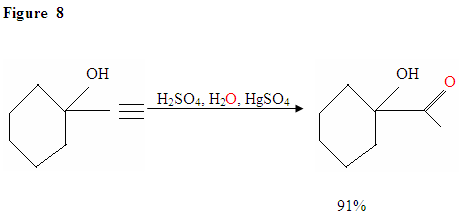
Proprio come descritto in Figura 7 gli elettroni π attaccheranno un protone, formando una carbocation, che poi viene attaccata dalle molecole d’acqua nucleofili. Dopo la deprotinazione, generiamo un enolo, che poi tautomerizza nella forma chetonica mostrata.
Idratazione di Alchini
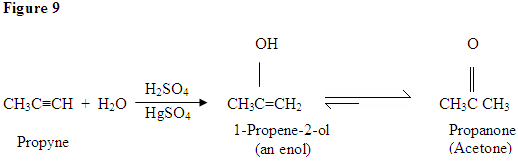
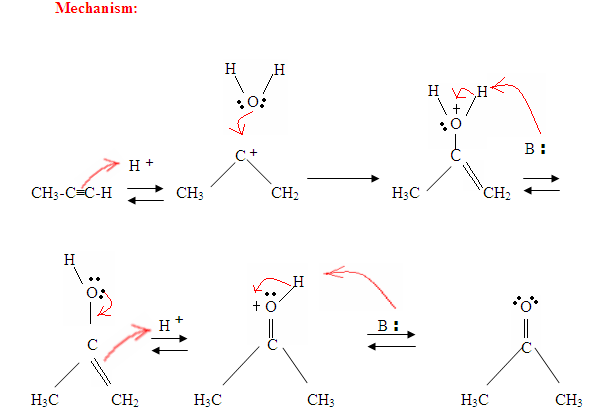
Come si può vedere qui, π elettroni del triplo legame stanno attaccando il protone, che forma un legame covalente con la fibra di carbonio con la maggior parte di idrogeno sostituenti. Una volta che l’idrogeno è legato si ha un carbocation, che viene attaccato dalla molecola d’acqua. Ora hai una carica positiva sull’ossigeno che si traduce in una base che entra e deprotina la molecola. Una volta deprotinato, hai un enol, che poi viene tautomerizzato.
Il tautomerismo è mostrato qui quando il protone viene attaccato dagli elettroni del doppio legame π che formano un legame covalente tra il carbonio e l’idrogeno sul carbonio meno sostituito. Gli elettroni dell’ossigeno finiscono per spostarsi verso il carbonio, formando un doppio legame con il carbonio e dandosi una carica positiva, che poi viene attaccata dalla base. La base deprotina l’ossigeno con conseguente prodotto finale più stabile all’equilibrio, che è un chetone.
Esercizio \(\PageIndex{1}\)
- Disegnare la struttura del prodotto formato quando ciascuna delle sostanze sottostanti viene trattata con H2O / H2SO4 in presenza di HgSO4.
- $ \ ce{\sf {CH3-CH2-C # C-H}}$
-
- Disegna la struttura della forma cheto del composto mostrato di seguito. Quale forma ti aspetteresti di essere la più stabile?
Risposta
Risposte:
La cheto modulo dovrebbe essere il più stabile.
Domande
Q9.4.1
Con quale alkyne inizieresti per ottenere i seguenti prodotti, in una reazione di ossidazione? Tieni a mente la risonanza.

Q9. 4.2
Proporre uno schema di reazione per il seguente composto partendo dall’alchino e mostrando i reagenti e gli intermedi necessari.

Soluzioni
S9.4.1

S9.4.2
