Miglia F. Greenwald, BS, Brittni A. Scruggs, MD, PhD, Jesse M. Vislisel, MD, Marco A. Greiner, MD
19 ottobre 2016
Introduzione
tecniche di Imaging per valutare la struttura e la funzione della cornea e del segmento anteriore sono fondamentali per la diagnosi e il trattamento di un’ampia varietà di malattie oculari. C’è una grande varietà di test diagnostici disponibili per gli oftalmologi, e imparare a interpretare questi test può sembrare scoraggiante. Per coloro che iniziano la formazione in oftalmologia, l’utilizzo di test diagnostici comuni fornisce una diagnosi e una gestione più rapide e accurate delle malattie corneali. L’obiettivo di questo tutorial è quello di spiegare le basi delle tecniche di imaging corneale più comunemente utilizzate presso l’Università dell’Iowa, inclusa una panoramica di come funzionano e come ciascuna modalità viene utilizzata nella pratica clinica.
Topografia e tomografia corneale
Principi di base
La topografia corneale viene utilizzata per caratterizzare la forma della cornea, simile a come si caratterizzerebbe una montagna usando una mappa topografica. Originariamente, la topografia corneale era usata solo per descrivere la superficie anteriore della cornea. I dispositivi ora sono in grado di caratterizzare sia le superfici corneali anteriore che posteriore, creando una mappa tridimensionale. I progressi nella fotografia digitale e nell’elaborazione del computer hanno notevolmente aumentato l’utilità della topografia corneale (1).
Il primo avanzamento nella valutazione della forma della superficie corneale anteriore fu fatto alla fine del 1800 con lo sviluppo del disco di Placido (Figura 1A) (1-2). Questa tecnica caratterizza la superficie corneale valutando il riflesso di una serie di anelli concentrici sulla superficie corneale anteriore. Mentre l’immagine del disco di Placido viene proiettata sulla cornea, parte della luce viene riflessa dall’interfaccia film lacrimale-aria come uno specchio. Il modello di riflessione della luce rivela la forma della superficie anteriore della cornea (1). Allo stesso modo, i cheratoscopi portatili (Figura 1B-C) sono strumenti pratici che visualizzano anelli concentrici sulla lampada a fessura per una rapida valutazione dei cambiamenti topografici (ad esempio, astigmatismo indotto dalle suture). La superficie corneale posteriore non può essere caratterizzata utilizzando la tecnologia del disco Placido o un cheratoscopio portatile. Molti anelli di macchine topografiche (ad es., Atlas, NIDEK OPD-Scan) ancora utilizzano dischi Placido ma prendere la tecnica un ulteriore passo avanti, fornendo una valutazione quantitativa computerizzata della superficie corneale per fornire informazioni più dettagliate di quanto si possa apprezzare semplicemente guardando il riflesso.

Figura 1. Topografia corneale qualitativa. A. Disco di Placido con cerchi bianchi concentrici. B-C. Il cheratoscopio portatile cilindrico Van Loenen, posizionato davanti all’occhio di un paziente presso la lampada a fessura, rifletterà sette anelli sulla superficie corneale per valutare rapidamente le variazioni topografiche qualitative
Una seconda tecnica per la valutazione topografica corneale è la tecnica di scansione a fessura (ad esempio, Orbscan). Questo metodo utilizza raggi di luce proiettati a scansione rapida e una telecamera per catturare i raggi riflessi per creare una mappa della superficie corneale anteriore e posteriore. Una terza tecnica, nota come Scheimpflug imaging, utilizza una telecamera rotante per fotografare sezioni trasversali corneali illuminate da fasci di fessure a diverse angolazioni (ad esempio, Pentacam). Questo metodo corregge la forma non planare della cornea e, quindi, consente una maggiore precisione e risoluzione nella creazione di una mappa 3-D della cornea (2-3).
Interpretazione del disco Placido
Le immagini del disco Placido possono essere interpretate sia qualitativamente che quantitativamente. Gli anelli concentrici proiettati sono indicati come ” mires.”La forma della superficie corneale può essere dedotta dall’ispezione di queste paludi. Simile a una mappa topografica di una montagna, le aree in cui le mire appaiono più vicine corrispondono a una curvatura corneale più ripida. Le aree in cui le paludi sono più distanziate sono più piatte. Le paludi possono anche fornire informazioni sulla qualità della superficie. Le paludi distinte e ben formate sono definite “croccanti” e suggeriscono che la superficie corneale sottostante sia regolare e liscia.
Come sfera ideale, la cornea dovrebbe avere miri equidistanti su tutta la sua superficie (Figura 2A). Variazioni minori e insignificanti sono presenti in ogni cornea, ma potrebbero non essere rilevabili sull’ispezione qualitativa di un’immagine del disco di Placido. Ad esempio, le mire distorte o ondulate suggeriscono irregolarità superficiali, come quelle causate dalla secchezza superficiale (Figura 2B). L’astigmatismo regolare provoca miri che appaiono ovoidali (Figura 2C). Se è presente astigmatismo irregolare, questo può essere visto come un riflesso irregolarmente distorto delle mire (Figura 2D). La valutazione del disco di Placido può anche essere utilizzata per guidare la rimozione della sutura dopo cheratoplastica penetrante. La rimozione selettiva delle suture può ridurre l’astigmatismo postoperatorio (Figura 2C).
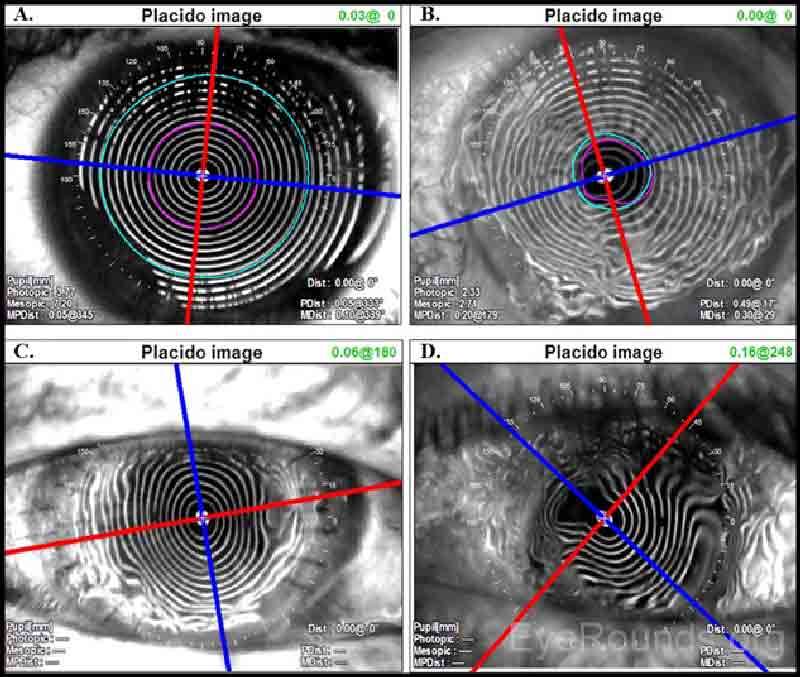
Figura 2. Proiezione di miri del disco di Placido su (A) una cornea normale con miri croccanti e astigmatismo minimo, (B) una cornea con secchezza superficiale, (C) una cornea con astigmatismo regolare contro la regola all’interno di un trapianto corneale a tutto spessore e (D) una cornea con astigmatismo irregolare all’interno di un trapianto corneale a tutto spessore. Le immagini di Placido possono aiutare a guidare la rimozione selettiva della sutura; ad esempio, le suture in (C) potrebbero essere rimosse a ore 3 e ore 9, decorso clinico permettendo, per ridurre l’astigmatismo post-operatorio.
Zeiss Atlas e NIDEK OPD-Scan Interpretation
Zeiss Atlas e NIDEK OPD-Scan sono topografi basati su dischi Placido. Come mostrato in Figura 3, il rapporto Zeiss Atlas include un’immagine del disco Placido e diverse mappe che forniscono informazioni sulla curvatura tangenziale, la curvatura assiale e l’elevazione. Una mappa tangenziale, o istantanea, è molto simile a una mappa assiale. È un modo leggermente più preciso di caratterizzare la curvatura corneale ma appare più “rumoroso” e irregolare. Le mappe assiali sono meno sensibili alla misurazione della curvatura corneale e, quindi, sono utilizzate principalmente per scopi di screening (4-5).
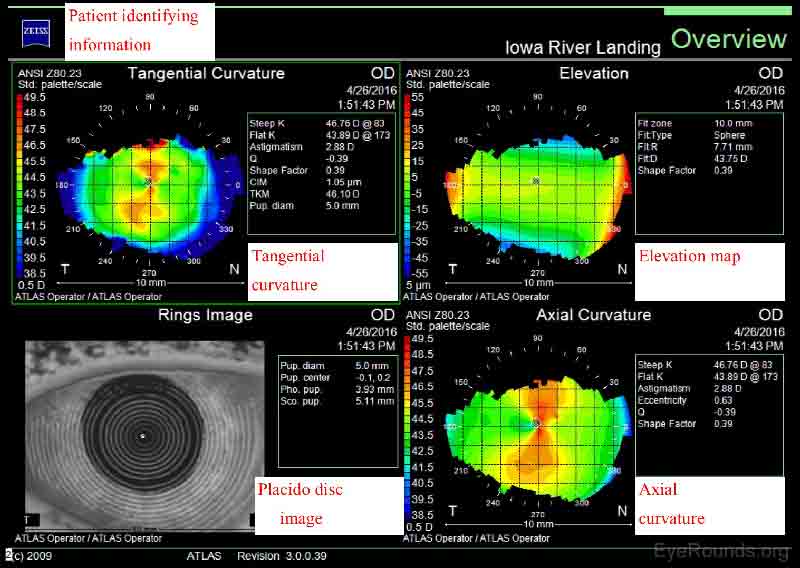
Figura 3. Rapporto Zeiss Atlas. Le mappe di curvatura tangenziale e assiale mostrano entrambi l’astigmatismo corneale con la regola con più potenza nel meridiano verticale. In particolare, il meridiano più ripido è a 083 gradi e ci sono 2,88 diottrie di astigmatismo. L’immagine del disco di Placido mostra mire concentriche regolari, che indicano una superficie corneale sana.
Simile a un rapporto Zeiss Atlas, il rapporto NIDEK imaging fornisce una mappa di curvatura assiale e un’immagine del disco Placido. Lo strumento NIDEK fornisce anche dati di cheratometria, che sono misurazioni simulate che forniscono la potenza di rifrazione diottrica nei due meridiani primari. L’errore di rifrazione del paziente viene approssimato utilizzando le misure autorefraction (REF) e wavefront (WF) e questa stima della rifrazione è disponibile nella finestra auto-rifrazione del rapporto NIDEK. Dal test NIDEK sono incluse due mappe aggiuntive che non sono disponibili con altre modalità: la Optical Path Difference (OPD) e le mappe OPD interne. L’OPD rileva specificamente l’errore di rifrazione totale (in diottrie) nell’occhio, comprese le aberrazioni nella cornea, nel cristallino e in altre strutture, mentre la mappa OPD interna cattura l’errore di rifrazione apportato dalle strutture interne dell’occhio sottraendo il potere di rifrazione corneale dall’OPD totale. Misurata anche in diottrie, questa misurazione aiuta a differenziare gli effetti dell’errore di rifrazione corneale e superficiale dalle aberrazioni interne (ad esempio, anomalie lenticolari).
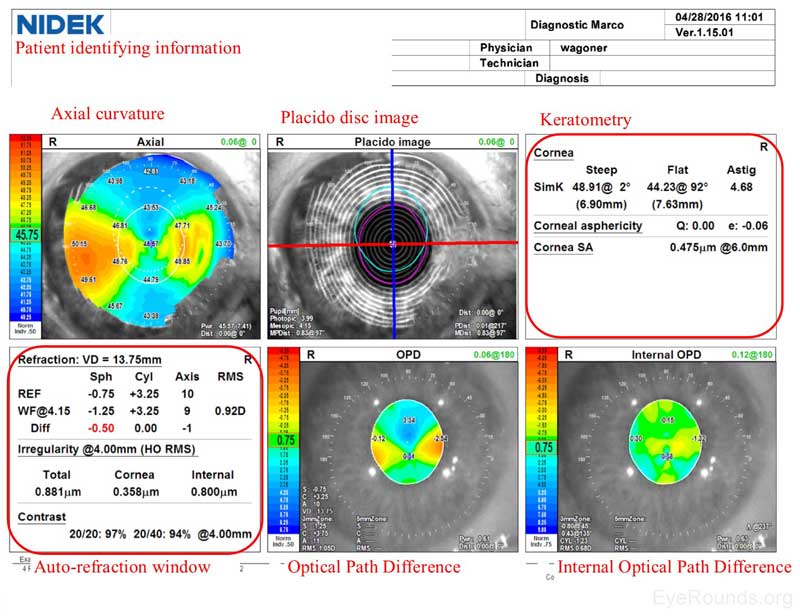
Figura 4. Rapporto NIDEK. Riquadri superiori: La mappa della curvatura assiale mostra l’astigmatismo corneale contro la regola con più potenza nel meridiano orizzontale. L’immagine del disco di Placido mostra miri concentrici con qualche irregolarità nella regione inferonasale della cornea. Il meridiano più ripido è a 002 gradi e ci sono 4,68 diottrie di astigmatismo. Riquadri inferiori: Sia le misurazioni autorefraction (REF) che wavefront (WF) stimano il paziente con miopia lieve (da -0,75 a -1,25) con correzione significativa dell’astigmatismo (+3,25) nel meridiano orizzontale (da 009 a 010 gradi). L’errore di rifrazione totale è stimato utilizzando la differenza di percorso ottico (OPD) per essere -0,75 diottrie con +3,25 di astigmatismo all’asse 010.
Interpretazione Pentacam
L’Oculus Pentacam utilizza la tecnologia Scheimpflug per creare report topografici. I rapporti contengono una grande quantità di informazioni, e esempi del rapporto panoramica e il rapporto 4 mappe sono forniti di seguito (Figura 5A-B). In particolare, il rapporto di panoramica fornisce l’immagine Scheimpflug, che è un’immagine in sezione trasversale che mostra la cornea, la camera anteriore, l’iride e la lente. Viene fornita anche una rappresentazione 3D della forma corneale del paziente. La densità della cornea viene valutata utilizzando la densitometria, che è una misurazione oggettiva della dispersione della luce nella cornea. Qualsiasi valore di densitometria inferiore a ~30 è considerato normale; così, una circostanza con conseguente chiarezza corneale diminuita (per esempio, edema corneale) aumenterà il valore di densitometria. C’è anche un comodo riassunto della cheratometria, pachimetria, e altre misurazioni numeriche in questo rapporto. Una mappa colore pachimetria indica spessore corneale.
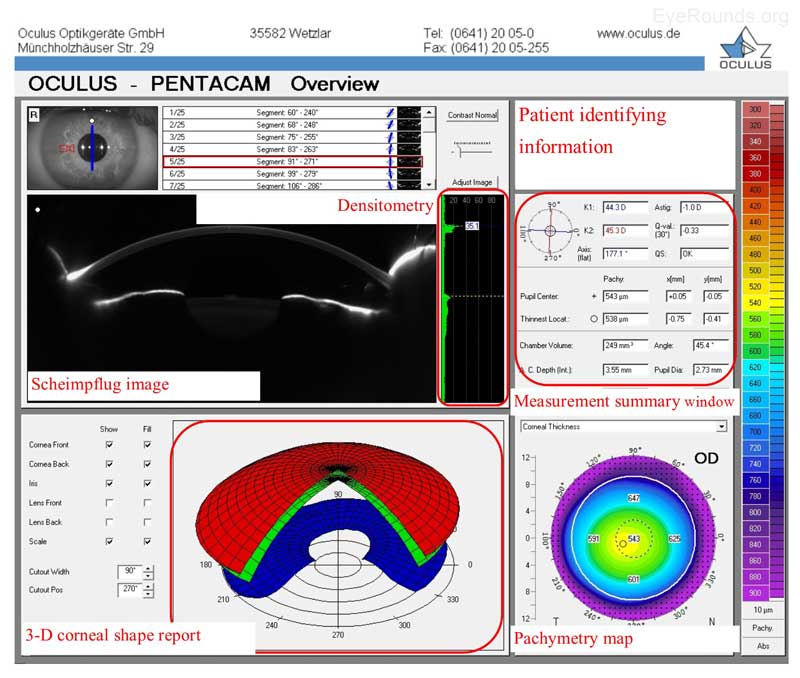
Figura 5A. Rapporto di panoramica Pentacam. Pannelli superiori: l’immagine Scheimpflug è un’immagine in sezione trasversale che mostra la cornea, la camera anteriore, l’iride e la lente. La misurazione della densitometria stima la chiarezza corneale; qualsiasi valore superiore a 30 può indicare una diminuzione della chiarezza corneale. Riquadri inferiori: viene fornita una rappresentazione 3D della forma corneale del paziente; la superficie corneale anteriore è mostrata in rosso, la superficie corneale posteriore in verde e l’iride in blu. Una mappa pachimetrica è una mappa a colori che indica lo spessore corneale; i colori più freddi sono più spessi e i colori più caldi sono più sottili (scala numerica a destra).
Il rapporto Pentacam 4 maps fornisce anche una sintesi di cheratometria, pachimetria con mappa e altre misurazioni numeriche. Simile al rapporto NIDEK, il rapporto Pentacam include una mappa assiale che descrive la curvatura della superficie corneale anteriore in valori diottrici per ciascun punto.
Le immagini float anteriori e float posteriori, che sono mappe di elevazione, vengono generate nel rapporto Pentacam. Invece di visualizzare il potere rifrattivo della cornea, le mappe di elevazione visualizzano la forma della cornea confrontandola con una sfera best-fit generata dal computer (cioè una sfera perfetta che si approssima meglio alla forma corneale in media). Il galleggiante posteriore, simile al galleggiante anteriore, mostra la forma della cornea posteriore rispetto a una sfera più adatta.

Figura 5B. Pentacam 4 Rapporto mappa. La mappa di curvatura assiale, nota anche come mappa sagittale, descrive la curvatura della superficie corneale anteriore in valori diottrici per ciascun punto. La scala dei colori rappresenta la potenza in diottrie in ogni punto particolare. I colori più caldi rappresentano una curvatura corneale più ripida mentre i colori più freddi rappresentano aree più piatte. Per le mappe di elevazione (galleggiante anteriore e posteriore), i colori più caldi indicano dove la cornea è elevata sopra la sfera più adatta e i colori più freddi indicano dove la cornea è depressa sotto la sfera più adatta. Una mappa pachimetrica è una mappa di colore che indica lo spessore corneale; i colori più freddi sono più spessi e i colori più caldi sono più sottili.
Usi clinici della topografia corneale
- Screening per ectasia corneale
Il cheratocono, l’ectasia corneale più comune, è una condizione corneale progressiva caratterizzata da assottigliamento centrale e ripido della cornea. Il cheratocono precoce sembra spesso normale all’esame della lampada a fessura e la cheratometria manuale, che valuta i 3 mm centrali, può dare una valutazione insufficiente. Per questo motivo, la topografia è diventata il gold standard per lo screening dei pazienti per il cheratocono e altre ectasie corneali (Figure 6-8).
- Monitoraggio e trattamento dell’ectasia corneale
Una volta diagnosticata un’ectasia (ad es. cheratocono, degenerazione corneale marginale pellucida), la topografia può essere utile per monitorare la progressione della malattia. Con la topografia di sorveglianza regolare, può essere determinato quando i pazienti sono a rischio di progressione e complicanze, e questo monitoraggio preciso consente un intervento precoce con trattamenti come il cross-linking del collagene o la cheratoplastica. I segni premonitori topografici includono un elevato potere corneale centrale, una grande differenza tra le due cornee di un paziente e una grande disparità tra il potere rifrattivo all’apice e alla periferia (Figure 6-8) (5).
- Chirurgia refrattiva screening e monitoraggio
Chirurgia refrattiva laser come la cheratectomia fotorefrattiva (PRK) e la cheratomileusis laser assistita in situ (LASIK) utilizzano il laser ad eccimeri per ablare il tessuto e rimodellare la cornea per correggere l’errore di rifrazione di un individuo. Non tutti i pazienti, tuttavia, possono tranquillamente sottoporsi a queste procedure. Lo screening deve essere eseguito per determinare la forma corneale e i modelli di astigmatismo sulla topografia prima che la chirurgia refrattiva possa essere eseguita in modo sicuro. La topografia può anche essere utilizzata post-operativamente per valutare l’eziologia per risultati visivi insoddisfacenti come ablazioni decentrate o incomplete.
- Selezione della lente intraoculare preoperatoria
Durante la chirurgia della cataratta, una lente intraoculare viene posizionata nell’occhio per ottenere il risultato rifrattivo desiderato. Le lenti intraoculari standard contengono solo correzione sferica. Se un paziente ha un astigmatismo corneale regolare, tuttavia, può essere utilizzata una lente torica che corregge l’astigmatismo. La topografia corneale è un test preoperatorio utile per valutare l’entità e la regolarità del cilindro corneale quando si seleziona un impianto di lenti intraoculari prima dell’intervento di cataratta.
- Valutazione e gestione dell’astigmatismo post-cheratoplastica
Dopo la cheratoplastica, l’astigmatismo corneale può essere valutato con la topografia. Questa tecnologia guida la rimozione selettiva della sutura e altri interventi per ridurre i livelli di astigmatismo.
- Valutazione del disturbo della superficie oculare
I disturbi della superficie oculare, come pterygia, cicatrici corneali e noduli di Salzmann, possono indurre astigmatismo corneale irregolare. La topografia corneale può essere utilizzata per valutare gli effetti rifrattivi di questi problemi e per aiutare nel monitoraggio della malattia e nella pianificazione chirurgica.
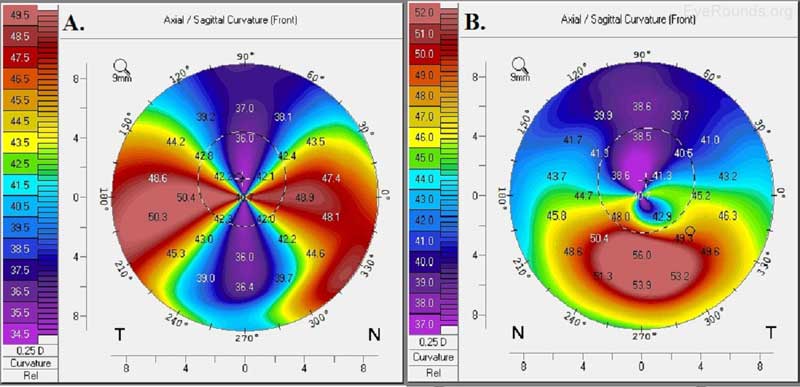
Figura 6. Degenerazione corneale marginale pellucida (A) e keratonconus (B). Le mappe assiali anteriori generate con la tecnologia Oculus Pentacam mostrano l’alto astigmatismo contro la regola in un modello di” artiglio di granchio ” di degenerazione corneale marginale pellucida e il modello di ripido inferiore del cheratoncono.
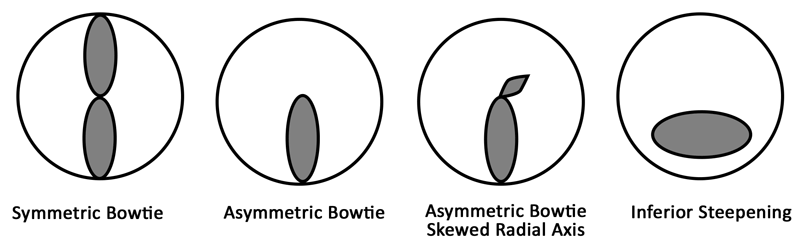
Figura 7. Progressione del cheratocono. Frequentemente la topografia mostrerà progressione del cheratocono da astigmatismo simmetrico ad astigmatismo asimmetrico, seguito da un modello di astigmatismo asimmetrico con un asse radiale inclinato. Con il cheratocono progressivo, alla fine può svilupparsi un ripido inferiore.
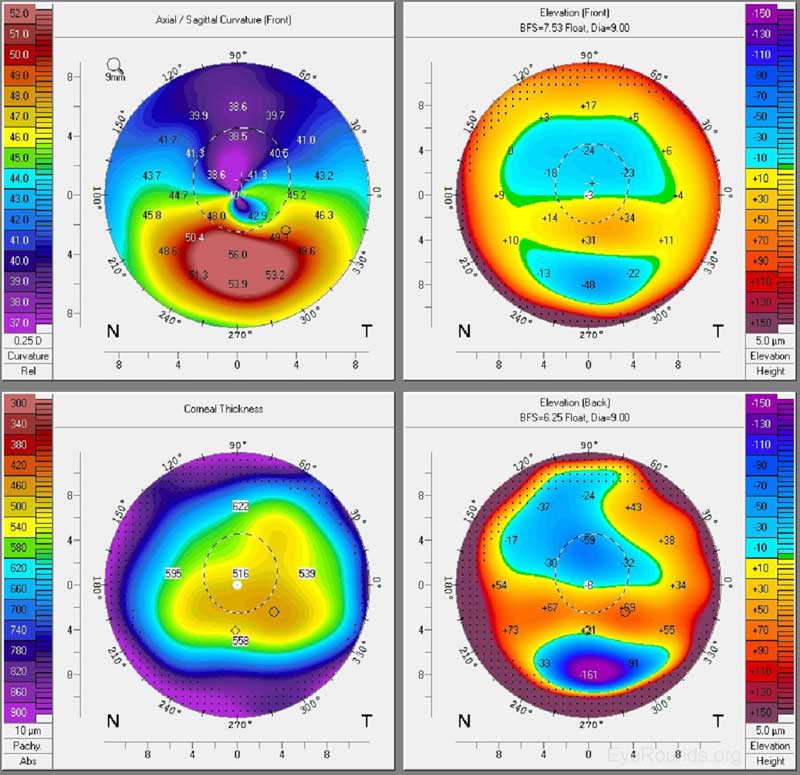
Figura 8. Cheratocono su Pentacam. La mappa assiale anteriore mostra significativo ripido paracentrale inferiore, mentre la mappa pachimetria mostra assottigliamento nella zona di ripido. I galleggianti anteriore e posteriore rivelano un rigonfiamento paracentrale, che suggerisce l’elevazione focale rispetto a una superficie sferica ideale.
Tomografia a coerenza ottica del segmento anteriore (AS-OCT)
Principi di base
La tomografia a coerenza ottica del segmento anteriore (AS-OCT) produce immagini ad alta risoluzione della cornea, dell’iride e della camera anteriore (ad esempio, Visante). È analogo agli ultrasuoni, ma utilizza onde luminose invece del suono per produrre immagini ad altissima risoluzione di strutture oculari molto piccole (Figure 9 e 10). AS-OCT utilizza due fasci di luce di scansione che vengono riflessi da una struttura oculare e quindi rilevati e confrontati con un raggio di riferimento per creare un’immagine in sezione trasversale (6).
Guida all’interpretazione
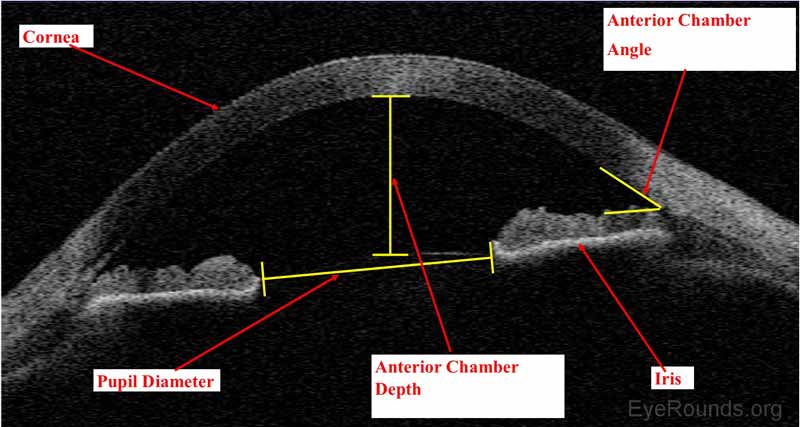
Figura 9. Visante AS-OCT mostra normale anatomia camera anteriore, tra cui la cornea, iride, angolo iridocorneale, profondità camera anteriore e diametro della pupilla.
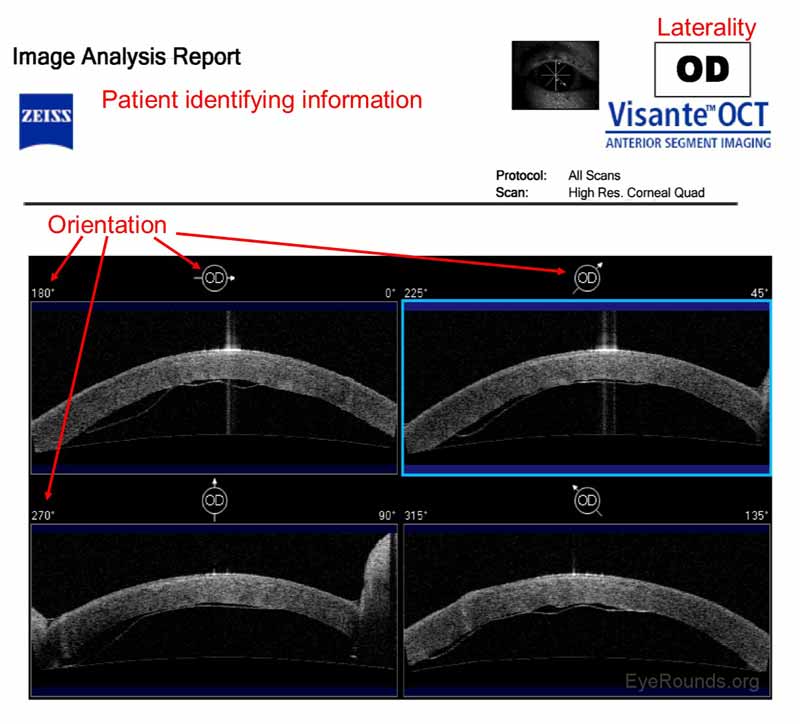
Figura 10. Rapporto Visante che mostra un innesto di cheratoplastica endoteliale a membrana Descemets poco aderente (DMEK). L’innesto ha aderito con successo dopo che un’altra bolla d’aria è stata posizionata all’interno della camera anteriore. Ogni immagine OCT è una fetta bidimensionale attraverso la camera anteriore. Le quattro frecce di orientamento, che si trovano sopra ogni immagine OCT, indicano il lato sinistro (coda della freccia) e il lato destro (punta della freccia) dell’immagine. Viene visualizzato anche l’angolo di orientamento.
Usi clinici
- Valutazione dell’angolo della camera anteriore
AS-OCT consente una valutazione qualitativa e quantitativa dell’angolo iridocorneale. Può essere utilizzato in aggiunta alla gonioscopia per la diagnosi e la gestione del glaucoma.
- Pianificazione chirurgica per miglioramenti LASIK
AS-OCT può essere utilizzato per misurare il letto stromale residuo sotto un lembo LASIK per determinare se vi è o meno sufficiente stroma rimanente per eseguire un lembo di sollevamento e valorizzazione (Figura 11).
- Pianificazione chirurgica per gli impianti di lenti intraoculari fachiche
Gli impianti di lenti intraoculari fachiche (ad es. Verisyse™) possono essere messi in serie con la lente cristallina naturale per la correzione di miopia elevata. L’AS-OCT consente misurazioni dettagliate delle dimensioni della camera anteriore per valutare se sia disponibile o meno uno spazio sufficiente della camera anteriore per uno di questi impianti di lenti (Figura 12) (7).
- Valutazione della posizione dell’innesto dopo cheratoplastica
AS-OCT è un utile complemento all’esame con lampada a fessura per la valutazione dell’aderenza dell’innesto endoteliale durante il periodo postoperatorio immediato.
- Cheratoprotesi gestione post-chirurgica
AS-OCT può fornire ulteriori informazioni riguardanti l’integrità strutturale delle cornee protesiche, come la cheratoprotesi di Boston di tipo I (Figura 14).
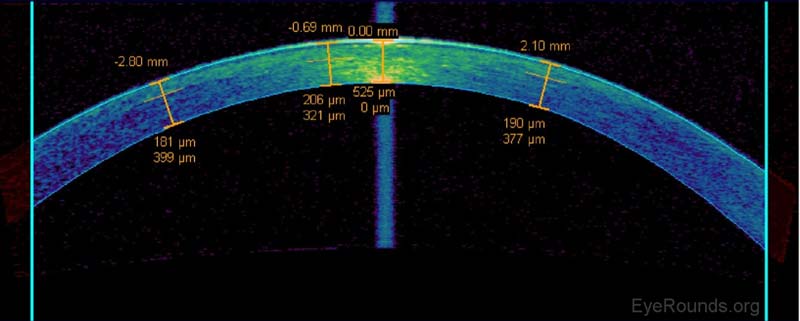
Figura 11. Misura del letto stromale residuo sotto un lembo LASIK su AS-OTT. Lo spessore corneale centrale è stimato essere 525µm ed il letto stromale residuo è misurato per essere 321µm centralmente e 377-399µm verso la cornea periferica. Presso l’Università dell’Iowa, un paziente non è considerato un candidato per LASIK o miglioramento se il letto stromale residuo calcolato finale è inferiore a 300µm.
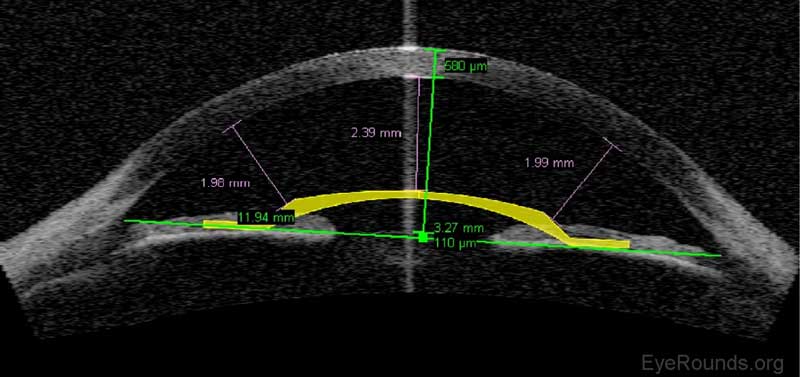
Figura 12. Lente intraoculare fachica (IOL) pianificazione chirurgica su AS-OTT. Il dispositivo Visante è in grado di sovrapporre uno IOL facico digitale nella camera anteriore per garantire che vi sia spazio adeguato per l’impianto sicuro del dispositivo.
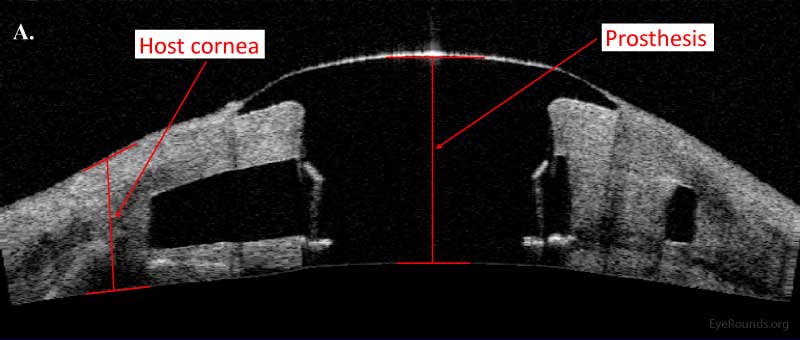
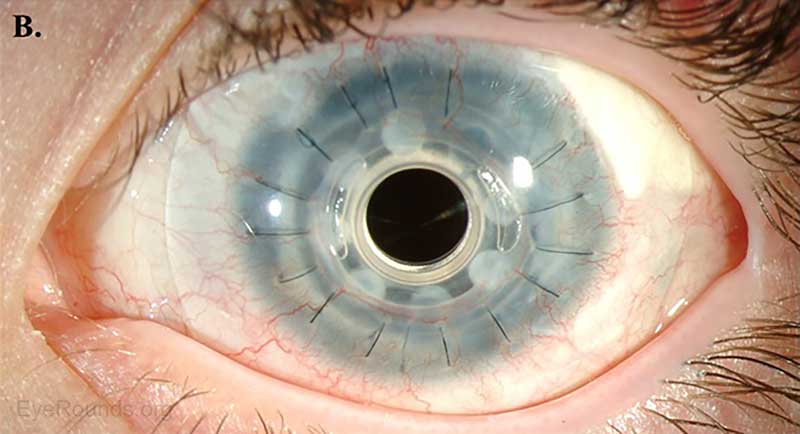
Figura 13. Tipo I Boston dispositivo di cheratoprotesi come esaminato utilizzando (A) AS-OCT e (B) una lampada a fessura (8).
Microscopia confocale
Principi di base
La microscopia confocale è una tecnica di imaging che consente l’esame in vivo delle strutture corneali ad alto ingrandimento e risoluzione. Partendo dai principi di imaging sviluppati per l’imaging neuronale, la microscopia confocale è stata utilizzata per la prima volta per studiare la cornea negli 1990 (9-10). Il dispositivo (ad es., NIDEK Confoscan, Heidelberg HRTII) consente la caratterizzazione di ciascuno dei cinque strati corneali illuminando e immaginando simultaneamente un singolo punto di tessuto (Figura 14) (11). La sorgente luminosa puntiforme e la fotocamera sono sullo stesso piano, da qui il nome ” confocale.”I moderni microscopi confocali scansionano piccole regioni di tessuto, illuminando e immaginando migliaia di punti di tessuto per creare l’immagine confocale finale (10). Scansionando diversi livelli di spessore di alcuni tessuti nel segmento anteriore, è possibile ottenere informazioni significative sulla struttura e sulla funzione a livello cellulare.
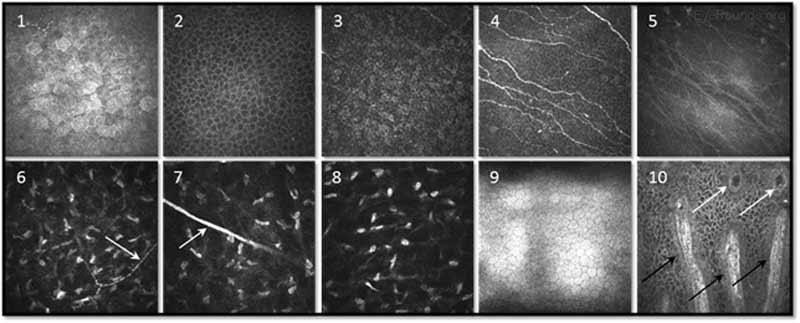
Figura 14. Microscopia confocale imaging dei vari strati corneali utilizzando la tecnologia confocale laser-scanning in vivo. 1-3. Epitelio superficiale, strato epiteliale delle cellule alari e epitelio basale; 4. Plesso nervoso subbasale; 5. Strato di Bowman; 6-8. stroma anteriore con nervo (freccia), stroma medio con tronco nervoso( freccia) e stroma posteriore; 9. Endotelio; e 10. Creste inferiori della palizzata limbale (frecce nere) con proiezioni stromali focali (frecce bianche). Immagine gentilmente concessa dal Dr. Neil Lagali (Università di Linköping, Linköping, Svezia) (11).
Guida all’interpretazione
Quando viene utilizzato per valutare la salute delle cellule endoteliali, devono essere eseguite sia l’ispezione qualitativa dell’endotelio che la valutazione quantitativa della densità delle cellule endoteliali. Le normali cellule endoteliali dovrebbero apparire piccole, esagonali e uniformi. Il pleomorfismo è la presenza di un’elevata variazione nella forma delle cellule, mentre il polimegatismo è una variazione nella dimensione delle cellule. La densità delle cellule endoteliali può essere ottenuta automaticamente o mediante conteggio manuale ed è espressa come cellule / mm2 (Figura 15).

Figura 15. Microscopia confocale che mostra un normale endotelio corneale. Notare le piccole celle esagonali con variazioni minime nella dimensione o nella forma delle celle.
Usi clinici
- Valutazione endoteliale corneale
L’esame dell’endotelio corneale a livello cellulare consente una valutazione qualitativa e quantitativa delle cellule. Le dimensioni, la forma e la densità delle cellule endoteliali possono essere tutte caratterizzate, il che fornisce informazioni importanti per diagnosticare e gestire le distrofie corneali posteriori, come la distrofia di Fuchs (Figura 16), la sindrome endoteliale iridocorneale (ICE) e la distrofia polimorfa posteriore. Il microscopio confocale può aiutare con decisioni diagnostiche, come se l’edema post-cheratoplastica sia dovuto al rigetto dell’innesto corneale (evidenziato da cellule infiammatorie visualizzate) o allo scompenso endoteliale (evidenziato da una bassa densità delle cellule endoteliali) (Figura 17) (7, 10).
- Identificazione della cheratite infettiva
La cheratite infettiva è una condizione pericolosa per la vista in cui è indispensabile una diagnosi tempestiva per preservare la vista e l’occhio. La microscopia confocale è un’aggiunta utile per aiutare rapidamente ad identificare l’agente causale in vivo, quali i funghi o l’Acanthamoeba, in modo dal trattamento appropriato può essere iniziata. Le acanthamoeba appaiono nella loro forma cistica come strutture ovoidali altamente riflettenti (Figure 18 e 19). I funghi possono apparire come filamenti brillantemente riflettenti e possono avere evidenza di septazioni (Figura 20) (9).
- Valutazione della morfologia del nervo corneale
La microscopia confocale può aiutare a quantificare la patologia del plesso nervoso subbasale in pazienti con cheratopatia neurotrofica e neuropatia diabetica che coinvolge la cornea.
- Misurazione della profondità corneale
Simile a OCT, la microscopia confocale può misurare la profondità delle strutture, come depositi, cicatrici o lembi LASIK all’interno della cornea per facilitare la pianificazione chirurgica.
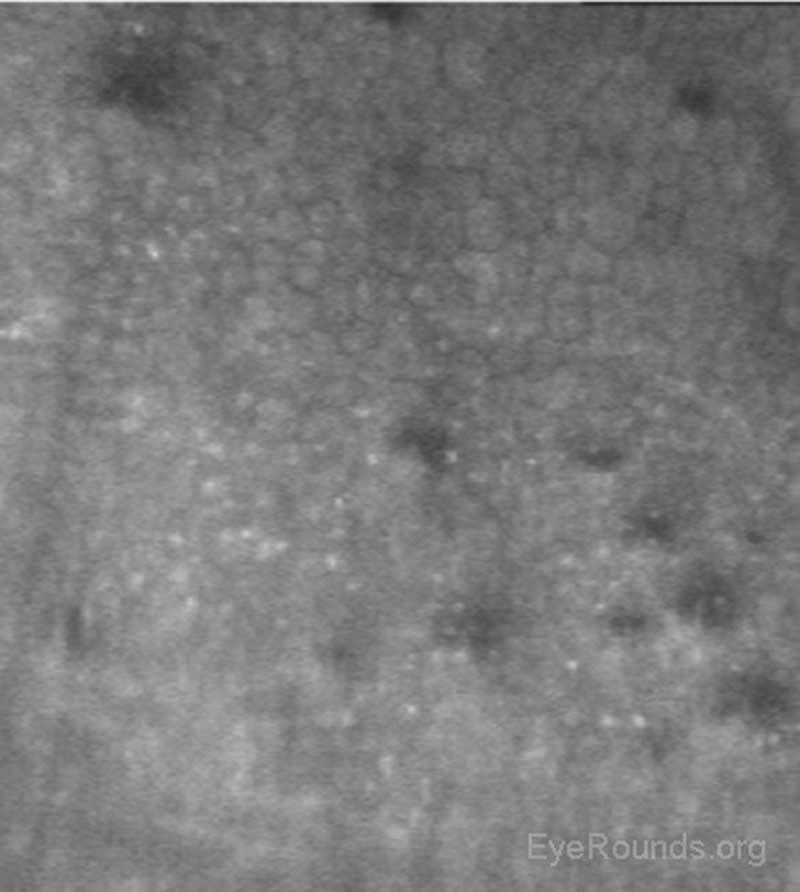
Figura 16. Distrofia endoteliale di Fuchs che mostra caratteristiche guttae (aree scure) e ridotta densità delle cellule endoteliali su microscopia confocale.
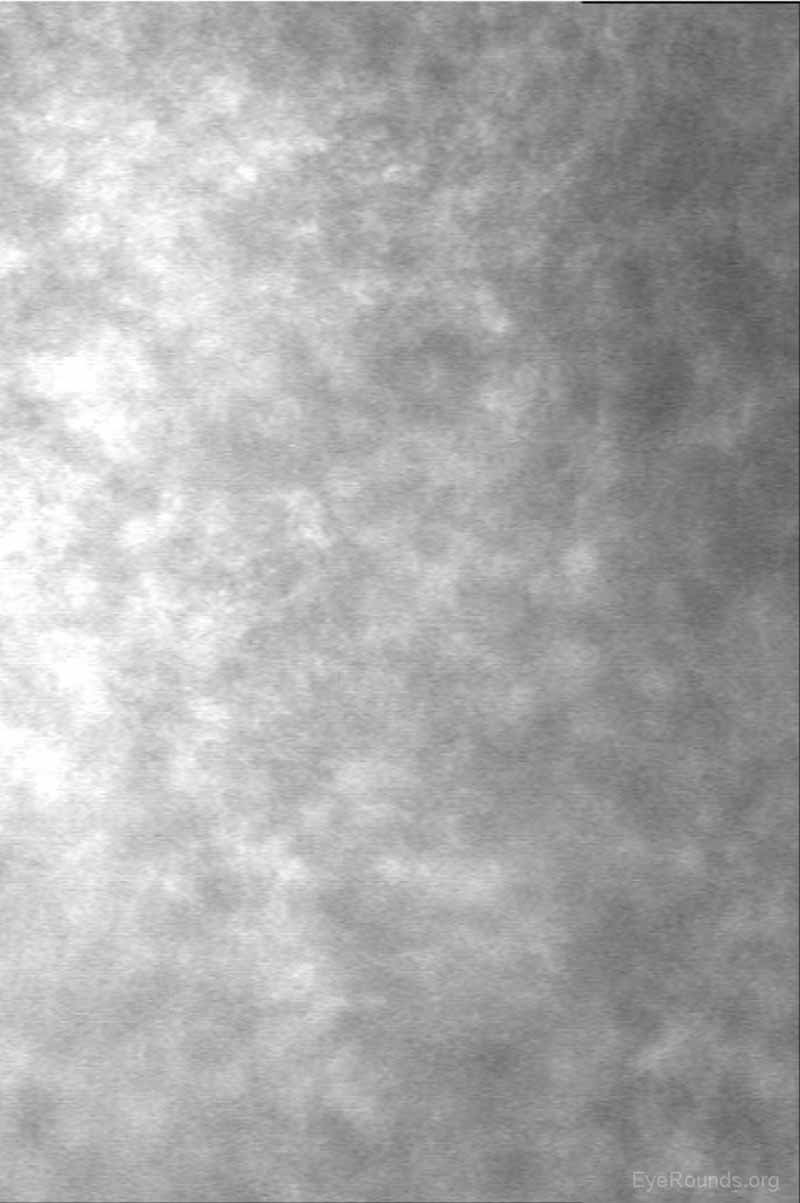
Figura 17. Scompenso endoteliale all’interno di un innesto di cheratoplastica penetrante. Non ci sono cellule endoteliali identificabili su microscopia confocale.

Figura 18. Cheratite da acanthamoeba vista su microscopia confocale. Le cisti appaiono come oggetti rotondi ad alto contrasto mentre i trofozoiti appaiono come forme irregolari.
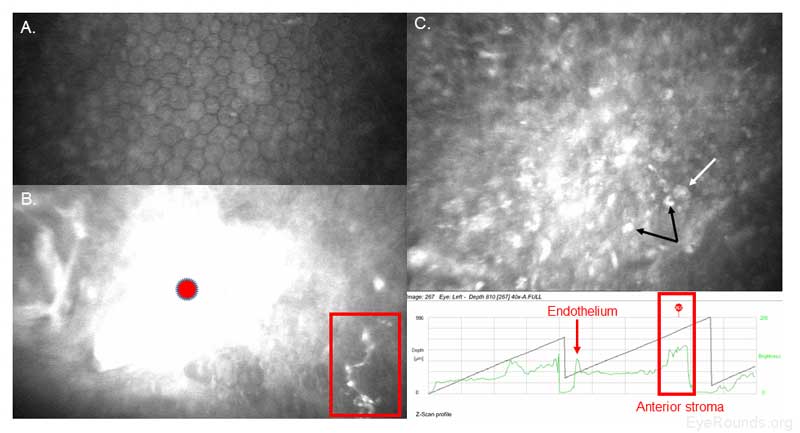
Figura 19. Microscopia confocale rilevamento di Acanthamoeba e cheratite fungina in un utente di lenti a contatto. A. Il polimegatismo endoteliale, che è un segno di stress corneale, è probabilmente il risultato dell’uso a lungo termine delle lenti a contatto del paziente. Nello strato endoteliale non sono presenti cisti o trofozoiti. B. Il reclutamento di globuli bianchi (cerchio rosso) è evidente nello stroma anteriore direttamente adiacente alle cisti di Acanthamoeba (freccia bianca) e agli elementi fungini (scatola rossa). I trofozoiti di Acanthamoeba si nutrono diph se entrambe le infezioni non vengono prontamente trattate. C. Acanthamoeba cisti a doppia parete (freccia bianca) e trofozoiti (frecce nere) sono presenti in tutto lo stroma anteriore. Il profilo Z-scan descrive il backscatter (cioè la luminosità delle singole scansioni confocali), che consente una rapida valutazione della posizione corneale (scatola rossa) e della densità cellulare nella regione specifica.
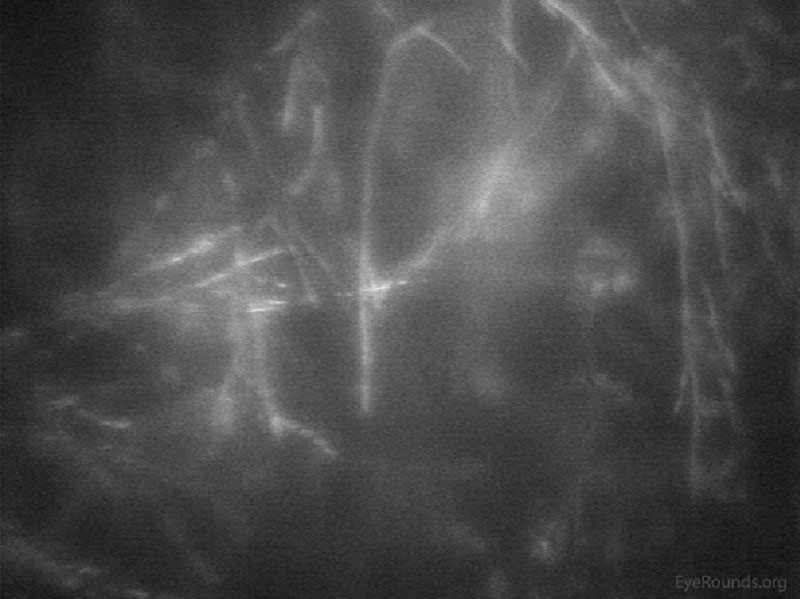
Figura 20. Cheratite fungina vista su microscopia confocale. Leph ramificate aiutano a confermare la diagnosi di cheratite Fusarium.
Sommario
L’oftalmologia è un campo in rapida evoluzione con nuove tecnologie per la diagnosi e il trattamento in fase di sviluppo e implementazione ogni anno. Con lo sviluppo di tecniche più avanzate (ad esempio LASIK, cheratoplastica endoteliale), l’utilità della tecnica avanzata di imaging corneale continua a crescere. Questo tutorial ha lo scopo di fornire una panoramica degli argomenti di imaging corneale e di dare ai tirocinanti una base su cui costruire mentre padroneggiano l’uso di questi strumenti fondamentali della moderna oftalmologia clinica.
- Brody J, Waller S, Wagoner M. Topografia corneale: storia, tecnica e usi clinici. Cliniche Oftalmologiche internazionali. 1994;34(3):197-207.
- Prakash G. Topografia corneale. 2015. ; Disponibile da http://eyewiki.org/Corneal_topography
- Hashemi H, Mehravaran S. Parametri di elevazione, spessore e curvatura corneali clinicamente rilevanti giorno per giorno utilizzando il topografo a fessura a scansione Orbscan II e il dispositivo di imaging Pentacam Scheimpflug. Medio Oriente Afr J Ophthalmol. 2010;17(1):44-55.
- Friedman N. Perle per l’interpretazione delle mappe topografiche corneali. 2013. ; Disponibile da http://www.ophthalmologyweb.com/Featured-Articles/142292-Pearls-for-Interpreting-Corneal-Topography-Maps/
- Lopes, B, Ramos, Io, Dawson, D, et. al. Rilevazione di malattie corneali ectatiche basate su Pentacam. Z. Med. Phys. 2016; 26(2): 136–142.
- Radhakrishnana S. Tomografia a coerenza ottica del segmento anteriore. 2014. ; Disponibile dahttp://eyewiki.aao.org/Anterior_Segment_Optical_Coherence_Tomography
- Kent C. Sfruttando al meglio il segmento anteriore OTT. 2011. ; Disponibile da http://www.reviewofophthalmology.com/content/i/1471/c/27717/
- http://webeye.ophth.uiowa.edu/eyeforum/cases-i/case211/L/5a-kpro.jpg
- Tavakoli M, Hossain P, Malik RA. Applicazioni cliniche della microscopia corneale confocale. Clin Oftalmolo. 2008;2(2):435-45.
- Erie JC, Mclaren JW, Patel SV. Microscopia confocale in oftalmologia. Am J Ophthalmol. 2009;148(5):639-46.
- Lagali N, Bourghardt Peebo B, Germundsson J, et. al. (2013). Microscopia confocale a scansione laser in vivo della cornea: Metodi di imaging e analisi per applicazioni precliniche e cliniche, Microscopia Laser confocale. Principi e applicazioni in Medicina, Biologia e Scienze dell’alimentazione, Neil Lagali (Ed.), InTech, Disponibile da: http://www.intechopen.com/books/confocal-laser-microscopy-principles-and-applications-in-medicine-biology-and-the-food-sciences/laser-scanning-in-vivo-confocal-microscopy-of-the-cornea-imaging-and-analysis-methods-for-preclinica