INTRODUZIONE
Drug eluting stent (DES) sono associati con tassi significativamente più bassi di rivascolarizzazione della lesione target rispetto bare-metal stent (BMS). Tuttavia, la terapia antipiastrinica doppia a lungo termine (DAPT) è invariabilmente necessaria per evitare la trombosi tardiva dello stent correlata alla guarigione ritardata, impedendo l’uso frequente di DES in pazienti ad alto rischio di sanguinamento. Per molti anni, le linee guida hanno raccomandato un periodo di almeno 12 mesi di DAPT in base alle prestazioni del DES di prima generazione.1 Recentemente, le linee guida europee hanno raccomandato 6 mesi di DAPT per pazienti stabili (livello di evidenza B).2 Studi e registri DES di nuova generazione hanno dimostrato tassi di trombosi più bassi rispetto a DES di prima generazione o anche BMS.3-7 Un’analisi retrospettiva di studi DES di nuova generazione ha riferito che l’interruzione precoce o l’interruzione del DAPT oltre 1-3 mesi dopo l’impianto sembrava non aumentare il rischio di rischio.8,9
Diversi studi hanno confrontato durate DAPT distinte (3-6 mesi vs 12-24 mesi).10-16 Analisi individuali e un pool di 4 di questi studi hanno dimostrato che i regimi di DAPT a breve termine mostrano tassi simili di eventi ischemici, riducendo contemporaneamente l ‘ incidenza di eventi emorragici.10-17
Tuttavia, alcuni avvertimenti limitano l’applicabilità diffusa di questi studi, tra cui la progettazione retrospettiva delle analisi e dei relativi pregiudizi, alcuni con campioni di piccole dimensioni, una limitata aderenza ai protocolli e l’uso frequente di DES obsoleti. Ad esempio, la versione dello stent a eluizione zotarolimus utilizzata in questi studi è nota per mostrare un grado relativamente elevato di perdita di lumen tardiva, guadagnandosi la reputazione di essere uno stent il cui comportamento è da qualche parte tra un BMS e il DES di nuova generazione. Queste prove includevano anche BMS e DES di prima generazione.
Presentiamo un registro prospettico multicentrico volto a valutare la sicurezza di un approccio DAPT di 6 mesi in pazienti che ricevono un DES non di prima generazione rispetto ai risultati di una serie abbinata di pazienti che ricevono 12 mesi di DAPT.
METODI
Il multicentrico, prospettico registro ESTROFA-DAPT coinvolge 18 centri in tutta la Spagna. Questa analisi fa parte del progetto ESTROFA e della rete di studio ed è stata supportata dal Gruppo di lavoro spagnolo di cardiologia interventistica della Società spagnola di Cardiologia. In ogni centro ai pazienti è stato prescritto DAPT con acido acetilsalicilico e clopidogrel per 6 mesi dopo l’impianto del DES secondo i seguenti criteri:
- •
Un’indicazione clinica per un intervento percutaneo con DES non di prima generazione in uno dei seguenti contesti clinici: a) ischemia silente; b) l’angina stabile; c) angina instabile senza il grado di elevazione della troponina; d) i pazienti con non–elevazione del tratto ST o ST-segment elevation infarto miocardico senza stimato a basso rischio di sanguinamento e di lungo termine, DAPT, ma ancora considerato candidati per il trattamento con DES (cioè, i pazienti > 75 anni, quelli con una storia di ulcera peptica senza sanguinamento, moderata-grave insufficienza renale cronica o malattia epatica moderata, e quelli con la chirurgia elettiva noncardiac > 6 mesi).
- •
Per quanto riguarda la procedura, sono state escluse le lesioni coronariche principali a sinistra e le biforcazioni trattate con 2 stent o pazienti che richiedono più di 3 stent. Sono stati esclusi anche i pazienti con una precedente storia di trombosi tardiva del DES.
La decisione di selezionare questi criteri di inclusione si è basata sui seguenti problemi di sicurezza: a) L’uso di DAPT per 12 mesi dopo una sindrome coronarica acuta (ACS) è supportato da prove ed è raccomandato in varie linee guida cliniche e documenti di consenso.1,2,18-21 Potrebbero essere inclusi solo i pazienti con ACS a basso rischio e un certo rischio di sanguinamento. b) Lo studio aveva un protocollo basato sulla sicurezza; pertanto, l’inclusione di pazienti con un rischio più elevato di trombosi dello stent (> 3 stent, biforcazioni con tecniche a 2 stent e precedente trombosi tardiva con DES) e quelli con un alto rischio di morte sotto un evento trombotico (stent nell’arteria principale sinistra) sono stati esclusi.
Infatti, questi sottogruppi (ACS, lesioni multiple e lesioni complesse) hanno mostrato una tendenza a trarre maggiori benefici dopo un periodo di DAPT più lungo rispetto ai sottogruppi con angina stabile o lesioni singole nello studio PRODIGY.10
Tutti i dati clinici, angiografici e di procedura al basale sono stati riportati all’interno di un database comune specificamente progettato per questo studio. Sono state presentate anche informazioni sul follow-up clinico e questi dati sono stati regolarmente aggiornati durante le revisioni del registro e del database ospedaliero, nonché attraverso il contatto del paziente. La verifica del DAPT per il periodo di DAPT ≤ 6 mesi è stata richiesta e confermata attraverso il contatto con il paziente. L’aggiudicazione dell’evento finale è stata effettuata presso il centro di coordinamento (Hospital Universitario Marqués de Valdecilla) da 2 ricercatori ciechi (Drs. De la Torre e García Camarero).
Per confrontare questa coorte con la coorte DAPT a 12 mesi, abbiamo esaminato il database dello studio ESTROFA-2, già pubblicato nel 2010.22 Si trattava di un registro prospettico multicentrico progettato per valutare l’incidenza di trombosi dopo l’impianto di DES di seconda generazione, che comprendeva 4768 pazienti; tra questi, 4354 sono stati trattati con 12 mesi di DAPT. Utilizzando entrambi i database del registro (ESTROFA-DAPT ed ESTROFA-2), è stata effettuata un’analisi del punteggio di propensione per ottenere 2 coorti comparabili di pazienti trattati con un DAPT di 6 mesi o 12 mesi.
Questi 2 registri, sebbene condotti in periodi di tempo diversi, sono stati costruiti utilizzando una metodologia simile. Il team di direzione e coordinamento era lo stesso e i moduli di registrazione clinica basati sul web condividevano lo stesso formato; la maggior parte dei centri attivi in ESTROFA-DAPT reclutava anche pazienti in ESTROFA-2 (13 dei centri 18). Infine, i principali ricercatori coinvolti nell’analisi delle due banche dati del registro erano gli stessi. L’aggiudicazione dell’evento è stata condotta con definizioni di evento prestabilite e sono state richieste ulteriori informazioni necessarie per ottenere una corretta aggiudicazione finale.
Endpoint e definizioni
L’endpoint primario dello studio era la sopravvivenza libera da eventi a 12 mesi (morte cardiaca, infarto miocardico, rivascolarizzazione e sanguinamento maggiore) in entrambi i gruppi di trattamento con DAPT. Gli endpoint secondari includevano morte per tutte le cause, morte cardiaca, infarto miocardico non fatale, rivascolarizzazione coronarica, trombosi definita dello stent, trombosi definita o probabile dello stent, trombosi definita o probabile dello stent nel periodo da 6 a 12 mesi dopo l’intervento coronarico percutaneo dell’indice e eventi di sanguinamento maggiore.
Le definizioni specifiche dei principali eventi avversi cardiovascolari erano le seguenti. Infarto del miocardio è stato definito come un tipico aumento e diminuzione graduale (troponina), o come un più rapido aumento e la caduta (creatina-chinasi MB) di marcatori biochimici coerente con necrosi miocardica in associazione con almeno 1 dei seguenti: ischemico sintomi, lo sviluppo di onde Q patologiche l’elettrocardiogramma, variazioni dell’elettrocardiogramma che indica ischemia (ST-segment elevation o depressione), o patologico risultati coerenti con infarto miocardico acuto. La rivascolarizzazione è stata definita come qualsiasi tipo di rivascolarizzazione coronarica percutanea o chirurgica clinicamente indicata. La trombosi dello stent definita o probabile è stata considerata secondo le definizioni del Consorzio di ricerca accademica.23 Eventi di sanguinamento sono stati classificati in base ai criteri del bleeding academic research consortium (BARC).24
Analisi statistica
Sulla base di dati precedenti di ESTROFA-2 nel sottogruppo di questo registro con un profilo simile a quello incluso in ESTROFA-DAPT, è stato ipotizzato un tasso di endpoint primario del 6,5% al 7,0% per entrambi i gruppi. Pertanto, con una potenza dell ‘ 80% e un errore di tipo I a 1 lato del 5%, una dimensione del campione di 1200 pazienti in ciascun gruppo dimostrerebbe la non inferiorità tra i 2 gruppi per l’endpoint primario con un margine fisso di noninferiorità del 2,5%, che è in accordo con i margini di noninferiorità utilizzati negli studi contemporanei di DES e in uno studio che confronta diversi periodi DAPT.13 Se il limite superiore dell ‘ intervallo di confidenza del 95% della differenza di trattamento (DAPT a breve vs DAPT a lungo termine) era inferiore a 2.5%, l’ipotesi nulla sarebbe respinta, il che significherebbe che il gruppo a breve termine non era inferiore al gruppo a lungo termine per quanto riguarda l’endpoint primario a 12 mesi.
Le variabili continue sono presentate come media ± deviazione standard. Le variabili categoriali sono espresse come percentuali. Le variabili continue sono state confrontate con il test Student t se hanno seguito una distribuzione normale e con i test Wilcoxon quando non lo hanno fatto (valutazione del tipo di distribuzione mediante il test Kolmogorov-Smirnov). Le variabili categoriali sono state confrontate con il test chi-quadrato o il test esatto di Fischer, come richiesto. Le curve di Kaplan-Meier per la sopravvivenza libera da eventi sono state ottenute per ciascun gruppo o sottogruppo considerato nell’analisi e sono state confrontate attraverso il log rank test. Sono stati condotti test di interazione per identificare sottogruppi che presentano diversi rischi di trombosi dello stent sotto i 2 diversi periodi di DAPT.
Sono state compiute due azioni per selezionare serie comparabili di pazienti da questi 2 registri. In primo luogo, abbiamo applicato i criteri di esclusione da ESTROFA-DAPT al database ESTROFA-2, quindi i pazienti con lesioni coronariche principali a sinistra trattate, biforcazioni trattate con 2 stent, pazienti con più di 3 stent impiantati e quelli con una precedente storia di trombosi tardiva del DES sono stati esclusi dall’analisi. In secondo luogo, abbiamo condotto un processo di corrispondenza del punteggio di propensione. Tutte le variabili elencate nelle Tabelle 1 e 2 sono state inserite come covariate per ricavare i punteggi di propensione. Il dialogo personalizzato “psmatching” è stato utilizzato in combinazione con SPSS versione 19. Il programma “psmatching” esegue tutte le analisi in R attraverso il plug-in SPSS R (versione 2.10.1). Questa procedura ha coinvolto 3 fasi: a) I punteggi di propensione sono stati stimati utilizzando la regressione logistica in cui la prescrizione di un regime di DAPT di 6 mesi è stata utilizzata come variabile di risultato e tutte le covariate come predittori. b) I pazienti sono stati abbinati utilizzando la semplice corrispondenza del vicino più vicino 1:1, che si basa su un algoritmo di corrispondenza “avido” che ha ordinato le osservazioni nel gruppo DAPT a 6 mesi in base al loro punteggio di propensione stimato. Questo algoritmo ha quindi abbinato ciascuna unità in sequenza a un’unità nel gruppo DAPT di 12 mesi con il punteggio di propensione più vicino. Per escludere partite negative, abbiamo imposto un calibro di 0.2 della deviazione standard del logit del punteggio di propensione. Abbiamo ignorato le unità al di fuori dell’area di supporto comune (definita come la regione delle distribuzioni dei punteggi di propensione stimati nei gruppi DAPT a 6 mesi e 12 mesi per i quali sono state osservate unità in entrambi i gruppi). Questo è stato fatto per migliorare l’equilibrio delle covariate. c) Una serie di controlli di adeguatezza del modello è stata eseguita per verificare se un adeguato equilibrio delle covariate è stato raggiunto attraverso la procedura di corrispondenza. Ciò è stato fatto calcolando la misura di squilibrio globale e attraverso la produzione di 5 grafici diagnostici: gli istogrammi dei punteggi di propensione in entrambi i gruppi prima e dopo di corrispondenza, un dot-plot dei singoli punteggi di propensione di unità di controllo e il gruppo di trattamento, abbinato o senza eguali, gli istogrammi di standard differenze di tutti i termini (covariate, quadratica termine, interazioni) prima e dopo di corrispondenza, un dot-plot che visualizzata la grandezza del standardizzate differenze prima e dopo di corrispondenza per ogni covariata, un appezzamento di media standardizzata le differenze prima e dopo di corrispondenza. Viene fornito un test chi-quadrato di squilibrio complessivo. Questa statistica di prova, che è correlata alla nota statistica T2 di Hotelling, valuta simultaneamente se qualsiasi variabile o qualsiasi combinazione lineare di variabili è significativamente sbilanciata dopo la corrispondenza. Il test ha esaminato tutte le covariate utilizzate per stimare il punteggio di propensione. Le differenze standardizzate sono state calcolate per tutte le covariate prima e dopo la corrispondenza per valutare l’equilibrio dopo la corrispondenza. Una differenza standardizzata
Caratteristiche Cliniche in Gruppi Abbinati
| 6-mese DAPT (n = 1286) | 12-mese DAPT (n = 1286) | P | ASD (%) | |
|---|---|---|---|---|
| l’Età, gli anni | 67.3 ± 11 | 67.1 ± 11 | .6 | 4.4 |
| Femmine | 304 (23.5) | 300 (23.3) | .9 | 1.1 |
| Fumatore | 270 (21.0) | 286 (22.2) | .5 | 4.3 |
| Ipertensione | 849 (66) | 836 (65) | .6 | 3.5 |
| Dislipidemia | 769 (59.8) | 751 (58.4) | .5 | 3.3 |
| Diabete mellito | 526 (40.9) | 502 (39.0) | .3 | 5.7 |
| Funzionalità renale compromessa* | 103 (8.0) | 99 (7.7) | .8 | 1.8 |
| MI precedente | 279 (21.7) | 270 (20.9) | .7 | 2.6 |
| PCI precedente | 370 (28.8) | 355 (27.6) | .4 | 5.6 |
| CABG precedente | 63 (4.9) | 71 (5.5) | .5 | 4.9 |
| FL, % | 56 ± 12.5 | 56.2 ± 12.5 | .8 | 2.1 |
| Angina stabile | 591 (45.9) | 581 (45.1) | .7 | 2.5 |
| Angina instabile | 342 (26.6) | 351 (27.3) | .4 | 5.6 |
| MI di elevazione del segmento non ST | 140 (10.8) | 150 (11.6) | .3 | 6.7 |
| Elevazione del segmento ST MI | 54 (4.2) | 59 (4.6) | .5 | 4.2 |
| Ischemia silenziosa | 159 (12.3) | 145 (11.3) | .3 | 6.6 |
ASD, differenza standardizzata assoluta; CABG, bypass coronarico; DAPT, doppia terapia antiaggregante piastrinica; LVEF, frazione di eiezione ventricolare sinistra; IM, infarto miocardico; PCI, intervento coronarico percutaneo.
Salvo diversa indicazione, i dati sono espressi come n. ( % ) o media ± deviazione standard.
La compromissione della funzionalità renale è stata definita come creatinina sierica > 1,5 mg / dL.
le Caratteristiche Procedurali e tecniche in Gruppi Abbinati
| 6-mese DAPT (n = 1286) | 12-mese DAPT (n = 1286) | P | ASD (%) | |
|---|---|---|---|---|
| No. di stent impiantati | 1.17 ± 0.40 | 1.19 ± 0.40 | .2 | 7.2 |
| Lunghezza dello stent, millimetro | 21.0 ± 8.0 | 21.2 ± 8.4 | .5 | 4.5 |
| Diametro dello stent, millimetro | 2.90 ± 0.40 | 2.91 ± 0.40 | .5 | 3.4 |
| In-stent restenosis | 96 (7.4) | 82 (6.3) | .3 | 6.7 |
| Bifurcation | 198 (15.4) | 217 (16.8) | .3 | 7.1 |
| Chronic total occlusions | 90 (7.0) | 72 (5.6) | .2 | 7.7 |
| LAD involvement | 602 (46.8) | 605 (47.0) | .9 | 0.9 |
| IVUS guidance | 71 (5.5) | 78 (6.0) | .6 | 3.5 |
| EES | 688 (53.5) | 646 (50.2) | .1 | 7.8 |
| Acetylsalicylic acid + clopidogrel | 1286 (100) | 1286 (100) | 1 | 0 |
ASD, absolute standardized difference; DAPT, dual antiplatelet therapy; EES, everolimus-eluting stent; IVUS, intravascular ultrasound; LAD, left anterior descending artery.
Salvo diversa indicazione, i DAT sono espressi come n. ( % ), o media ± deviazione standard.
Un valore P
RISULTATI
Come mostrato nel diagramma di flusso dello studio (Figura 1), dalle coorti ESTROFA-2 ed ESTROFA-DAPT originali e dopo aver eseguito la corrispondenza del punteggio di propensione, abbiamo ottenuto 2 gruppi di 1268 pazienti ciascuno: i gruppi DAPT a 6 mesi e DAPT a 12 mesi. Le caratteristiche cliniche e procedurali dei 2 gruppi sono presentate nelle tabelle 1 e 2. Vengono fornite le differenze standardizzate postmatching stimate per tutte le covariate. Tutti erano
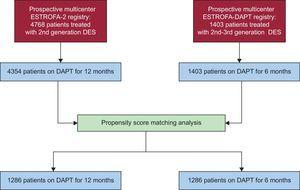
Diagramma di flusso di studio. DAPT, doppia terapia antiaggregante piastrinica; DES, stent medicamentosi.
Per quanto riguarda la distribuzione del DES, il DES più frequentemente usato in entrambi i gruppi è stato lo stent a eluizione di everolimus (53,5% nel gruppo DAPT a 6 mesi vs 50,2% nel gruppo DAPT a 12 mesi; P = .1). Lo stent a eluizione zotarolimus è stato utilizzato in 28.8% del gruppo DAPT a 6 mesi contro il 49,8% del gruppo a 12 mesi; in coincidenza con i marchi Resolute® e Endeavor®, rispettivamente. Lo stent a eluizione biolimus è stato utilizzato nel 12,7% del gruppo DAPT a 6 mesi.
Nessun paziente è stato perso al follow-up e i tassi di aderenza al trattamento sono stati del 97% e del 95% nei gruppi DAPT a 6 mesi e 12 mesi, rispettivamente. Ciò significa che solo il 3% nel gruppo DAPT a 6 mesi ha esteso la doppia terapia oltre i 6 mesi e solo il 5% nel gruppo DAPT a 12 mesi ha prolungato la doppia terapia oltre il primo anno.
Gli eventi clinici al follow-up di 12 mesi sono riportati nella Tabella 3. Non sono state osservate differenze significative tra i gruppi per l’endpoint primario (hazard ratio = 0,75; intervallo di confidenza al 95%, 0,54-1,05 per DAPT a 6 mesi vs 12 mesi) o per uno qualsiasi degli endpoint considerati, con un P = .001 per non inferiorità. Non solo c’era un’incidenza simile di eventi ischemici nei gruppi DAPT a 6 mesi e 12 mesi, ma anche l’incidenza di trombosi definita e definita o probabile era numericamente inferiore nel gruppo a 6 mesi (Figure 2 e 3). Gli eventi emorragici maggiori erano numericamente più frequenti nel gruppo trattato con DAPT a 12 mesi, ma non differivano significativamente rispetto al gruppo trattato con DAPT a 6 mesi. L ‘ incidenza degli eventi clinici nel periodo da 6 a 12 mesi è riportata nella Tabella 4, mentre i pazienti erano off-DAPT/on-DAPT nei gruppi a 6 mesi e 12 mesi di DAPT, rispettivamente. Non sono state osservate differenze tra i gruppi in questo periodo.
i Risultati a 12 Mesi di Follow-up
| 6-mese DAPT (n = 1286) | 12-mese DAPT (n = 1286) | P | |
|---|---|---|---|
| endpoint Primario | |||
| morte Cardiaca, infarto miocardico, rivascolarizzazione o BARC ≥ 3 sanguinamento | 65 (5.0) | 85 (6.6) | .09 |
| Endpoint secondari | |||
| Morte per tutte le cause | 21 (1.6) | 24 (1.9) | .4 |
| Morte cardiaca | 11 (0.9) | 13 (1.0) | .9 |
| Infarto miocardico | 10 (0.85) | 13 (1.00) | .8 |
| Rivascolarizzazione | 41 (3.2) | 55 (4.3) | .1 |
| Trombosi definita | 3 (0.24) | 5 (0.40) | .5 |
| Trombosi definita e probabile | 6 (0.5) | 9 (0.7) | .4 |
| BARC ≥ 3 eventi emorragici | 10 (0.8) | 18 (1.4) | .2 |
BARC, Bleeding Academic Research Consortium; DAPT, doppia terapia antiaggregante piastrinica.
I dati sono espressi come n. (%).
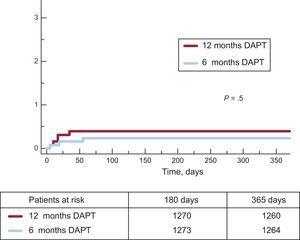
Incidenza cumulativa di trombosi definita dello stent in entrambi i gruppi. DAPT: doppia terapia antipiastrinica.
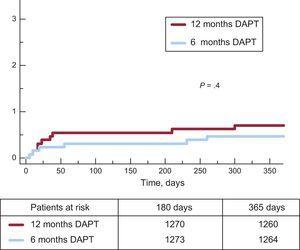
Incidenza cumulativa di trombosi stent definita o probabile in entrambi i gruppi. DAPT, doppia terapia antiaggregante piastrinica.
Risultati Da 6 a 12 Mesi
| 6-mese DAPT (n = 1272)* | 12-mese DAPT (n = 1270)* | P | |
|---|---|---|---|
| endpoint Primario | |||
| morte Cardiaca, infarto miocardico, rivascolarizzazione o BARC ≥ 3 sanguinamento | 38 (2.9) | 54 (4.2) | .1 |
| Endpoint secondari | |||
| Morte per tutte le cause | 7 (0.55) | 8 (0.60) | .8 |
| Morte cardiaca | 3 (0.23) | 4 (0.31) | .8 |
| Infarto miocardico | 3 (0.23) | 5 (0.40) | .8 |
| Rivascolarizzazione | 32 (2.5) | 44 (3.5) | .2 |
| Definitiva trombosi | 0 (0.0) | 0 (0.0) | |
| certi e probabili trombosi | 2 (0.15) | 2 (0.15) | .9 |
| BARC ≥ 3 eventi emorragici | 2 (0.15) | 5 (0.40) | .5 |
BARC, Bleeding Academic Research Consortium; DAPT, doppia terapia antiaggregante piastrinica.
I dati sono espressi come n. (%).
Numero di pazienti vivi al follow-up di 6 mesi.
Le analisi dei sottogruppi non hanno rivelato interazioni significative. Da notare, nel sottogruppo di pazienti con o senza infarto miocardico con elevazione del segmento ST, che comprendeva il 15% dei pazienti nel gruppo DAPT a 6 mesi e il 16,2% nel gruppo DAPT a 12 mesi, l’endpoint primario è stato raggiunto rispettivamente nel 7,7% e nell ‘ 8,1% (P = .8).
DISCUSSIONE
I risultati di questo studio suggeriscono che, in pazienti selezionati (che rappresentano circa il 40% dei pazienti trattati con DES), un regime di DAPT a 6 mesi sembra essere sicuro quanto un regime di DAPT a 12 mesi dal punto di vista dei tassi di eventi ischemici.
L’uso di DES riduce significativamente la necessità di ripetere la rivascolarizzazione coronarica. I DES di nuova generazione, in particolare gli stent a eluizione di everolimus, sono collegati a riduzioni dei tassi di trombosi rispetto ai DES di prima generazione o anche ai BMS.3-7 Pertanto, una limitazione importante per l’uso di DES risiede nella necessità di un regime di DAPT a più lungo termine rispetto al regime di DAPT a 1 mese dopo l’impianto di BMS. Il DAPT a lungo termine è associato a un rischio di sanguinamento più elevato e a un costo maggiore. Queste limitazioni spiegano perché, in alcuni contesti senza restrizioni apparenti sull’uso del DES, fino al 15-20% dei pazienti sembra non trarre beneficio dal DES, specialmente tra la popolazione anziana.
Diversi studi hanno confrontato un breve periodo da 3 a 6 mesi con un periodo più lungo da 12 a 24 mesi.10-16 Un’analisi congiunta dei primi 4 studi ha pubblicato prove dell’assenza di una differenza significativa negli eventi ischemici tra i periodi più brevi e più lunghi, ma l’incidenza di sanguinamento era più alta nel periodo più lungo.17 Tre prove aggiuntive riguardanti periodi DAPT brevi o lunghi sono state presentate molto recentemente.14-16 Il test di sicurezza14 ha confrontato DAPT a 6 mesi vs 12 mesi in 1399 pazienti a basso rischio trattati con DES di seconda generazione in angina stabile o instabile (l’infarto come indicazione per l’intervento coronarico percutaneo è stato escluso). Non sono state osservate differenze per nessuno degli endpoint clinici a 12 mesi. La limitazione principale era la dimensione del campione, la bassa aderenza al protocollo (il 34% dei pazienti assegnati a 6 mesi ha continuato il DAPT dopo 6 mesi) e l’inclusione di pazienti anatomicamente a basso rischio. Nello studio ITALIC, 15 1894 pazienti con dimostrata non resistenza all’acido acetilsalicilico sono stati randomizzati a 6 mesi vs 24 mesi DAPT dopo l’impianto di un Xience®. stent. Non sono state riscontrate differenze per nessuno degli endpoint clinici, comprese le complicanze emorragiche. Infine, lo studio ISAR-SAFE, 16 che non è stato ancora pubblicato, era previsto per reclutare 6000 pazienti, ma è stato interrotto dopo l’inclusione di 4000 pazienti. Questi sono stati randomizzati a 6 mesi o 12 mesi-DAPT dopo l’impianto di DES (89% di nuova generazione). Anche in questo caso, non sono state osservate differenze in nessuno degli endpoint di efficacia o sicurezza.
Tuttavia, questi studi presentano alcune limitazioni. Essendo studi clinici, la loro rappresentatività clinica è limitata, l’aderenza al protocollo è stata inadeguata, sono stati utilizzati 10, 14 DES di prima generazione,10,11, 16 e BMS, 10 resistenza all’acido acetilsalicilico è stata pretestata, 15 e la prima versione di stent a eluizione di zotarolimus, con perdita di lume tardiva vicina a quella di BMS, sono stati ampiamente o10,12,13
Il grande studio DAPT25 ha valutato un periodo di DAPT più lungo di 12 mesi dopo l’impianto del DES. In tale studio, i pazienti con un periodo di 12 mesi senza eventi dopo l’intervento coronarico percutaneo sono stati randomizzati alla sospensione del DAPT in quel momento o ad un periodo prolungato di DAPT (fino a 30 mesi). Sono stati inclusi i pazienti trattati con DES di prima e seconda generazione. Il periodo di DAPT più lungo (30 mesi) ha determinato una diminuzione degli eventi avversi cardiaci ma un aumento del sanguinamento rispetto al periodo di 12 mesi. Tuttavia, il tipo DES ha raggiunto l’interazione per l’endpoint (hazard ratio = 0,52 per lo stent di eluizione paclitaxel e hazard ratio = 0.89 per lo stent everolimus-eluting con P=.048 per l’interazione).
Anche i registri clinici che valutano il rischio di trombosi dopo il ritiro precoce del DAPT sono limitati dalla loro progettazione retrospettiva.8,9 Diversi pregiudizi sono notevoli, poiché l’interruzione del trattamento potrebbe essere stata decisa dopo un’attenta considerazione del rischio di trombosi. C’è una mancanza di grandi registri prospettici dalla pratica del mondo reale che valuta periodi DAPT più brevi.
Infine, una caratteristica importante che limita l’applicabilità di un regime di DAPT a breve termine è che i pazienti nel contesto di un evento coronarico instabile (la maggior parte dei pazienti sottoposti a intervento coronarico percutaneo al giorno d’oggi) beneficiano di un periodo di DAPT di 12 mesi rispetto a un periodo di trattamento di 1 mese.18,19 Tuttavia, non sappiamo se questo beneficio viene mantenuto quando un regime di 12 mesi viene confrontato con un regime di 6 mesi. Pertanto, la discussione rimane aperta e sono giustificati studi prospettici e/o registri adeguatamente progettati utilizzando DES di attuale generazione.
Seguendo queste considerazioni, abbiamo cercato di progettare questo registro ESTROFA-DAPT prospettico multicentrico valutando un regime DAPT di 6 mesi. I criteri di inclusione sono stati selezionati per incorporare principalmente pazienti con malattia coronarica stabile. Per quanto riguarda i pazienti instabili, abbiamo incluso solo quelli con angina instabile e nessun aumento dei marcatori cardiaci. Abbiamo anche incluso pazienti con infarto miocardico con elevazione del segmento ST o infarto miocardico con elevazione del segmento ST con un rischio di sanguinamento che non ha necessariamente evitato la necessità di DES a favore di un’opzione BMS. Diversi punteggi di rischio di sanguinamento in ospedale sono disponibili per l’uso in pazienti con ACS, ma questi algoritmi non sono stati progettati o standardizzati per prevedere il rischio di sanguinamento nell’ambito del DAPT a lungo termine. Pertanto, questa decisione è stata lasciata alla discrezione degli investigatori per considerare l’equilibrio tra restenosi e rischio di sanguinamento. Per quanto riguarda la procedura, sono stati esclusi i pazienti con stent per le lesioni coronariche principali di sinistra, così come le biforcazioni trattate con una strategia a 2 stent o i pazienti che richiedono più di 3 stent, dato il rischio considerevolmente più elevato di trombosi dello stent in questi casi10.
Per poter confrontare efficacemente i risultati della nostra serie di coorti DAPT di 6 mesi rispetto a 12 mesi, abbiamo utilizzato la coorte DAPT di 12 mesi dal database degli studi ESTROFA-2.22 Questo registro pubblicato in precedenza includeva 4768 pazienti arruolati prospetticamente trattati con DES di seconda generazione e, tra questi, 4354 (91%) trattati con un regime di DAPT di 12 mesi secondo le linee guida esistenti in quel momento.
Sono state seguite due fasi per ottenere serie comparabili di pazienti da questi registri. In primo luogo, i pazienti in ESTROFA-2 che presentavano criteri di esclusione da ESTROFA-DAPT sono stati esclusi (in particolare quelli con lesioni coronariche principali a sinistra trattate, biforcazioni trattate con 2 stent, pazienti con più di 3 stent impiantati e quelli con precedente storia di trombosi tardiva del DES). In secondo luogo, è stato condotto un processo di corrispondenza del punteggio di propensione.
Infine, 2 gruppi comparabili in tutte le caratteristiche cliniche e procedurali sono stati inclusi nell’analisi dei risultati. Solo DES non di prima generazione sono stati inclusi in entrambi i registri con una proporzione simile per gli stent everolimus-eluting. Tuttavia, il modello di stent a eluizione di zotarolimus differiva, con Endeavor® utilizzato in DAPT a 12 mesi (ESTROFA-2) e Resolute® in DAPT a 6 mesi (ESTROFA-DAPT). Lo stent Endeavor®, la prima versione di stent a eluizione zotarolimus, ha mostrato una perdita di lumen tardiva vicina a quella del BMS (0,6 mm) mentre lo stent Resolute® ha mostrato una perdita di lumen tardiva di circa 0,15 mm. Infatti, le prove RESET e OPTIMIZE non hanno rilevato alcuna differenza tra DAPT di 3 mesi e 12 mesi con l’uso dello stent Endeavor®.12,13 Pertanto, questo fattore differenziale potrebbe aver influenzato negativamente i risultati nel gruppo DAPT a 6 mesi, ma questo sembra non essere stato il caso. Pertanto, questa differenza supporta i risultati dell’approccio DAPT a 6 mesi.
Limitazioni
Una limitazione importante del nostro studio è la mancanza di randomizzazione. I registri comportano il problema del bias secondario a fattori confondenti noti e sconosciuti non sempre contabilizzati dopo un attento aggiustamento statistico con analisi abbinate come il punteggio di propensione.
Tuttavia, sebbene gli studi randomizzati siano il disegno più appropriato per confrontare i trattamenti, i registri sono ancora un’importante fonte di conoscenza e informazioni date le avvertenze ben riconosciute degli studi randomizzati, come le dimensioni dei campioni limitanti i costi, l’inclusione restrittiva oltre i criteri di esclusione, la ricerca non indipendente o nessuna gestione e follow-up del paziente “full real-practice”.
Una seconda limitazione è la dimensione relativamente piccola del campione di vari sottogruppi, in particolare il sottogruppo ACS, che non consente di trarre conclusioni definitive sulla sicurezza DAPT a breve termine in tali contesti. Un’altra limitazione è la natura della selezione del paziente. Come descritto nei “Metodi”, lo studio è stato principalmente guidato dalla sicurezza. I sottogruppi con un beneficio dimostrato dopo 12 mesi di DAPT (pazienti con ACS senza alto rischio di sanguinamento)18,19 e quelli con un rischio più elevato di trombosi e che mostravano una tendenza al beneficio su DAPT più lungo negli studi, sono stati sistematicamente esclusi.10
Una considerazione importante riguarda i diversi periodi di tempo per l’assunzione in entrambi i registri. Tuttavia, la potenziale influenza di questo intervallo di tempo potrebbe essere stata attenuata dai seguenti fattori: a) Solo DES di nuova generazione sono stati utilizzati in entrambi i registri; b) Solo i pazienti trattati con clopidogrel sono stati inclusi nell’analisi. Nel più recente registro ESTROFA-DAPT, i pazienti non sono stati trattati con nuovi agenti antipiastrinici secondo il protocollo, in base ai criteri di inclusione (pazienti in condizioni cliniche stabili o dopo ACS ma con rischio di sanguinamento moderatamente elevato); c) La metodologia di entrambi i registri era abbastanza simile, come precedentemente menzionato nella sezione “Metodi”.
CONCLUSIONI
Un periodo di DAPT di 6 mesi dopo l’impianto di DES di nuova generazione sembra non inferiore a un regime di DAPT di 12 mesi nei contesti clinici e angiografici valutati in questo studio multicentrico.
FINANZIAMENTO
Questo studio è stato finanziato dal gruppo di lavoro spagnolo di cardiologia interventistica per i moduli di case report basati sul Web (CRF) della Società spagnola di Cardiologia.
CONFLITTI DI INTERESSE
Nessuno dichiarato.