Introduzione
Un’interpretazione adeguata dei marcatori di necrosi miocardica è essenziale per la diagnosi, la stratificazione e il trattamento di pazienti con sospetta sindrome coronarica acuta (ACS). I protocolli sui marcatori cardiaci dell’infarto miocardico acuto (AMI) sono riferiti alla terza definizione universale di AMI.
Questo documento stabilisce che l’elevazione e l’abbassamento della troponina cardiaca (cTn) è fondamentale per stabilire la diagnosi nel contesto di sintomi ischemici, cambiamenti elettrocardiografici o alterazioni segmentali appena manifestate in uno studio di imaging.1
I progressi tecnologici nella determinazione del cTn hanno migliorato la capacità di rilevare e quantificare il danno cellulare miocardico. I criteri di elevazione dei valori cTn dipendono dalla prova utilizzata e devono essere definiti sulla base del profilo di precisione di ciascuna prova, compresa quella di prova ad alta sensibilità.2 L’esistenza di diverse commerciale crt analisi immunologiche con diversa percentile 99 (p99) concentrazioni; il fatto che alcuni laboratori utilizzano diversi riferimenti al danno miocardico risultati del test (“normale”, “indeterminato” o “suggestivi”); e l’uso indiscriminato del crt test in grandi popolazioni con differenti probabilità di presentare ACS, tendono a generare confusione nel contesto della gestione clinica.
Vi è un numero significativo di pazienti che in assenza di AMI presentano comunque concentrazioni cTn>p99. Questi pazienti di solito hanno fattori di rischio cardiovascolare e la probabilità di complicanze in tali individui è simile a quella dei pazienti con ACS.3
Le ultime raccomandazioni europee sulla gestione di pazienti con sindrome coronarica acuta non elevata (NSTE-ACS) sostengono l’uso di cTn ad alta sensibilità (hs-cTn) rispetto alle troponine convenzionali o di quarta generazione (4G) e contemplano fino a due algoritmi (0h/3h, 0h/1h) per la conferma (regola in) o l’esclusione (regola fuori) dell’AMI.4
Le troponine cardiache sono estremamente specifiche del danno miocardico. Tuttavia, in nessun modo il danno miocardico è esclusivo di ACS. Di conseguenza, le guide cliniche sottolineano che la concentrazione cTn deve essere interpretata in relazione ai sintomi del paziente. A questo proposito, elevate concentrazioni di cTn in pazienti con sepsi, crisi ipertensive, embolia polmonare, ecc., sono indicativi di danno del miocardio, ma non di AMI e non dovrebbero essere usati per indicare i trattamenti specifici per ACS.5
Il termine “alta sensibilità” dovrebbe essere riservato a quei test immunologici in grado di determinare p99 con un coefficiente di variazione (CV) di 6
Vi sono dubbi nella comunità scientifica sul fatto che l’uso di hs-cTn rappresenti un miglioramento clinico significativo e se implichi più test e interconsultazioni.7 Il presente studio è stato condotto per valutare le prestazioni diagnostiche della troponina T ad alta sensibilità (hs-TnT), determinare se riduce il tempo alla diagnosi e analizzare le conseguenze cliniche del suo uso.
Metodo
prospettico, longitudinale studio osservazionale è stato condotto in ospedale, i servizi di emergenza (HES) di Hospital Clínico (Valencia), l’Ospedale istituto Clinico (Malaga), Ospedale Severo Ochoa (Leganés), Ospedale Sant Pau (Barcellona) e l’Ospedale Miguel Servet (Zaragoza)(Spagna), che coinvolgono i pazienti di TUSCA (Troponina Ultrasensible en el SCA) trial8 tra giugno 2009 e aprile 2010. Lo studio è stato condotto in conformità con i principi della Dichiarazione di Helsinki ed è stato approvato dai Comitati etici locali dei centri partecipanti. Il consenso informato scritto è stato ottenuto da tutti i pazienti. Abbiamo incluso consecutivamente pazienti di età superiore ai 18 anni osservati nell’HES a causa di dolore toracico indicativo di NSTE-ACS. L’iscrizione del paziente è stata effettuata durante l’assistenza iniziale nell’HES, dopo la valutazione dei criteri di inclusione ed esclusione. La gestione del paziente e il trattamento applicato hanno seguito protocolli interni basati sulle guide di consenso della Società Europea di Cardiologia, sotto le indicazioni dei medici responsabili dei pazienti in ogni momento e con totale indipendenza di partecipazione allo studio. Le determinazioni cTn seriali 4G sono state effettuate per la diagnosi di ACS, in conformità con la pratica clinica e immunologica di routine in ciascun centro.
Le caratteristiche del paziente sono state inserite in un modulo case report e comprendono dati demografici, tempo riferito all’insorgenza dei sintomi, presenza di fattori di rischio (ipertensione arteriosa, diabete mellito, broncopneumopatia cronica ostruttiva , insufficienza cardiaca e insufficienza renale). Abbiamo anche registrato le caratteristiche dell’ECG con e senza dolore, nonché le informazioni relative alla gestione dopo le cure di emergenza iniziali (cateterizzazione, angioplastie, chirurgia di bypass, ecc.), la diagnosi finale e la destinazione del paziente.
I pazienti con ACS di elevazione del segmento ST sono stati esclusi, così come quelli con blocco del fascio sinistro appena manifestato, defibrillazione o cardioversione prima delle prime determinazioni di laboratorio, chirurgia cardiaca nelle tre settimane prima del ricovero, donne in gravidanza, pazienti con grave deterioramento cognitivo e soggetti con insufficienza renale cronica sottoposti a emodialisi.
Durante le prime 12 ore di permanenza in HES, Unità di terapia intensiva (ICU) o reparto ospedaliero, sono stati ottenuti campioni di sangue seriali per la misurazione di hs-TnT, sulla base del seguente protocollo:
- –
Campione T0. Al momento della prima assistenza nel HES.
- –
Campione T1. Due ore dopo il timepoint di campionamento 0 o immediatamente prima del ricovero in qualche unità ospedaliera (ICU o reparto).
- –
Campione T2. Tra 4 e 6 ore dopo il campionamento timepoint 0 o immediatamente prima del ricovero in qualche unità ospedaliera.
- –
Campione T3. Tra 8 e 12 ore dopo il campionamento timepoint 0 se il paziente era ancora in servizio, o immediatamente prima del ricovero in qualche unità ospedaliera, o al momento della dimissione del paziente dal HES.
È stato raccolto sangue sufficiente per ottenere 5 aliquote di 0,5 ml di plasma eparinizzato da ciascuno dei campioni del paziente, oltre al campione richiesto per i test di routine. Le aliquote sono state congelate a -80°C e sono state identificate con il codice di ciascun centro: tre cifre corrispondenti al numero del paziente e al timepoint di raccolta (T0, T1, T2 o T3), a seconda del campione coinvolto. Sono stati ottenuti in media 3,7 campioni per paziente. Tutti i campioni sono stati trasferiti al laboratorio principale (Ospedale Sant Pau, Barcellona) per l’analisi di 4G cTn e hs-TnT, con non più di un mese di tempo trascorso da ogni raccolta. Tutti gli ospedali hanno eseguito il test di routine 4G cTn utilizzato al momento (2 centri con cTnT e 3 con cTnI). La diagnosi finale del paziente è stata stabilita da un esperto, sulla base di tutte le informazioni cliniche fornite dal modulo di case report compilato dal ricercatore principale in ciascun centro, riflettendo i dati clinici e ECG e la determinazione centralizzata 4G cTn effettuata nel laboratorio principale. L’esperto è stato accecato alle determinazioni hs-cTn.
L’infarto è stato diagnosticato in presenza di un aumento o riduzione della concentrazione cTnT di >20% (criterio Δ) tra diversi campioni, con almeno un valore maggiore di p99 per la popolazione di riferimento (≥ 0,01 µg/l). La diagnosi di angina instabile (UA) è stata stabilita in pazienti con evidenza clinica di ischemia miocardica senza cTn 4G positivo. I pazienti con UA hanno presentato una storia di angina a riposo, peggioramento della precedente angina cronica, cambiamenti del segmento ST indicativi di ischemia senza variazioni del biomarcatore (cinetica), test di rilevamento dell’ischemia positivi o stenosi>70% di un’arteria coronaria come evidenziato dall’angiografia coronarica. I livelli di cTnT a loro volta sono stati misurati utilizzando una tecnica ad alta sensibilità su un analizzatore Cobas e601 (hs-TnT, Roche Diagnostics, Basilea, Svizzera). La tecnica ha un limite di rilevazione di 5.0 ng/l, e il riferimento p99, utilizzato come la decisione clinica limite, era 13.0 ng/l. L’imprecisione analitica di questi crt test è stato valutato in 20 ripetizioni di 8 gruppi di campioni con fine concentrazioni regolato per coprire l’intervallo tra 7 e 928ng/l, diluendo un alto cTnT concentrazione del campione con un siero piscina presentare inosservabile hs-TnT livelli (
ng/l). Il p99 del test cTnT (10ng/l=0,01 µg/l) è stato misurato con un coefficiente di variazione (CV) del 15,2%. Il valore con CV 10% era 35ng / l=0,035 µg / l. Il p99 del test hs-TnT (13ng/l) è stato misurato con un CV del 6,9%.
Frequenze e percentuali sono state calcolate per l’analisi descrittiva delle variabili qualitative, con misure di tendenza centrali nel caso delle variabili quantitative. I dati sono stati espressi come media e deviazione standard (SD) in presenza di una distribuzione normale e come intervallo mediano e interquartile (IQR) nel caso di una distribuzione non normale come evidenziato dal test di Kolmogorov-Smirnov.
Il confronto delle variabili quantitative era basato sul t-test dello Studente o Mann–Whitney U-test in presenza o assenza di una normale distribuzione dei dati, rispettivamente. Il confronto delle variabili qualitative a sua volta è stato basato sul test chi-quadrato o sul test esatto di Fisher, a seconda dei casi.
In tutti i casi il livello di significatività statistica è stato definito come 5% (α=0,05%) nei test a due code.
Lo studio di discriminazione 4G cTn e hs-TnT è stato effettuato calcolando l’area (AUC) sotto la curva ROC (Receiver Operating Characteristic) ai diversi timepoint di campionamento, con il corrispondente intervallo di confidenza (CI) del 95%. La significatività di queste curve è stata valutata a partire dal calcolo dell’IC dell’AUC, definendo come significativi quei valori nell’area con un limite inferiore superiore allo 0,5%. Il confronto delle aree sotto la curva ROC è stato effettuato studiando la sovrapposizione dei valori CI.
Le prestazioni diagnostiche sono state valutate calcolando la sensibilità, la specificità e i valori predittivi positivi e negativi. L’intervallo di confidenza del 95% è stato calcolato per la valutazione clinica dell’entità di queste misure – l’intervallo è considerato significativo in assenza di sovrapposizione dei valori.
Risultati
Lo studio comprendeva un totale di 351 pazienti; 234 erano maschi (67,9%) e l’età media era di 65,7 anni. I principali dati demografici e fattori di rischio cardiovascolare sono riassunti nella Tabella 1. Una diagnosi finale di AMI è stata stabilita in 77 pazienti, con UA in 102 pazienti. A un totale di 172 pazienti è stata diagnosticata la mancanza di ACS.
Caratteristiche e fattori di rischio cardiovascolare del campione in studio.
| le Variabili | Totale | No ACS | angina Instabile | AMI | p |
|---|---|---|---|---|---|
| No. pazienti n (%) | 351 | 172 (49) | 102 (29.1) | 77 (21.9) | – |
| Età (mediana) | 66 (27-93) | 64.4 (27-93) | 71 (31-90) | 73 (36-88) | |
| Maschi, % | 67.9 | 61.5 | 73.5 | 74 | |
| storia di Malattia n (%) | |||||
| AHT | 220 (62) | 101 (58.7) | 73 (71.6) | 46 (59.6) | NS |
| il Diabete | 92 (26.2) | 38 (22.1) | 35 (34.3) | 19 (24.7) | NS |
| insufficienza Cardiaca | 52 (14.8) | 20 (11.6) | 20 (19.6) | 12 (15.6) | NS |
| la velocità di filtrazione Glomerulare (ml/min/1.73 m2 disposte) | 79.6 | 81.9 | 80.7 | 72.9 | |
| TnT µg/l (mediana) | 0.285 (0.01–6.87) | 0.009 (0.001–0.46) | 0.009 (0.009–0.03) | 0.066 (0.009–6.870) | |
| Hs-TnT ng/l (mediana) | 63.87 (2.99–7.096) | 5.5 (1.2–481.6) | 11.69 (1.99–66) | 90.4 (2.9–7.096) | |
| NT-proBNP pg/ml (mediana) | 1.130 (5.46255) | 141 (5-13.302) | 238.5 (16.4–9.164) | 589 (41-46.255) | |
| Elettrocardiogramma con dolore (70.67%) | |||||
| Normale | 103 (41.1) | 70 (61.4) | 22 (27.5) | 11 (20) | |
| T neg | 57 (23) | 21 (18.6) | 23 (28.8) | 13 (23.6) | |
| ↓ ST | 60 (24.5) | 9 (8) | 26 (32.6) | 25 (45.4) | |
| Evoluzione dei sintomi (min.) (88%) | |||||
| ≤ 3h (%) | 46 | 63 (42) | 43 (44.8) | 41 (55.4) | 0.16 |
| >3h (%) | 57 | 87 (58) | 53 (55) | 33 (44.6) | NS |
| Catheterization | 36.9 | 12 (7) | 64 (62.7) | 53 (68.8) | |
| Angioplasty | 20.9 | 2 (1.2) | 29 (28.4) | 41 (53.2) | |
| Stent | 18.7 | 1 (0.6) | 28 (27.5) | 35 (45.5) | |
| Bypass | 2.2 | 0 | 4 (3.9) | 4 (5.2) | |
| servizio di Emergenza di scarico | 41.1 | 128 (74.7) | 10 (10.9) | 5 (6.6) | |
| alla dimissione dall’Ospedale | 57.8 | 44 (25.3) | 92 (88.1) | 72 (91) | |
| Morte | 1.1 | 0 | 1 (1.9) | 3 (3.8) | |
AHT: ipertensione arteriosa; AMI: infarto miocardico acuto; NS: non significativa; NT-proBNP: brain natriuretic peptide; ACS: sindrome coronarica acuta; TnT: troponina T; hs-TnT: alta sensibilità troponina T.
Un totale di 55,4% dei pazienti con AMI raggiunto HES entro le prime tre ore, mentre una percentuale maggiore di coloro con UA e quelli senza ACS è arrivato dopo tre ore. Per quanto riguarda la positività dei marcatori secondo la diagnosi finale, l ‘ 87% dei pazienti con diagnosi finale di AMI ha presentato 4G cTn>0,035 µg/l durante le prime 12 ore dello studio. Nel caso di pazienti non ACS e quelli con UA, la positività è stata registrata nel 4% dei casi. La concentrazione di hs-TnT era > 13ng / l (p99)nel 26,7% e nel 46% dei pazienti con diagnosi di non-ACS e UA, rispettivamente (Fig. 1). D’altra parte, 4G cTn utilizzando p99 con un punto di cut-off di 0.01µg / l (il gold standard dello studio) si è rivelato positivo nel 16% dei pazienti con diagnosi di UA e nell ‘ 11% di quelli senza ACS.
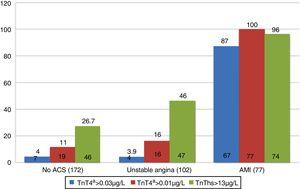
Positività del marcatore secondo la diagnosi finale. AMI: infarto miocardico acuto; ACS: sindrome coronarica acuta; TnT: troponina T; hs-TnT: alta sensibilità troponina T.
Applicando la cinetica tra alcune delle quattro determinazioni (criterio Δ), il 21,5% dei pazienti con UA ha mostrato un aumento di hs-TnT+Δ (Fig. 2).

Positività + Δ dei marcatori in base alla diagnosi finale. AMI: infarto miocardico acuto; ACS: sindrome coronarica acuta; TnT: troponina T; hs-TnT: alta sensibilità troponina T.
Alla prima misurazione (T0), la sensibilità diagnostica di hs-TnT era significativamente maggiore di quella di 4G cTn (CV) (87,0%; 83,0–90,3% vs. 42,9%; 37,6–48,2%; p
0,05), risultando in un valore predittivo negativo del 95,1%. Tuttavia, la sua specificità (71,5%; 66,5–76,2% vs 97,4%; 95,2–98,8%; p0.05) e il valore predittivo positivo (46,2% vs 82,5; p0.05) erano chiaramente inferiori a quelli di 4G cTn (CV). Analizzando l’area sotto la curva ROC, hs-TnT è stato visto essere superiore a 4G cTn (CV) (0.792; 0.746–0.833 vs. 0.701; 0.650–0.748) (Fig. 3 e 4).
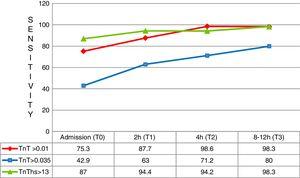
Sensibilità ai diversi tempi di test. TnT: troponina T; hs-TnT: alta sensibilità troponina T.
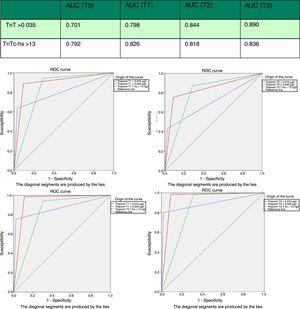
Area sotto la curva (AUC) di hs-TnT e TnT 4G nelle curve ROC (Sampling and Receiver Operating Characteristic). AUC: area sotto la curva; TnT: troponina T; hs-TnT: alta sensibilità troponina T.
Due ore dopo l’arrivo del paziente nell’HES (T1), hs-TnT ha continuato a mostrare una sensibilità diagnostica molto più elevata rispetto a 4G cTn (94,4%; 91,3–96,6 vs. 63,0%; 57,6–68,2; p0.05). Il valore predittivo negativo di hs-TnT era praticamente assoluto (97,9%) e la sua accuratezza diagnostica tendeva ad essere superiore a quella di 4G cTn (ROC 0,826 vs. 0,798). La bassa specificità di hs-TnT ha determinato un basso valore predittivo positivo (46,5%). Il resto dei risultati del campionamento si è rivelato simile, sebbene riflettendo prestazioni diagnostiche minori.
Nelle prime tre ore dopo l’insorgenza dei sintomi, un totale di 41 pazienti è arrivato con una diagnosi finale di AMI. In questi casi la sensibilità diagnostica superiore di hs-TnT rispetto a 4G cTn (CV) e anche 4G cTn (p99) è stata particolarmente significativa, con una sensibilità di 87.8% contro 36.6% e 73.2%, rispettivamente (Fig. 5).
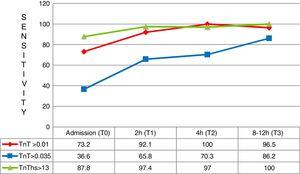
Sensibilità ai diversi tempi di test per i pazienti con insorgenza dei sintomi min. TnT: troponina T; hs-TnT: alta sensibilità troponina T.
I pazienti con diagnosi di infarto miocardico senza innalzamento della ST (n=36) e con lunghi tempi evolutivi (> 3h) hanno mostrato una minore accuratezza diagnostica con hs-TnT (a causa della minore specificità) rispetto ai pazienti con un tempo più breve dall’insorgenza dei sintomi. Applicando la cinetica, è stato nuovamente osservato un aumento della specificità, con un aumento dell’AUC. Di conseguenza, nel caso di hs-TnT, abbiamo iniziato con una specificità del 69% e, applicando Δ, la specificità ha raggiunto l ‘ 85%, con un valore predittivo positivo del 55,3%, che ha migliorato le prestazioni diagnostiche complessive (Tabella 2).
Cinetica (Δ) delle diverse troponine cardiache in pazienti con insorgenza dei sintomi >180min.
| Sensibilità | Specificità | PPV, % | NPV, % | AUC | |
|---|---|---|---|---|---|
| cTnT>0.01+Δ | 100% (97.9–100) | 96.4% (92.4–98.6) | 86.8 | 100 | 0.982 |
| cTnT>0.035+Δ | 81.8% (75.2–87.2) | 97.9% (94.4–99.4) | 90.0 | 95.8 | 0.898 |
| hs-TnT>13+Δ | 78.8% (71.9–84.6) | 85.0% (78.8–89.9) | 55.3 | 94.4 | 0.818 |
AUC: area sotto la curva; cTnT: la troponina cardiaca T; hs-TnT: troponina T ad alta sensibilità; PPV: valore predittivo positivo; VAN: valore predittivo negativo.
Inoltre, abbiamo valutato i punti di cut-off ottimali derivati dall’analisi ROC. Il punto ottimale è stato stabilito come 37ng / l (hs-TnT-ROC) (Tabella 3). Il valore per hs-TnT-ROC presentava una sensibilità di 59.7 – – molto inferiore a quello di hs-TnT, ma maggiore di quello di 4G TnT – CV) – e una specificità del 95,3% nella prima misurazione. Questa maggiore sensibilità rispetto al TnT 4G (CV) persisteva nel resto dei campionamenti.
Confronto delle prestazioni diagnostiche di hs-TnT ROC (> 37).
| T0 | Sensitivity, % | Specificity, % | EFF, % | LR+ | LR− | PV+, % | PV−, % |
|---|---|---|---|---|---|---|---|
| cTnT>0.01 | 75.3 | 91.2 | 87.7 | 8.60 | 0.27 | 70.7 | 92.9 |
| cTnT>0.035 | 42.8 | 97.5 | 85.5 | 16.8 | 0.59 | 82.5 | 85.8 |
| hs-TnT>13 | 87 | 71.5 | 74.9 | 3.1 | 0.18 | 46.2 | 95.1 |
| hs-TnT>37 | 59.7 | 95.3 | 87.5 | 12.6 | 0.42 | 78 | 89.4 |
cTnT: la troponina cardiaca T; hs-TnT: alta sensibilità troponina T.
Il risparmio di tempo per giungere ad una diagnosi quando si utilizza hs-TnT contro 4G crt (CV) è stato 113min. Il risparmio a sua volta sarebbe di 147 minuti (p0.001) nel caso di pazienti ricoverati in meno di 3 ore dall’insorgenza dei sintomi e di 63 minuti (p=0,024) nel caso di pazienti ricoverati in oltre tre ore dall’insorgenza dei sintomi.
Discussione
I dati ottenuti nel presente studio sono in grado di chiarire alcune questioni riguardanti l’uso di hs-TnT nel processo decisionale, in considerazione della forte evidenza della sua utilità come strumento diagnostico e prognostico in ACS. Alla fine, le prestazioni diagnostiche del nostro hs-TnT sono risultate superiori a quelle del cTn 4G in ciascuno dei diversi timepoint di campionamento. Le prestazioni a loro volta sono state osservate diminuire nelle ore successive all’insorgenza dei sintomi. Nel nostro studio abbiamo utilizzato cambiamenti relativi tra due campioni (in particolare 20%) che hanno discretamente migliorato il valore predittivo positivo, anche se senza diventare di uso pratico. A questo proposito, un Δ del 20% potrebbe essere troppo piccolo e, come proposto da alcuni autori, avrebbe potuto essere consigliabile aumentare Δ ad una percentuale più alta, poiché molti casi di AMI sono risultati essere a valori discretamente superiori al limite di riferimento superiore (URL).9,10 Altri ricercatori propongono cambiamenti relativi di Δ (tra 30 e 250%) per aumentare la specificità diagnostica e migliorare la diagnosi di AMI.11-14 Mueller et al.15 risultati pubblicati che spiegano perché i cambiamenti relativi di Δ non riescono a governare nell’infarto miocardico con elevazione non ST. Con l’uso di cambiamenti assoluti di Δ, un aumento o una diminuzione di almeno 9,2 ng/l per la popolazione di pazienti con ACS e non-ACS, o di 6,9 ng/l per una popolazione con ACS, sembra essere più adeguato rispetto ai cambiamenti relativi di Δ per escludere l’AMI. Oltre a questi problemi con la diminuzione della specificità, ci sono differenze nell’URL in base al test utilizzato. Ciò evidenzia l’importanza della razza, del sesso, dell’età o del numero di partecipanti allo studio,16 e aggiunge una maggiore difficoltà nel raggiungere il consenso nel prendere decisioni.
Nel nostro studio, la superiorità della sensibilità di hs-TnT nella diagnosi di infarto miocardico con elevazione non ST è risultata maggiore nei pazienti con insorgenza di sintomi recenti, in concordanza con i risultati di altri autori.17,18 Per un paziente che riporta dolore toracico per meno di tre ore, e con una seconda determinazione negativa due ore dopo l’arrivo, possiamo escludere l’AMI in quasi il 100% dei casi. Questo, combinato con i risultati clinici ed ECG, può identificare i candidati per la dimissione precoce e la gestione ambulatoriale. D’altra parte, i pazienti con diagnosi di infarto miocardico con elevazione non ST e che presentano lunghi tempi evolutivi (oltre 3h) mostrano una minore precisione diagnostica con hs-TnT, anche quando si eseguono due determinazioni seriali. In questi casi dovremmo valutare i punti di cut-off ottimali derivati dall’analisi ROC. Nel nostro studio il punto di cut-off era 37ng / l, che ci permetterebbe di “governare”, cioè i pazienti con punteggi superiori a questo punto di cut-off avrebbero una probabilità molto alta di presentare AMI. È stato anche sostenuto che questa diminuzione della specificità è stata sottovalutata in letteratura e che non riflette i pazienti osservati negli HES dei nostri ospedali, dove l’età media, le comorbidità e gli aumenti della cTn tendono ad essere elevati.
Il tempo per la diagnosi è stato notevolmente ridotto (da 247 a 71.5 min).19,20 Nel nostro studio è il risparmio di tempo per la diagnosi di linfoma non-ST elevation infarto miocardico era 147min nel caso di pazienti di reporting meno di tre ore dopo che i sintomi di esordio e 63min quando reporting dopo 3h.
Venti-due dei pazienti (il 21,5%) con diagnosi di UA allo scarico può essere non-ST elevation myocardial infarction casi dopo due determinazioni di hs-TnT con cinetica di oltre il 20% tra di loro. Fino a 13.il 9% dei pazienti non-ACS (n=24) mostrerebbe positività con hs-TnT all’applicazione di tale cinetica e corrisponderebbe ad altre condizioni di malattia che causano danni cardiaci progressivi, come miocardite, embolia polmonare o sindrome di takotsubo. Diverse analisi hs-TnT rilevano fino al 27% in più di casi di AMI rispetto al metodo attuale in pazienti con dolore toracico e una probabilità bassa o intermedia di ACS.20,21 Si potrebbe anche ipotizzare che la diagnosi di UA scomparirebbe, come sottolineato da Sabatine et al.22 in pazienti con test di esercizio positivo valutati con tecniche ultrasensibili. In questo studio, hs-TnI era rilevabile in tutti i pazienti prima dei test; è rimasto senza cambiamenti nei pazienti senza ischemia; e aumentato del 24% in quelli con ischemia lieve e del 40% in quelli con ischemia da moderata a grave. Non sono state osservate modifiche con 4G cTn. Di conseguenza, i risultati riferiti alla diagnosi di infarto miocardico con elevazione non ST utilizzando cTn convenzionale sono motivo di preoccupazione, poiché il danno miocardico ha una misura limitata e i valori cTn non sempre aumentano precocemente, o i loro incrementi non sono sufficienti per consentire l’identificazione precoce.
Dovrebbero essere introdotti protocolli di soluzione rapida, per cui i nostri pazienti con basso rischio ischemico e un normale tracciamento ECG passerebbero solo 3-4 ore in ospedale.23,24 Si è riflettuto se una singola determinazione hs-TnT sia sufficiente per escludere l’AMI,25 e altri studi hanno valutato la possibilità di una singola determinazione se il valore hs-TnT è
ng/l (cioè non rilevabile).24 Tutte queste situazioni devono essere considerate in futuro.Conclusioni
Test di troponina T ad alta sensibilità migliora le prestazioni diagnostiche, riduce il tempo alla diagnosi di AMI ed è in grado di identificare un numero maggiore di pazienti con infarti più piccoli, che in precedenza erano diagnosticati come UA e che hanno un alto rischio di mortalità, rispetto al cTn convenzionale. Inoltre, riduce il tempo per escludere i casi, poiché l’AMI potrebbe essere scartata entro 2h. Tutto ciò comporta un trattamento precoce per i pazienti con necrosi miocardica e un accorciamento della permanenza del paziente nell’HES. Tuttavia, in quegli individui che riferiscono all’HES dopo tre ore di insorgenza dei sintomi, hs-TnT non sarebbe in grado di migliorare le prestazioni diagnostiche del cTn 4G e il processo decisionale dovrebbe quindi essere più attento. I test hs-cTn stanno cambiando la gestione e il concetto di pazienti con dolore toracico suggestivo di ACS. Ciò rende necessario che i medici di emergenza e di assistenza critica si familiarizzino con il loro uso di routine.
Conflitto di interessi
Gli autori dichiarano di non avere conflitti di interesse.