膵臓嚢胞は、膵臓の異常 膵臓嚢胞性病変の約70%が偶然に発見されている。 最も頻繁に発生する腫瘍性膵臓嚢胞には、乳管内乳頭粘液性新生物(IPMN)、漿液性嚢胞腺腫(SCA)、卵巣間質を伴う粘液性嚢胞性新生物(MCN)、および固体偽乳頭上皮新 IPMNはさらに、分岐ダクト(BD)、メインダクト、および複合形態に細分されます。 一緒に、これらは前癌性膵臓、主に嚢胞性腫瘍の90%を構成する。 対照的に,偽嚢胞,真上皮嚢胞,リンパ上皮嚢胞,粘液性非腫よう性嚢胞は悪性の可能性を有さない。
悪性腫瘍は粘液嚢胞にのみ発生する。 SCAは非悪性病変と考えられ,文献で報告されている悪性しょう液性腫ようはSCNのWHO基準を満たすことは見出されていない。 IPMNは、低悪性度から高悪性度の異形成、そして最終的には膵管腺癌(PDAC)に進行する可能性があります。 主要な管を含むIPMNsに敵意の危険が62%であると推定されて枝のそれらより高い敵意率が、あります;MCNsの敵意のための危険は15%よりより少しです。 固体偽乳頭上皮新生物および嚢胞性膵臓神経内分泌腫瘍(cPNET)などの他のまれな嚢胞性病変は、通常、外科的除去につながる、特定の診断を示唆する特徴を
無症候性個体における付随的膵嚢胞の頻度を研究するために、クロムリーは集団ベースのコホート研究に登録された1077人の参加者において磁気共鳴胆管膵管造影(MRCP)検査を実施した。 元のグループのうち、676人は5年後に繰り返し検査を受けました。 最初の検査の時点で、49%は直径が2mm以上の少なくとも一つの嚢胞を有していた。 フォローアップ期間中の新しい嚢胞の発生率は年間2.6%であった。 嚢胞の存在は年齢に強く関連していた;75歳までに、参加者の75%が一つ以上の嚢胞を持っていた。 良性および前悪性または悪性膵嚢胞の間の識別は、放射線学的追跡検査または外科的切除などの不必要な処置を避けるために非常に重要である。
卵巣間質を伴う粘液性嚢胞性新生物(MCN)
Mcnは中年女性に共通しており、通常は明確に定義されており、主に膵臓の尾部にある(>90%)。 漿液性嚢胞性腫瘍と比較して、Mcnはより大きく(直径が>20mm)、それほど多くはない(通常<6)。 MCNsの生物学的挙動は可変であり、異なる組織学的パターンは、多くの場合、同じ腫瘍に共存しています。 腫瘍は粘液性のcystadenomasかintraductal papillary粘液性の腺腫があるように完全に温和であるかもしれません。 いくつかの腫瘍は境界線であり、細胞性異形成を示すが、他の腫瘍は率直に悪性である。 悪性嚢胞腺癌および髄内粘液癌は、さらに非侵襲的および侵襲的なタイプに細分される可能性がある。
(MCNsの放射線学的特徴は以下の画像で示されている。)
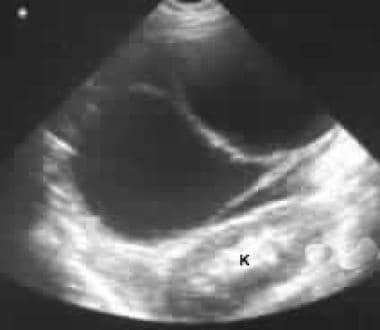 左のhypochondriumを通したSonogramは腎臓に前方の大きいseptateの固まりを示します(K)。
左のhypochondriumを通したSonogramは腎臓に前方の大きいseptateの固まりを示します(K)。 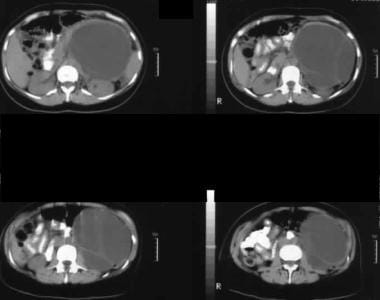 非強化軸方向CTスキャンを示しています。 画像1は、左のhypochondriumに大きな隔壁の塊を示しています。 粘液性嚢胞性新生物の典型的な滑らかな外部輪郭に注意してください。
非強化軸方向CTスキャンを示しています。 画像1は、左のhypochondriumに大きな隔壁の塊を示しています。 粘液性嚢胞性新生物の典型的な滑らかな外部輪郭に注意してください。 膵管内乳頭粘液新生物(IPMN)
膵管の関与に基づいて、Ipmnは、主膵管と側枝の両方を含む主管IPMN、側枝IPMN、または混合変異IPMNのいずれかに分類されます。 主管Ipmnはしばしば腸型上皮を有し、側枝Ipmnは通常胃型上皮を有する。 IPMNの全ての形態学的変異体は癌に進行することができるが,胃型Ipmnに由来する浸潤性腺癌は他のタイプのIpmnに由来するものよりも有意に悪い生存率と関連している。 しかし、イメージング機能は、IPMNsの様々な組織学的変異体を区別するために特異的ではありません。
側枝Ipmnは高齢の男性で一般的に検出され、より頻繁に近位膵臓に位置する(頭部および吻合プロセス)。 MCNとIPMNの重要な差別化機能は、膵管通信の可視化です。 すい管との明確なコミュニケーションチャネルが視覚化されると、SCAsおよびMCNsはすい管系と通信しないため、側枝IPMNの診断はほぼ確実である。
3cm以下の粘液性嚢胞性病変の攻撃性の発生率は低いにもかかわらず、発生率は病変を完全に却下するのに十分低くなく、画像機能の慎重なレビューが義務付けられている。 さらに、その状態が外科的管理に適していないことが判明した患者は、しばしば画像機能の成長および変化のための頻繁な評価を必要とする。
(Ipmnは下の画像に見られます。)
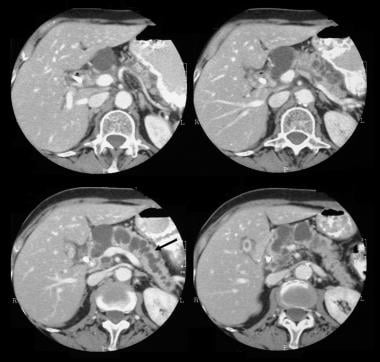 膵管内乳頭粘液腫よう(IPMT)。 膵臓を通る対照高められた軸CTスキャンは膵臓の頭部の5.5cm嚢胞性腫瘍を示します。 膵管の上流の総拡張に注意してください。 副膵管も拡張している。
膵管内乳頭粘液腫よう(IPMT)。 膵臓を通る対照高められた軸CTスキャンは膵臓の頭部の5.5cm嚢胞性腫瘍を示します。 膵管の上流の総拡張に注意してください。 副膵管も拡張している。 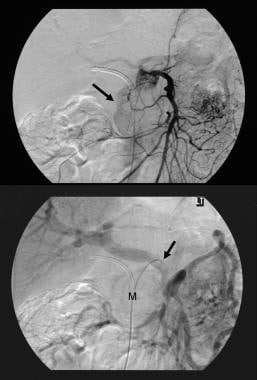 膵管内乳頭粘液腫よう(IPMT)。 (上)上腸間膜血管造影では、動脈期の間に膵頭の腫りゅうに毛細血管の血管性を示しています。 (下)門脈相画像は、門脈枝の変位と上腸間膜静脈と門脈の接合部の包摂を示している。 Mは膵臓の塊を示す。
膵管内乳頭粘液腫よう(IPMT)。 (上)上腸間膜血管造影では、動脈期の間に膵頭の腫りゅうに毛細血管の血管性を示しています。 (下)門脈相画像は、門脈枝の変位と上腸間膜静脈と門脈の接合部の包摂を示している。 Mは膵臓の塊を示す。 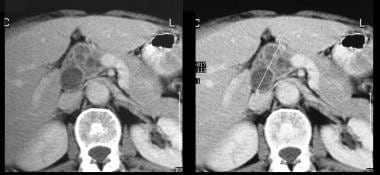 膵管内乳頭粘液腫よう(IPMT)。 膵臓を通るコントラスト増強軸CTスキャンは、膵臓の頭部に多受容体腫瘍を示す。
膵管内乳頭粘液腫よう(IPMT)。 膵臓を通るコントラスト増強軸CTスキャンは、膵臓の頭部に多受容体腫瘍を示す。 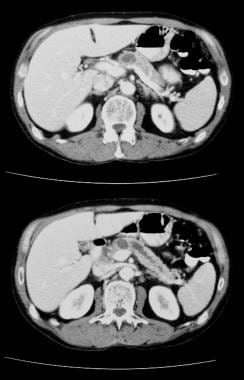 膵管内乳頭粘液腫よう(IPMT)。 膵臓を通る造影c tスキャンでは,すい管の総拡張を示した。 手術時にIPMTを確認した。
膵管内乳頭粘液腫よう(IPMT)。 膵臓を通る造影c tスキャンでは,すい管の総拡張を示した。 手術時にIPMTを確認した。 漿液性嚢胞腺腫
漿液性嚢胞腺腫(小嚢胞性腺腫)(下の画像を参照)は、膵臓の第二の最も一般的な嚢胞性腫瘍である。 しょう液性嚢胞腺腫の臨床像は粘液性嚢胞性すい腫ようの臨床像と類似していた。
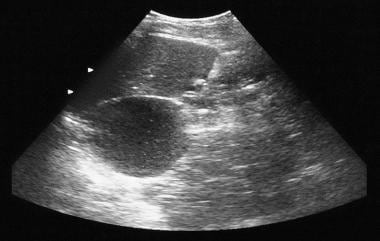 膵微小嚢胞腺腫が示されている。 超音波検査は、膵臓の尾部の領域に嚢胞性の塊を示す。
膵微小嚢胞腺腫が示されている。 超音波検査は、膵臓の尾部の領域に嚢胞性の塊を示す。 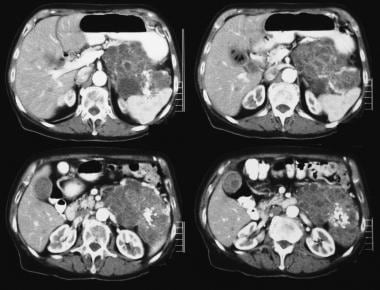 膵微小嚢胞腺腫。 造影c Tでは,すい尾部にサンバースト石灰化を伴う血管過多腫ようを示した。 スイスチーズの強化に注意してください。
膵微小嚢胞腺腫。 造影c Tでは,すい尾部にサンバースト石灰化を伴う血管過多腫ようを示した。 スイスチーズの強化に注意してください。 断面画像の使用が増加しているため、これらの腫瘍の多くは偶発的な無症候性の所見として検出されます。
断面画像では、漿液性嚢胞腺腫は繊細な線維性中隔によって分離された多数の小さな嚢胞として現れ、ハニカムの外観を与える。 嚢胞は透明で水っぽい液体で満たされ、しばしば石灰化する可能性のある中央の星状瘢痕の周りに配置される。 CTスキャンでは、海綿状塊のサンバースト中心石灰化はこの腫瘍の病理学的であるが、この所見は患者のわずか10%で起こる。
超音波内視鏡(EUS)は、CTよりもハニカム構造のより良い解像度を可能にします。 時には、嚢胞は大きく、これらの嚢胞をMcnと区別することを困難にする特徴であり得る。
血管造影で血管過多が示されることがあり、いくつかの腫瘍は腹腔内出血を伴って発生する。
鑑別診断
膵偽嚢胞または膵液採取
急性膵炎の症例の50%にもわたって体液採取が行われています。 偽嚢胞は通常、超音波検査では無響液空間として見られますが、壊死組織または凝塊が含まれている場合は内部エコーを示すことがあります。
嚢胞性新生物ではなく偽嚢胞の診断を示唆する画像所見には、コンピュータ断層撮影(CT)スキャンでの中隔、局在、固形成分、または嚢胞壁石灰化の欠如、血管造影での血管性低下、および内視鏡的逆行性胆管すい管造影(ERCP)での嚢胞と膵管間の通信が含まれる。 ほとんどの偽嚢胞は膵外嚢胞であるが、膵嚢胞性新生物は膵内嚢胞である。
膵膿瘍
膵膿瘍は、通常、偽嚢胞の感染に二次的ですが、まれに、腎または結腸感染からの直接の広がりの結果として発生する可能性があります。 典型的には、膵臓膿瘍は、急性膵炎のエピソードの2-4週間後に起こる。
画像では、これらの膿瘍は偽嚢胞に似て見えることがあります。 一般的に、外観は年齢に依存します。 急性期では,変化は微妙であり,すい輪郭およびすい周囲血管および他の軟部組織空間の抹消に関連する正常なすい輪郭の喪失のみである。 これらの変化は、重度の急性膵炎に見られるものと区別できない可能性があります。 亜急性および慢性の段階では、中心壊死が起こると、通常、無響性または複雑な嚢胞性塊が見られる。 膿瘍の従属部分に破片レベルが観察されることがある。 亜急性期または慢性期では、ガスが膿瘍内に存在する場合を除いて、透過性は通常良好である。 ガスの存在下では、膿瘍はエコー原性になり、影を落とすことがある。
亜急性および慢性膵膿瘍の壁には様々な特徴があります。 壁は厚く、不規則で、明確に定義されていてもよく、または膿瘍に定義可能な壁が全くないかもしれません。 超音波所見は非特異的であるが,適切な臨床設定では,経皮吸引またはCTによって膿ようの診断が示唆され,確認されることがある。
寄生性嚢胞
膵臓のエキノコッカス肉芽腫嚢胞および多発性嚢胞が記載されているが、膵臓の関与は非常にまれである。 E.肉芽腫嚢胞は、単房性、多房性、または複雑な嚢胞性であり得る。
画像化だけでは、これらの嚢胞性腫瘤および他の嚢胞性腫瘤の分化は困難である。 血清学的検査は、適切な臨床設定において有用であり得る。 E.multilocularis嚢胞はエコー原性浸潤パターンを示した。 このようなパターンが見られるとき、この診断は風土病地域で楽しまれるべきである。
固形および乳頭上皮膵臓腫瘍
膵臓の固形および乳頭上皮新生物は、固形または嚢胞性であり得る。 これらは、しばしばムチン分泌腫瘍または非機能性腺腫と誤解されるまれな腫瘍である。
固形および乳頭上皮膵臓腫瘍は、ほとんどの場合、膵臓尾部に位置する。 それらは、出血および壊死の領域を有する大きく、十分にカプセル化された塊である。 超音波検査では、それらは嚢胞性壊死中心およびジストロフィー石灰化を伴う不均一で円形の固体塊として現れ、陰影を生じる可能性がある。
Dysontogenic嚢胞
Dysontogenic嚢胞は、しばしば腎嚢胞、小脳血管腫、および脳細胞に関連する過誤腫性嚢胞である。 イメージングは、桑の構成を持つ大規模な、薄い壁の嚢胞を明らかにする。
偽動脈瘤
偽動脈瘤は通常、真に膵内ではなく、膵嚢胞と混同される可能性があります。 これらの動脈瘤は、患者の3.5-10%における膵炎の合併症である。 Doppler超音波検査では偽動脈りゅう内で乱流動脈流を示すが,カラーフロードップラー超音波検査では無響塊内で双方向の流れと旋回を示す。 ドップラーイメージングは、偽動脈瘤を供給する動脈の暫定的な同定を可能にすることができる。
後腹膜神経線維腫または神経鞘腫
これらの腫瘍は、散発的な内部エコーを伴う高エコーまたは低エコー/嚢胞性病変である可能性があります。 これは嚢胞性の退化および出血が起こったより大きい腫瘍の共通の特徴です。 腫瘍は後腹膜であるが、膵臓腫瘤を模倣する可能性がある。
膵臓肉腫
膵臓肉腫は、膵臓の間葉系支持構造のまれな腫瘍である。 それは比較的sonolucent固まりで、流動コレクションかpseudocystと誤解されるかもしれません。 Sonographic結果は正常であるかもしれませんまたはsonogramsは周囲のティッシュと比較されて比較的sonolucentである後腹膜の固まりを示すかもしれません。 したがって、この病変は嚢胞性膵臓腫りゅうと混同される可能性がある。
膵リンパ腫
原発性膵リンパ腫はまれである。 臨床的な提示は膵臓癌のそれとは異なりません。 超音波検査は、均質な、sonolucent、または複雑な塊を明らかにすることができます。 これらの固まりは通常エコー貧乏人で、嚢胞性の損害をまねるかもしれません。 すいリンパ腫の予後は良好であるため,癌との鑑別が重要である。 超音波所見,CT所見および血管造影所見の相関は,正しい診断をもたらす可能性がある。 ただし、疑いがあれば、超音波検査導かれたバイオプシーは固まりの本当の性質を明らかにするかもしれません。
膵腺房細胞癌
膵細胞癌(PACCs)は、膵外分泌腫瘍の約1%を構成しています。 PACCは腺房分化の証拠を有する上皮新生物である。 腺房細胞癌の患者は管型腺癌の患者よりも予後が良好であるが,すい内分泌腫ようの患者よりも予後が悪い。 CTでは、PACCは、不十分に定義された密な塊としてを含む、さまざまな方法で記載されています;中心壊死を伴う明確に定義された塊として; そして、厚い血管壁に囲まれた嚢胞性の塊として。
優先検査
mriは、嚢胞性膵臓腫瘍の診断に適した技術です。 MRIは、通常、偽嚢胞と嚢胞性新生物の区別に有用である。 磁気共鳴胆管すい管造影(MRCP)は胆管およびすい管の解剖学的構造を非侵襲的に描写することができ,管内腫ようの診断に役立つ。
超音波検査は、一般的に上腹部症状を有する患者における最初の技術である。 これは、嚢胞性膵臓腫瘤の診断のための優れたモダリティである。 超音波検査はまた、吸引および生検などのガイド付き介入の機会を提供する。 ドップラー超音波検査は膵臓の腫瘍と関連付けられるhypervascular腫瘍および管の血栓症/閉塞の評価の加えられた利点を提供します。 エコー増強パワードップラー超音波検査は,すい腫ようの鑑別診断において高い感度と特異性を有する。
曖昧な症例または悪性腫瘍が非常に疑われる症例では、EUS-FNAは、様々な腫瘍マーカーの分析のための細胞学的サンプルおよび嚢胞性液の取得を可能にす
場合によっては、嚢胞性腫瘤の完全な評価にもかかわらず、嚢胞のタイプが不確定なままであることがあります。 高価で侵襲的であるが,腹腔鏡超音波検査,嚢胞壁の生検,および嚢胞吸引液の分析はすい嚢胞病変の鑑別診断に有意に寄与している。
CTは腫瘍石灰化を示し、局所および遠隔metastasesの検出に優れたモダリティです。 CTやMRIではムチン含量をすい液と区別することはできないが,嚢胞性病変と拡張したMPDとの間のコミュニケーションや隆起した開口部を有する隆起した乳頭がIPMTの特徴である。 粘液性腫瘍の内部構造は、病変内の石灰化(MRIが明らかにする能力が限られている)を除いて、CTスキャンと同様に、少なくともMRIスキャンでも表示されます。
スパイラルおよび/またはマルチセクションCTは、優れた空間分解能と解剖学的詳細を提供し、膵臓をイメージングするための優れた技術です。 薄い視準および幹線および静脈段階およびmultiplanarおよび/または3次元の(3D)再建によって、管の解剖学の優秀な細部は描写されます;ほとんどの中心は
単純なx線写真は、多くの場合、膵臓石灰化を探すために得られます。 上部のGIのバリウムの調査は上腹部の苦痛の文脈で行われるかもしれません。 膵臓腫瘍では、バリウム検査は胃および十二指腸の外因性変位を示す可能性がある。
技術の限界
MRIは普遍的に利用可能ではなく、高価であり、閉所恐怖症の患者にとって問題を提起する。 嚢胞型または付随する悪性腫瘍を診断するために画像を使用する場合、ACGガイドラインは注意を推奨し、嚢胞型の診断におけるMRIまたはMRCPの精度は40-50%であり、良性腫瘍対悪性腫瘍の決定において55-76%である。
内臓ガス、患者の習慣、および操作者の依存性は、超音波検査の値を制限する。 腹腔鏡下超音波検査は侵襲的である。 EUSイメージングは良性と悪性Ipmnを確実に区別することができず,悪性の可能性が高い粘液性病変のイメージング特徴が臨床管理に影響を与えるのに十分 外科組織学が参照標準として使用されるとき、EUSイメージ投射の診断正確さは40から96%まで及ぶ。 単一の前向き研究は、感度(56%)と非粘液嚢胞から粘液嚢胞(粘液嚢胞新生物とIPMNs)を区別するためだけでEUS形態の特異性(45%)が悪い全体的な精度(51%)で、その結果、低
単純x線写真および上部消化管バリウム検査は非特異的であり、様々な病理において同様の所見が見られる可能性がある。 CTは重要な電離放射線の重荷を運び、anaphylaxisおよびnephrotoxicityの危険のヨウ素処理された対照材料を使用する。
超音波検査、CT、MRIなどの断面研究では、腫瘍が転移または隣接臓器に浸潤していない限り、粘液性嚢胞腺腫と嚢胞腺癌を区別することはできません。 血管造影は非特異的で侵襲的である。 それはまたアナフィラキシーおよびnephrotoxicityの危険のヨウ素処理された造影剤を、要求します。
フォローアップ画像
ACGガイドラインでは、ipmnsまたはMCNsと推定される無症候性嚢胞を外科的に適合させるために、嚢胞サーベイランスを提供することが推奨されている。 すべての外科的に切除されたIpmnは術後のサーベイランスを必要とするが、膵臓癌のないMcnを切除することはできません。 MRCPは監視のための好まれた様相である;MRIスキャンが禁忌とされるときEUSはまた第一次監視用具であるかもしれない。 さらなる評価のためのサーベイランスまたは紹介の増加を保証する関連機能がない場合、嚢胞サイズは推定IPMNsおよびMcnのサーベイランス間隔をガイドする。
ガイドライン
膵嚢胞の診断と管理のためのガイドラインは、以下の組織によって公開されています:
-
アメリカ消化器大学(ACG)
-
膵臓の嚢胞性腫瘍に関する欧州研究グループ
-
アメリカ放射線大学(ACR)
2018年のACGガイドラインでは、非侵襲性、放射線の欠如、および主膵管と嚢胞(側枝Ipmnの特徴である)との間の通信を評価する精度が高いため、磁気共鳴画像法(MRI)または磁気共鳴胆管膵すい管造影(MRCP)を推奨しています。 Mriが禁忌であれば,すいプロトコールc tまたは超音波内視鏡(EUS)は”優れた選択肢”とみなされた。 EUS細針吸引(FNA)および嚢胞液分析は,診断が不明であり,結果が管理を変える可能性がある嚢胞において考慮すべきである。
嚢胞液の分析CEAは、IPMNsおよびMCNsを他の嚢胞型と区別すると考えられるが、高悪性度異形成または膵臓癌を有するIPMNsおよびMCNsを同定するために使用することはできない。 以下のいずれかの特徴を有するIPMNsまたはMCNsは、FNAの有無にかかわらずEUSを受ける必要があり、および/またはさらなる評価のために学際的なグループに:
-
以下の症状または徴候のいずれか:嚢胞に続発する黄疸、嚢胞に続発する急性膵炎、有意に上昇した血清CA19-9
-
次の画像所見のいずれか: 嚢胞内または膵実質内の壁画結節または固体成分の存在、>5mmの主膵管の拡張、主管IPMNまたは閉塞病変に関する膵管の焦点拡張、または直径≤3cmのムチ
-
細胞診における高悪性度異形成または膵臓癌の存在
また、2018年の欧州ガイドラインでは、膵臓嚢胞性新生物(PCN)の診断のための好ましい方法としてMRIを推奨しています。 石灰化の同定が重要な場合,腫ようの病期分類,術後再発性疾患の診断には,マルチモーダルイメージングを考慮する必要がある。 しかし、精度は、PCNの特定のタイプを識別するため、非腫瘍性または非上皮嚢胞から小さなPCNを区別するため、または管システムへの接続のために比較的低 CTは、以下の臨床状況で考慮する必要があります :
-
実質の、壁画または中央石灰化の検出のため、そして特に膵臓の嚢胞性の新生物から慢性の膵臓炎と関連付けられるpseudocystsを区別する場合
-
悪性腫瘍または付随する膵臓癌の疑いがある場合であり、血管の関与、腹膜疾患、または転移性疾患の評価が必要な場合。
-
膵臓癌の術後再発の疑いがある場合。
欧州のガイドラインでは、外科的切除のために考慮すべき特徴を有するPCNを同定するためにEUSが有用であることが見出されている。 MRIやCTと同様に、EUSはPCNの正確なタイプを識別するための精度が低いです。 EUS-FNAは、CTまたはMRI所見が不明な場合に、粘液性PCN対非粘液性PCN、ならびに悪性PCN対良性PCNを区別するための診断精度を向上させます。 EUS-FNAの使用に関する追加の推奨事項には、次のものが含まれます:
-
EUS-FNAは結果が臨床管理を変えると期待されるときだけ行われるべきです
-
診断が横断面イメージ投射によって既に確立されるか、または外科のための明確な徴候があるところにeus-FNAは行われるべきではないです
-
PCNにおけるEUS-FNAの相対禁忌は、嚢胞とトランスデューサとの間の>10mmの距離、出血障害による出血のリスクが高い、または二重抗血小板薬の使用である