はじめに
5型ホスホジエステラーゼ(PDE5)の酵素作用は、血管拡張剤一酸化窒素(NO)の下流メディエーターであるcGMPの不活性化の主要なメカニズムである(Lugnier、2006)。
勃起不全(ED)の過程で、内皮海綿体血管からのNOの産生障害は、cGMP半減期を延長し、残存血管拡張機能を増強するために、PDE5阻害剤(Pde5I)の使用によっ PDE5上の阻害活性を有するいくつかの分子は、その後、効果の異なる発症と持続時間を示す、市場に投影され、リリースされています。 現在、Pde5Iは、EDの治療に使用される第一選択薬である(Mehrotra e t a l., 2007).
非選択ED患者の80%近くで有効性が認められているにもかかわらず(Eardley et al. ら、2 0 1 0;Hatzimouratidis e t a l. ら、2 0 1 0;Porst e t a l.、2013)、Pde5Iによる治療からの顕著な脱落が最近報告されている。 定量的には、1ヶ月あたり4%の平均中止率が報告されており、年間ベースで50%の症例で治療の全体的な放棄が報告されている(Carvalheira et al. ら、2 0 1 2;Corona e t a l., 2016). 治療の放棄を正当化するために患者によって与えられた主な理由の中で、有効性および副作用の欠如が最も一般的であると呼ばれる(Corona et al., 2016). 頭痛、紅潮、消化不良などのPDE5阻害に厳密に関連するものと、血管拡張および頻脈(PDE1)、視覚障害(PDE6)、および腰痛(PDE1 1)などの他のPDE上の薬物の残留阻害活性に関連するものである(Bischoff,2 0 0 4;Gupta e t a l., 2005). 副作用の発生は、血清レベルおよび薬物への時間暴露の両方で増加するので(Gupta et al. ら,2 0 0 5;Taylor e t a l. 薬物の安全性/有効性プロファイルは、新規薬物製剤の設計により薬物動態学的アプローチにより代替的に改善することができる(Mehrotra e t a l.,2 0 0 9)。, 2007). このアプローチはVardenafilの場合にはPde5Iに首尾よく適用されました。 実際、この分子は比較的低い生物学的利用能に苦しんでいる(≧15%、薬物評価研究センター、2003)。 フィルムコーティング錠剤(FCT)と比較して、古典的なos投与のための元の製剤は、バルデナフィルのためのoro-dispersible錠剤(ODT)の製剤は、舌下吸収を好むことによっ, 2011).
シルデナフィル(Sild)は、EDの治療のために承認された最初の選択的PDE5阻害剤であった(Boolell et al., 1996). これは、比較的親油性分子であり、経口投与後、ピーク血漿濃度は、0.5から2hまで変化する時間内に達成される。Sildは、主に広範な腸および初回通過代謝に起因して、比較的低い経口生物学的利用能(38-41%)を示す(Gupta et al., 2005). 市場での長い存在にもかかわらず、薬物の新規製剤の開発は、新しい製剤のイタリア市場での最近のリリースまで、不十分に追求してきた:オロ分散性フ 実際に、ODFは、fctの生物学的に同等な形態として承認された(Leoni e t a l., 2013). しかしながら、口腔内崩壊製剤は、経粘膜、特に舌下吸収を支持するのに適した系を表すことができる(KathpaliaおよびGupte、2 0 1 3)。
本研究では、odfまたはODTのいずれかの舌下投与に関連するSild薬物動態を、os製剤ごとの元のFCTと比較して評価しました。 この目的のために、我々は、薬物の経粘膜吸収を評価するために特別に開発されたin vitroシステムによる異なるSild製剤の放出/透過プロファイルを調べた。 さらに,ED患者におけるperosfctおよび舌下ODTおよびODFの投与後のSild薬物動態の血清プロファイルを定量した。<2 5 2 7><1 4 8 7>材料および方法<6 9 8 2><2 4 6 6>化学物質および薬物製剤<4 6 0 8><5 1 1 1>Hank’s balance salts solution pH7. 市場で入手可能な代替生物学的同等性製品の使用に起因する交絡結果を避けるために、以下の製品が使用されました: Viagra(登録商標)FCT(Pfizer、イタリア、ミラノ)、Viagra ORO(登録商標)ODT(Pfizer)、およびRabestrom(登録商標)ODF(Ibsa、Lodi、イタリア)。 薬物は、外来での評価中に患者に処方され、私的使用のために処方された。 In vitro試験およびin vivoでの薬物動態の評価(下記参照)のために、薬物は、地元の薬局施設で研究に関与する人員によって特に購入され、その後、最適な条件
脱凝集試験
In vitro脱凝集試験は、錠剤崩壊試験機(Sotax DT2、補足図S1A)を用いて、37±0.5℃で水を浸漬液として用い、欧州薬局方(2016)に従って行われた。 完全崩壊は、試験装置のスクリーン上に残っているか、またはディスクの下面に付着しているユニットの残留物が触知可能にしっかりしたコアを有 テストは三重で行われ、結果は平均値±標準偏差として報告されました。
溶出試験
In vitro薬物溶出試験は、欧州薬局方に従って実施した。 溶解試験は、パドル装置、パドル速度50rpmを使用して実施し、溶解培地体積(900ml、37±0.5℃)としてHBSS pH7.4を使用した。
放出試験中、溶解培地サンプル2ml、at0, 2, 4, 6, 10, 20, 30, そして40分、除去し、0.45μ mセルロースエステルフィルターを通して濾過し、したがって希釈した。 続いて、高速液体クロマトグラフィー(HPLC)-UVによりSild定量を行った。 除去された容積を毎回新鮮な培地と交換した。 テストは三重で行われ、結果は平均値±標準偏差として報告されました。 データは、製剤の薬物含有量について正規化した。
経粘膜透過試験
Sildの経粘膜透過プロファイルは、Delvadiaらによると、特定のデバイスを使用してin vitroで評価しました。 (2012年) 簡単に言えば、デバイスは、使い捨てセルロース–酢酸膜(細孔0.45μ m)によって分離されたドナー–レシーバ室によって特色垂直拡散システムで構成されていた。 ドナー細胞は1.5mlのHBSSを含んでいたが、レシーバチャンバーはチューブとリザーバの容量を含む30mlの閉じた再循環回路の一部であった。 サンプリングは、の時間間隔で受信機室リザーバから行われました0, 5, 10, 20, 30, そして40分および同等の容積の新しいHBSSによって取り替えられて。 試料を、薬物含有量についてHPLC−UVによって分析した(Fej Β s e t a l., 2014). 純粋なクエン酸塩について観察された最高透過Sild濃度についてデータを正規化した。 テストは三重で行われ、結果は平均値±標準偏差として報告されました。
ボランティア心因性ED患者に対する薬物動態研究
この研究は、パドヴァ大学病院倫理委員会(プロトコル番号3982/AO/16および連続修正)の承認を得て、ヘルシンキ宣言に従って、2017年から9月の間に、アンドロロジーと生殖医学のユニット(イタリア、パドヴァ大学病院)で実施された。 交絡の結果を避けるために、心因性EDを有する被験者は、有機的障害の発生が低いことがEDに関連するため登録された(Ludwig and Phillips、2014)。
サンプルサイズは、少なくとも0.5の効果サイズを達成するために計算され、統計的検出力は0.8、有意水準は0.05の三つのグループ比較のために(検出力計算–one-way independent ANOVAを参照)。
20人の患者(平均年齢31.4±5.7歳)は、署名されたインフォームドコンセントのリリースによって連続して登録されました。 患者は前の6か月または多くの間に満足な性交のための建設を得、維持する一貫した無力を報告する外来患者の評価に出席しました。 その後の臨床評価は、糖尿病、高血圧、神経学的障害、および抗うつ薬の使用などのEDに関連する疾患の不在を確認するために、すべての患者において行 心因性EDの診断は、国際勃起機能指数-15(IIEF-15)アンケートの投与における指数スコア<26の達成によって確認された(Lotti et al. ら、2 0 1 6)、および前述のように2泊連続して、Rigiscan Plus Rigidity Assessment System(Dacomed、United States)を介した夜間陰茎腫大および剛性モニタリングによって評価された夜間自発勃起の維持(munozら、2 0 1 6) ら、1 9 9 3;Caretta e t a l., 2005). 除外基準は、悪性腫瘍の診断、異常なホルモン血漿レベル(それぞれ、黄体形成ホルモン>8UI/l、総テストステロン<10.4nmol/l、チロトロピン>4.5mUI/l、プロラクチン>20ng/ml)、および大動脈幹上での内膜-培地厚の増加(>0。3mm)、および/または海綿動脈(<2 5 0 6>0., 2005, 2009).
患者は、単回投与、三方クロスオーバーのオープンラベル研究を遵守することに同意した。 薬物投与スキームは、図1に報告されています。 Sildの投与量は、心因性EDの治療に関する以前の報告と一致して、50mgとして選択された(Banner and Anderson、2007)。 患者は、研究の過程の前および中に1週間、薬物またはアルコールを服用しないように要求された。 さらに、薬物投与の日中、患者はまた、試験の少なくとも2時間前に非脂肪の朝食(牛乳または他の脂肪のない食品)を食べるように要求された。 参照製剤と考えられるFCTは、経口錠剤を一杯の水で嚥下することによって、osごとに古典的に投与された。 ODTおよびODFについて、患者は、水を仮定せずに処方物を舌の下に1 5分間保持し、その後嚥下するように指示された。 静脈血試料を、標準管(Vacutainer,B d Biosciences,Milan,Italy)中で採取した。0, 5, 10, 15, 30, 60, 90, 120, そして薬物投与の後の240分。 滅菌生理食塩水の連続注入による補償を行った。 投与後、被験者は採血を完了するまで収容された。 追加の血液回収は、完全な薬物クリアランスを確認するために、制御理由のために投与から24時間で行われた。 洗浄期間として、1回の投与と次の投与との間に7日間を許容した。 採血後、血漿を直ちに単離し、使用するまで-80℃で保存した。
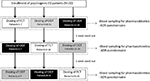
図1. 心因性勃起不全(ED)を有する20人の患者における薬物動態パラメータの評価のための投薬スキームおよび評価は、3つのグループ(それぞれ、患者1-7;患者8-14; 患者の各グループは、osフィルム被覆錠剤(FCT)、舌下oro−分散性錠剤(ODT)、または舌下oro−分散性フィルム(ODF)ごとに、各投与から少なくとも1週間の洗浄を受けた。 すべての製剤には50mgのシルデナフィル(Sild)が含まれていました。
収容中に、患者はまた、Agenzia Italiana del Farmaco(AIFA1)のADR報告フォームから適応された特別に考案された形で有害薬物反応(ADR)を記録するよう要求されました。 アンケートの翻訳版は補足資料として入手可能です(補足データシートS1を参照)。 患者は、有害反応の種類、全体的な強度(主観的評価尺度では1、非常に弱い、5、非常に強い)、発症時間、および全体的な持続時間を指定するように求められた。
ヒト血清中のシルデナフィルの定量
Sildの血清レベルの定量のために、血清サンプル400μ lに内部標準(IS)ベンザニリド(5μ g/ml)を補充したメタノール500μ lを加えた。 続いて、この混合物に5mlの酢酸エチルを加え、試料をボルテックスして液液抽出を行い、遠心分離により二相を分離した。 次いで、有機部分を4 0℃の真空遠心分離機下で蒸発させた。 得られた残渣を200μ lのメタノールで再溶解し、最終的に高速液体クロマトグラフィー-タンデム質量分析(HPLC-MS/MS)分析に使用した。
高速液体クロマトグラフィー-MS/MS分析では、Agilent-Varian1260システムと三重四重検出器Agilent-Varian320MSを使用しました。 正の検出モードは、isの遷移198>105Daに適用され、毛細管張力40Vと衝突エネルギー16Vの間、475>100Da sildの毛細管張力40Vと衝突エネルギー22.5Vのそれぞれ。 実際の試料中のISおよびSildの代表的なクロマトグラムは、補足図S2Bに報告されています。
統計分析
薬物動態パラメータ(PK)、例えば最大血清濃度(Cmax)、最大血清濃度までの時間(tmax)、および異なる時点での曲線下面積(AUC)は、GraphPadソフトウェア(La Jolla、CA、United States)を使 0for Windows(SPSS,Chicago,IL,United States)を用いてデータの統計分析を行った。 Kolmogorov-Smirnov検定は、分布の正規性をチェックするために使用されました。 正規分布を示さない変数を対数変換した。 患者、PKs、およびin vitro実験からのデータのベースライン特性は、多重比較のためのBonferroni-Holm補正と対になっていないStudentのtテストと比較しました。 反復測定A NOVAを実施して、薬物放出およびSild血清濃度の差を試験した。 Leveneの検定を使用して、グループ間の分散の均質性を検定しました。 分散の同質性の仮定に違反した場合には,Welch検定を行い,それぞれのP値を報告した。 ADRの割合はσ2厳密なテストと比較されました。 P値<0.05は統計的に有意であると考えられた。
結果
異なる薬物製剤からのシルデナフィルの放出/透過のIn Vitro分析
三つの薬物製剤からのシルデナフィルの放出/透過の動態は、以前はin vitroで調査されていた(図2)。 FCT、ODT、およびODFの分解を完了するまでの時間を、欧州薬局方(2 0 1 6;図2A)に記載された標準試験によって評価した。 ODFは、FCTおよびODTの両方と比較して、脱凝集までの最も高い時間を示した(それぞれ、P=0.
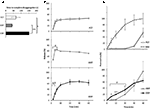
図2. 50mgのSildを含むFct、Odt、およびodfsのバイオ技術特性のin vitro評価。 結果は、3つの独立した実験の代表であり、平均値±標準偏差として報告される。 (A)脱凝集試験の結果、製剤の完全な脱凝集までの時間(秒単位)を報告する。 有意性:示された製剤間の≤P<0.05および≤p<0.01。 (B)溶解試験の結果、各製剤によって放出されるSildの量を薬物の投与量の百分率として報告する。 有意性:aP<0.01対FCT;bP<0.001対ODT。 (C)浸透試験の結果(“材料および方法”のセクションに詳述)は、酢酸セルロース膜を透過したSildの量を、純粋なSild粉末50mgによって達成された最高値の百分率として報告している(上部パネルの不連続ライン)。 有意性:≦P<0.05対ODT;≦P<0.01対odt;AP<0.01対fct。
このエビデンスが製剤からの薬物放出に及ぼす影響を評価するために、標準的な溶解試験を実施した(欧州薬局方、2016;図2B)。 参照製剤FCTと比較して、ODTは、試験の開始からわずか2分後であっても最大範囲が達成された薬物のより速い放出を示した(P=0.006対FCT)。 一方、アッセイの最初の4分以内にODFから放出された薬物の割合は、FCTおよびODTの両方と比較して低かった(それぞれ、P=0.004およびP<0.001)。 特に、ODFは、FCTと比較して薬物のより進行性の放出を示し、試験の開始から2 0分後に最大の程度を達成した。
これに基づいて、各製剤からのSildの経粘膜透過を、特別に開発されたデバイスによって評価した(図2C)。 参照目的のために、Sildの50mgに相当する重量で使用される純粋なsildクエン酸塩は、経粘膜透過のために評価され、二つのチャンバ間の自由で速い拡散を示 ほぼ反対のプロファイルは、テストの開始から30分まで無視できる透過を示す、FCTのために観察されました。 ODTとODFの透過プロファイルは前の二つの条件と比較して中間的な挙動を示した。 アッセイの最初の20分以内に、ODFは、ODTと比較して有意に高い浸透範囲を示した(それぞれ、5分でP=0.033、10分でP=0.003、および20分でP=0.041)。 ドナー室で完全に脱凝集したFCTおよびODTとは異なり、odfの残留ソフトゼリー塊は、アッセイの終わりにも酢酸セルロース膜上に持続した(補足図S2C)。
シルデナフィルの差動薬物動態
心因性DEの影響を受けた二十人の男性被験者は、代わりにFCT、ODT、またはODFを受け、一週間の洗浄によって分離された。 「材料および方法」の項に詳述されているように、FCTを古典的に飲み込んで、古典的なper os投与を可能にし、一方、ODTおよびODFを舌下に1 5分間維持して舌下経路 患者の臨床的特徴を表1に報告する。 3つの投与条件に対応するSildの血清レベルを図3に報告する。 かなりの変動は、三つの製剤の薬物血清プロファイルを特色にした。 FCTと比較して,ODTはSild血清レベルの明らかな早期増加を示したが,この傾向は統計的に有意ではなかった。 一方、投与から120分および240分でのSildレベルのより速い減衰が、ODT製剤について観察された(それぞれ、P=0.044およびP=0.024対FCT)。
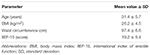
表1. 研究参加者の臨床的特徴(N=20)。
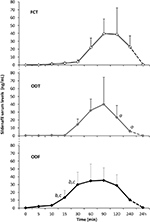
図3. 心因性EDの影響を受けた2 0人の患者において、「材料および方法」の節に詳述されているように、代わりにosあたりのFCT、または舌下ODT、または舌下ODFのいず「データは、平均値±標準偏差の有意性として報告される:aP<0.05対FCT;bP<0.01対FCT;cP<0.05対ODT。
ODF製剤の薬物血清プロファイルは、投与から15分および30分で、それぞれFCT(P=0.001およびP=0.003)およびODT(p=0.048およびP=0.041)の両方と比較して、Sildレベ In vitroでの遅い脱凝集時間(図2B)と一致して、in vivoでのODF平均濃度–時間曲線は、FCTおよびODTのものよりも滑らかであった(図3)。
Sild血清レベルの分析から得られた三つの製剤の薬物動態パラメータを表2に要約する。 Cmax、tmax、およびAUC0-240分に関して3つの製剤間で有意差は観察されなかったにもかかわらず、ODFはCmaxの最低値(38.2±23.7ng/ml)および最短tmax(70.0±24.5分)を示 特に、ODFは、FCTおよびODTの両方と比較して、AUC0〜6 0分の有意に高い値を示した(それぞれ、P=0.ODFの投与から舌下経路を経て最初の1時間以内に、Sildの相対的生物学的利用能が増加した。

表2. シルデナフィル製剤の薬物動態パラメータ。
有害薬物反応
研究参加者が経験したADRの種類と特徴に関する自己投与アンケートから得られた結果を表3にまとめた。 Sildについて報告された既知のADRの中で(Taylor e t a l.、2009)、最も頻繁に記録された頭痛、潮紅、および鼻の鬱血であった。 ある患者は、FCTの投与後に低悪性度の筋肉痛(主観的評価スケールでグレード1)を報告した。 患者のいずれも、視力の変化、頻脈、衰弱、または聴力の変化を報告しなかった。

表3. 研究参加者によって記録された有害薬物反応(N=20)。
参照製剤としてのFCTと比較して、ODTはADRの有病率が変化していないことを示した。 しかし、フラッシング強度の個人的な認識は有意に低かった(P=0.031)。 一方、ODFはFCTと比較して頭痛の有病率の低下を示した(P=0.043)。 さらに、紅潮および鼻づまりの持続時間および強度は、FCT(それぞれ、P=0.011およびP=0.015)およびODT(それぞれ、P=0.026およびP=0.037)の両方と比較して低いレベ
ディスカッション
本研究では、Sild投与の舌下経路が早期薬物の生物学的利用能の向上と忍容性プロファイルの改善と関連しているという証拠 この証拠は、Sild製剤が脱凝集するのに長い時間が、有意に経粘膜吸収を支持し、in vivoの証拠によって特色にされていることを示す、in vitroの調査の両方に
ホスホジエステラーゼ阻害剤はEDの治療のための最初の選択の治療上の選択である;但し、患者が経験する副作用は療法の中断の最も一般的な理由, 2016). 新規な薬物製剤の設計を通じた薬物動態の改変は、薬物自体の安全性/有効性プロファイルを改善するための魅力的な戦略を表し得る(Mehrotra e t a l., 2007). この点に関して、いくつかの欧州諸国におけるクエン酸塩Sildに関する特許の2013有効期限は、Sildの新しい製剤の数をリリースする機会を可能にしました。 今日市場で入手可能なSild製剤の大部分は、実際には元のFCTの生物学的に同等な形態として承認されていることに留意すべきである(Leoni e t a l., 2013). 興味深いことに、水による嚥下を必要とせずに患者の口腔内での迅速な脱凝集によって特徴づけられる口腔内崩壊製剤が開発されている(Goel et al., 2008). これらの新規製剤は、小児、老人患者、および嚥下障害患者などの従来の固形投与量を嚥下することが困難な患者の集団において、改善されたコンプライアンスを見出している。 さらに、より高い経口薬物の利用可能性を提供することによって、口腔内崩壊製剤は、経粘膜、特に舌下吸収を支持する価値のある系を表し得る(Kathpalia and Gupte、2013)。 特にイタリアでは、Sildの2つの口腔内崩壊製剤が薬局施設で正式に入手可能です:ODTsとODFs。
本研究では、薬物の利用可能な二つの口腔内崩壊製剤の舌下投与を通じてSildの経粘膜吸収を支持することから、可能な薬物動態変動、およびADRの対応 結果をSildの元の製剤,すなわちFctと比較した。 興味深いことに、in vitroとin vitroの両方で、生物技術的特性と異なる製剤のPKsとの間に厳密な相関があることがわかりました。 特に、同等の薬物投与量(50mg)と溶解試験における薬物放出速度がわずかに低下したにもかかわらず、ODFは、一方では脱凝集までの時間が長く、経粘膜モデル 我々はその後、舌下シルド吸収が長期の薬物-粘膜接触によって支持されていることを仮定するかもしれません。 実際、この現象は、一般的に、製剤と口腔粘膜との間の長期間の接触を保証するために、粘膜接着性ポリマーの使用が推奨される経口経粘膜薬物(Lam et al. ら、2 0 1 4)、特に、低水溶性の影響を受けるSildのようなそれらの薬物から(Zayed e t a l. ら、2 0 1 2;Sun e t a l., 2014). これらの予備的結果はまた、元の製剤と比較して、このクラスの薬物に対する臨床的有効性の改善の可能性を示唆している。 これらの側面を明確にするためには、さらなる研究が必要です。
本研究の最も顕著な証拠は、同じ用量で投与されたODTおよびFCTと比較して、ODFの舌下投与のAdrが有意に減少し、患者のコンプライアンスが増加する可 この証拠は、血清レベルおよび薬物自体への曝露時間を増加させることによって薬物副作用の発生率が増加するという原則に照らして解釈するこ ら,2 0 0 5;Taylor e t a l., 2009). 分析される他の公式と比較されるunvaried全体的な生物利用可能性にもかかわらずODFの副lingual管理はcmaxのより低い価値およびより短いtmaxを示し、投薬からの最初の時間以内に生物利用できるSildのかなりより高い割合に終って。 したがって,lingfの舌下投与は,薬物の効率的な吸収とSildの平均低い血清レベルの達成とAdrsの結果として低いリスクを組み合わせていると推測することができる。 しかし、この研究の主な欠点として、サンプルサイズが低いことを認識しています。 この問題を確認するには、より大きなコホートと異なる投与量のさらなる調査が必要です。
結論として、本研究では、Sild ODFの舌下投与は、ジェネレータFctと比較して改変された薬物動態の関与の可能性が高いことにより、薬物忍容性プロファイ ODFはもともとこの目的のために考案されたものではありませんが、これは治療に対する患者の遵守を改善するための魅力的な戦略です。 私たちは、心因性および有機ED患者における臨床的有効性を評価するためのさらなる比較研究を開発しています。
著者の貢献
LDTとCFは研究を調整し、原稿を起草しました。 MDRPは患者を評価し、登録した。 EFはinvitro分析を行った。 SDAは血清分析を行った。 RPは薬物動態比較を行った。 RP、NR、AGは批判的に原稿を改訂し、確定しました。
利益相反声明
著者らは、この研究は利益相反の可能性があると解釈される可能性のある商業的または財政的関係がない場合に行われたと宣言
謝辞
患者カウンセリングのためのアルベルト-バロッソ博士、ジュゼッペ-マッジョーニ博士、ディミトリ-ポルターレ博士、患者管理のためのフラビア-ロザーノ博士とアリス-パサドーレ博士、およびアンドロロジー-生殖医療ユニットのすべてのスタッフに感謝します。
補足資料
この記事の補足資料はオンラインで見つけることができます: https://www.frontiersin.org/articles/10.3389/fphar.2018.00059/full#supplementary-material
図S1|それぞれ脱凝集試験および溶解試験に使用される錠剤崩壊試験機(A)および溶解装置(B)の代表画像。
図S2|(A)シルデナフィル(Sild)の血清レベルの高速液体クロマトグラフィー-タンデム質量分析(HPLC-MS/MS)分析に使用される移動相勾配の詳細。 実際の試料中の内部標準ベンザニリドにおける両Sildの代表的なクロマトグラムと質量スペクトルを報告した(B)。 (C)酢酸セルロース膜を介した経粘膜吸収のin vitro推定に使用されるデバイスにおける透過試験後に持続する残留オロ分散性膜の代表画像(不連続線で強調)。
データシートS1|有害薬物反応アンケート。
脚注
- ^http://www.aifa.gov.it/en/content/reporting-adverse-reaction
Banner,L.L.,And Anderson,R.U.(2007). 心因性勃起不全のための統合されたシルデナフィルおよび認知行動性療法:パイロット研究。 J.セックス。 メッド 4, 1117–1125. ドイ:10.1111/j.1743-6109.2007.00535.x
PubMed要約/CrossRef全文|Google Scholar
Bischoff,E.(2004). PDE阻害の非選択性の効力、選択性、および結果。 Int. J.Impot. レッサーパンダ-サプリメントス… 1、S11-S14。 土井:10.1038/イジール3901208
PubMed要約/CrossRef全文/Google Scholar
Boolell,M.,Allen,M.J.,Ballard,S.A.,Gepi-Attee,S.,Muirhead,G.J.,Naylor,A.M.,et al. (1996). Sildenafil:penile勃起不全の処置のための口頭で活動的なタイプ5循環GMP特定のホスホジエステラーゼの抑制剤。 Int. J.Impot. 8,47-52
PubMed Abstract/Google Scholar
Caretta,N.,Palego,P.,Ferlin,A.,Garolla,A.,Bettella,A.,Selice,R.,et al. (2005). 勃起不全および頸動脈壁の変化の様々な程度の影響を受けた選択された患者における自発的勃起の再開:タダラフィルの役割。 ユーロ ウロール 48, 326–331. 土井:10.1016/j.eururo.2005.01.013
PubMed要約/CrossRef全文/Google Scholar
ることを可能にすることを目的としたものである。 海綿動脈内膜-メディアの厚さ:血管勃起不全の診断における新しいパラメータ。 J.セックス。 メッド 6, 1117–1126. ドイ:10.1111/j.1743-6109.2008.01112.x
PubMed要約/CrossRef全文|Google Scholar
とができるようになることを期待しています。 PDE5による勃起不全の治療における脱落:予測因子に関する研究および中止理由の定性分析。 J.セックス。 メッド 9, 2361–2369. ドイ:10.1111/j.1743-6109.2012.02787.x
PubMed要約/CrossRef全文|Google Scholar
医薬品評価研究センター(2003年)。 NDA021400レビトラ(バルデナフィル塩酸塩)錠: 臨床薬理学/バイオ医薬品レビュー。 ロックビル、Md:健康と人間サービスの部門。 銀のばね、MD:食品医薬品局。
Corona,G.,Rastrelli,G.,Burri,A.,Serra,E.,Gianfrilli,D.,Mannucci,E.,et al. (2016). 第一世代ホスホジエステラーゼ5型阻害剤ドロップアウト:包括的なレビューとメタ分析。 アンドロロジー4,1002-1009. 土井:10.1111/andr.12255
Pubmed要約/CrossRef全文/Google Scholar
デルヴァディア、P.R.、バー、W.H.、およびカーネス、H.T. (2012). A biorelevant in vitro release/permeation system for oral transmucosal dosage forms. Int. J. Pharm. 430, 104–113. doi: 10.1016/j.ijpharm.2012.03.050
PubMed Abstract | CrossRef Full Text | Google Scholar
Eardley, I., Donatucci, C., Corbin, J., El-Meliegy, A., Hatzimouratidis, K., McVary, K., et al. (2010). Pharmacotherapy for erectile dysfunction. J. Sex. Med. 7, 524–540. doi: 10.1111/j.1743-6109.2009.01627.x
PubMed Abstract | CrossRef Full Text | Google Scholar
European Pharmacopoeia (2016). 欧州医薬品品質総局&ヘルスケア(EDQM)、9Th Edn。 ストラスブール:ヨーロッパの評議会。
とができるようになりました。 唯一の参照としてsildenafilを使用してHPLC-UVによる偽造の薬そして食餌療法の補足のPDE-5抑制剤の質的な、定量分析。 J.ファーム バイオメッド アナル… 98, 327–333. doi:10.1016/j.jpba.2014.06.010
PubMed要約/CrossRef全文/Google Scholar
とができるようになりました。 (2008). 口腔内崩壊システム:製剤と技術の革新。 最近のパット。 ドラッグデリブ… フォルムル 2, 258–274. 土井: 10.2174/187221108786241660
CrossRef全文|Google Scholar
ることができる。 勃起不全のためのホスホジエステラーゼ-5阻害剤の臨床薬物動態。 J.Clin. ファーマコール… 45, 987–1003. 土井: 10.1177/0091270005276847
PubMed Abstract|CrossRef全文|Google Scholar
Hatzimouratidis,K.,Amar,E.,Eardley,I.,Giuliano,F. ら,hatzichristou,D.,Montorsi,F.,et a l. (2010). ヨーロッパ泌尿器科協会。 男性の性機能障害の指針:勃起不全および早漏。 ユーロ ウロール 57, 804–814. 土井:10.1016/j.eururo.2010.02.020
Pubmed要約/CrossRef全文/Google Scholar
Hawksworth,D.J.,And Burnett,A.L.(2015). 勃起不全の薬物療法管理。 クリン ファーマコール… Ther。 98, 602–610. doi:10.1002/cpt。261
Pubmed要約/CrossRef全文/Google Scholar
Heinig,R.,Weimann,B. とができるようになりました。 バルデナフィルの新しいorodispersible錠剤製剤の薬物動態:三つの臨床試験の結果。 クリン 麻薬捜査官。 31, 27–41. 土井: 10.2165/11584950-000000000-00000
PubMed Abstract|CrossRef全文|Google Scholar
とができるようになりました。 高速溶解経口薄膜薬物送達システムへの紹介:レビュー。 カー ドラッグデリブ… 10, 667–684. 土井:10.2174/156720181006131125150249
PubMed要約/CrossRef全文/Google Scholar
Lam,J.K.,Xu,Y.,Worsley,A.,And Wong,I.C.(2014). 小児科の使用のための口頭transmucosal薬剤配達。 Adv.Drug Deliv. 73,50-62 doi:10.1016/j.addr.2013.08.011
PubMed要約/CrossRef全文/Google Scholar
レオーニ,L.A.,レイテ,G.S.,ウィチ,R.B.,とロドリゲス,B.(2013). Sildenafil:利点または危険の二十年か。 高齢男性16歳85-91歳 ドイ:10.3109/13685538.2013.801952
PubMed要約/CrossRef全文/Google Scholar
Lotti,F.,Corona,G.,Castellini,G.,Maseroli,E.,Fino,M.G.,Cozzolino,M.,et al. (2016). 精液の質の減損は重大度に従って性機能障害と関連付けられます。 ハム リプロド 31, 2668–2680. doi:10.1093/humrep/dew246
PubMed要約/CrossRef全文/Google Scholar
ることができます。 40歳未満の男性の勃起不全の有機的原因。 ウロール Int. 92, 1–6. 土井:10.1159/000354931
Pubmed要約/CrossRef全文/Google Scholar
Lugnier,C.(2006). サイクリックヌクレオチドホスホジエステラーゼ(PDE)スーパーファミリー:特定の治療薬の開発のための新しいターゲット。 ファーマコール… Ther。 109, 366–398. 土井:10.1016/j.pharmthera.2005.07.003
PubMed要約/CrossRef全文/Google Scholar
とができるようになりました。 ホスホジエステラーゼ-5阻害剤療法における薬物動態および薬力学の役割。 Int. J.Impot. Res.19,253-264. ドイ:10.1038/sj.イジール3901522
PubMed要約/CrossRef全文/Google Scholar
およびMarshall,I.(1 9 9 3)。 陰茎のtumescenceおよび剛性率の測定のRigiscanの性能。 Int. J.Impot. 5号、69-76頁。
Porst,H.,Burnett,A.,Brock,G.,Ghanem,H.,Giuliano,F.,Glina,S.,et al. (2013). 性的医学のためのISSM基準委員会。 勃起不全のsop保守的な(医学的および機械的な)治療。 J.セックス。 メッド 10, 130–171. 土井:10.1111/12023
Pubmed要約/CrossRef全文/Google Scholar
Sun,D.,Wei,X.,Xue,X.,Fang,Z.,Ren,M.,Lou,H.,et al. (2014). D-α-トコフェリルポリエチレングリコール1000コハク酸ナノエマルションに基づくアセチルプエラリンの経口吸収および治療効果を増強した。 Int. J.ナノ医学9、3413-3423。 ドイ:10.2147/日本.S63777
PubMed要約/CrossRef全文|Google Scholar
Taylor,J.,Baldo,O.B.,Storey,A.,Cartledge,J.,And Eardley,I.(2009). ホスホジエステラーゼ5型阻害剤の副作用期間と関連するレベルの違い。 BJU Int. 103, 1392–1395. doi:10.1111/j.1464-410X.2008.08328.x
PubMed要約/CrossRef全文|Google Scholar
とができるようになりました。 肺の幹線高血圧の管理のための直接圧縮された固体分散および凍結乾燥させていたsildenafilのクエン酸塩のsublingualタブレットの生体外および生体内の比較 アクタ-ファーム 62, 411–432. 土井:10.2478/v10007-012-0027-9
PubMed Abstract | CrossRef Full Text | Google Scholar