Reaksjon: Hydrering Av Alkyner
som med alkener,hydrering (tilsetning av vann) til alkyner krever en sterk syre, vanligvis svovelsyre, og er tilrettelagt av kvikksølvsulfat. I motsetning til tilleggene til dobbeltbindinger som gir alkoholprodukter, gir tilsetning av vann til alkyner ketonprodukter (unntatt acetylen som gir acetaldehyd ). Forklaringen på denne avviken ligger i enol-keto tautomerisering, illustrert av følgende ligning. Det opprinnelige produktet fra tilsetning av vann til et alkyn er en enol (en forbindelse som har en hydroksylsubstituent festet til en dobbeltbinding), og dette omarrangeres umiddelbart til den mer stabile keto-tautomeren.
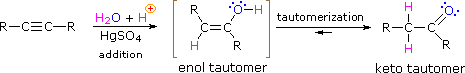
Tautomerer er definert som raskt interkonverterte konstitusjonelle isomerer, vanligvis preget av en annen bindingssted for et labilt hydrogenatom (farget rødt her) og en annerledes plassert dobbeltbinding. Likevekten mellom tautomerer er ikke bare rask under normale forhold, men det favoriserer ofte en av isomerer (aceton, for eksempel, er 99,999% keto tautomer). Selv i slike ensidige likevekter kommer bevis for tilstedeværelsen av den mindre tautomeren fra forbindelsens kjemiske oppførsel. Tautomere likevekter katalyseres av spor av syrer eller baser som vanligvis er tilstede i de fleste kjemiske prøver. De tre eksemplene vist nedenfor illustrerer disse reaksjonene for forskjellige substitusjoner av trippelbindingen. Tautomeriseringstrinnet er angitt med en rød pil. For terminale alkyner følger tilsetningen Av vann Markovnikov-regelen, som i det andre eksemplet nedenfor, og sluttproduktet ia a metylketon(unntatt acetylen, vist i det første eksemplet). For interne alkyner (trippelbindingen er innenfor en lengre kjede ) er tilsetningen av vann ikke regioselektiv. Hvis trippelbindingen ikke er symmetrisk plassert (dvs. Hvis R & R ‘ i den tredje ligningen ikke er den samme ) vil to isomere ketoner bli dannet.
HC≡CH + H2O + HgSO4 & H2SO4 –> –> H3C-CH=O
RC≡CH + H2O + HgSO4 & H2SO4 –> –> RC(=O)ch3
RC≡CR’ + H2O + HgSO4 & H2SO4 –> –> RCH2-C(=O)R’ + RC(=O)-CH2R’
med tilsetning av vann kan alkyner hydreres for å danne enoler som spontant tautomeriserer til ketoner. Reaksjonen katalyseres av kvikksølvioner. Følger Markovnikovs Regel: Terminale alkyner gir metylketoner
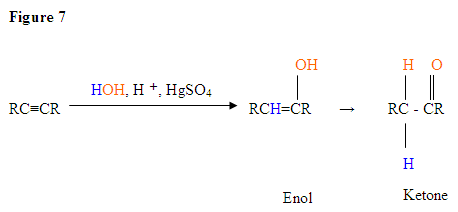
- det første trinnet er en syre / base-reaksjon hvor de π elektronene i trippelbindingen fungerer Som En Lewis-base og angriper protonen og protinerer karbonet med de fleste hydrogen-substituenter.
- det andre trinnet er angrepet av det nukleofile vannmolekylet på den elektrofile karbokasjonen, som skaper en oksoniumion.
- deretter deprotonerer du ved en base, genererer en alkohol kalt en enol, som deretter tautomeriserer til et keton.
- Tautomerisme er et samtidig proton-og dobbeltbindingsskift, som går fra enolformen til keto-isomerformen som vist ovenfor i Figur 7.
la Oss nå se på Noen Hydreringsreaksjoner.
Hydrering Av Terminal Alkyne produserer metylketoner
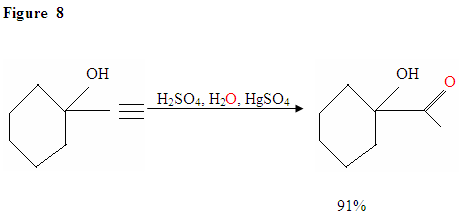
På samme måte som beskrevet i Figur 7 vil de π elektronene angripe en proton, som danner en karbokasjon, som deretter blir angrepet av nukleofile vannmolekyler. Etter deprotinering genererer vi en enol, som deretter tautomeriserer i ketonformen som vises.
Hydrering Av Alkyne
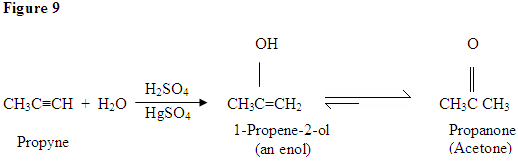
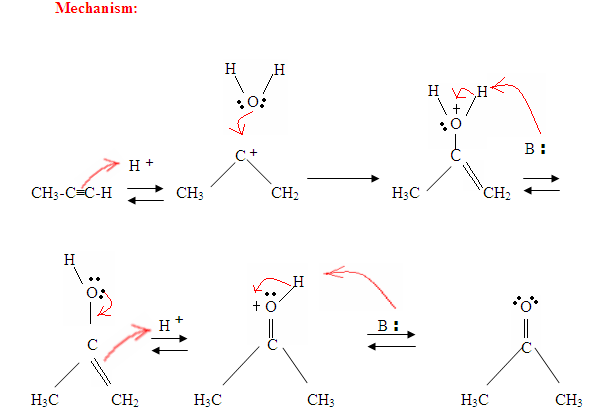
som du kan se her, angriper de π elektronene i trippelbindingen protonen, som danner en kovalent binding på karbonet med de fleste hydrogen-substituenter. Når hydrogenet er bundet, har du en karbokasjon, som blir angrepet av vannmolekylet. Nå har du en positiv ladning på oksygen som resulterer i en base som kommer inn og deprotinerer molekylet. Når deprotinert, har du en enol, som deretter blir tautomerisert.
Tautomerisme vises her når protonet blir angrepet av de dobbeltbindende elektronene som danner en kovalent binding mellom karbonet og hydrogenet på det mindre substituerte karbonet. Elektroner fra Oksygen ender opp med å flytte til karbon, danner en dobbeltbinding med karbon og gir seg en positiv ladning, som deretter blir angrepet av basen. Basen deprotinerer Oksygenet som resulterer i det mer stabile sluttproduktet ved likevekt, som er et keton.
Øvelse \(\PageIndex{1}\)
- Tegn strukturen til produktet som dannes når hvert av stoffene under behandles MED H2O / H2SO4 i nærvær Av HgSO4.
- $ \ ce{\sf{CH3-CH2-C # C-H}}$
-
- Tegn strukturen av ketoformen av forbindelsen vist nedenfor. Hvilken form vil du forvente å være mest stabil?
Svar
Svar:
ketoformen skal være den mest stabile.
Spørsmål
Q9.4.1
Hva alkyne ville du begynne med å få følgende produkter, i en oksidasjonsreaksjon? Husk resonans.

Q9.4.2
Foreslå et reaksjonsskjema for følgende forbindelse som starter fra alkynen og viser nødvendige reagenser og mellomprodukter.

Løsninger
S9.4.1

S9.4.2
