Innledning
Tilstrekkelig tolkning av myokardnekrosemarkører er avgjørende for diagnose, stratifisering og behandling av pasienter med mistanke om akutt koronarsyndrom (ACS). Protokollene på hjertemarkører for akutt myokardinfarkt (AMI) refereres til den tredje universelle definisjonen AV AMI.
dette dokumentet fastslår at hjerte troponin (cTn) heving og senking er grunnleggende for å etablere diagnosen i sammenheng med iskemiske symptomer, elektrokardiografiske endringer eller nylig manifesterende segmentale endringer i en avbildningsstudie.1
Teknologiske fremskritt i bestemmelsen av cTn har forbedret kapasiteten til å oppdage og kvantifisere myokardcelleskader. Kriteriene referert til heving av cTn-verdiene avhenger av testen som brukes og må defineres på grunnlag av presisjonsprofilen til hver test, inkludert den for høy følsomhetstesting.2 eksistensen av forskjellige kommersielle cTn-immunoassays med forskjellige persentil 99 (p99) konsentrasjoner; det faktum at noen laboratorier bruker forskjellige referanser til testresultatene for myokardskade («normal»,» ubestemt «eller» suggestiv»); og den diskriminerende bruken av cTn-testing i store populasjoner med svært forskjellige sannsynligheter for å presentere ACS, har en tendens til å generere forvirring i sammenheng med klinisk ledelse.
det er et betydelig antall pasienter som i fravær AV AMI likevel utviser cTn-konsentrasjoner> p99. Disse pasientene har vanligvis kardiovaskulære risikofaktorer, og sannsynligheten for komplikasjoner hos slike personer er lik den hos pasienter med ACS.3
de siste Europeiske anbefalingene om behandling av pasienter med akutt koronarsyndrom uten st-elevasjon (NSTE-ACS) anbefaler bruk av høysensitiv cTn (hs-cTn) versus konvensjonelle eller fjerde generasjons (4g) troponiner, og vurderer opptil to algoritmer (0h/3h, 0h/1H) for bekreftelse (regel inn) eller utelukkelse (utelukke) AV AMI.4
Hjerte troponiner er ekstremt spesifikke for myokardskade. Men på ingen måte er myokardskade eksklusiv ACS. De kliniske veiledningene understreker derfor at cTn-konsentrasjon må tolkes i forhold til pasientens symptomer. I denne forbindelse økte cTn-konsentrasjoner hos pasienter med sepsis, hypertensive kriser, lungeemboli, etc., er indikativ for myokardskade, men ikke AV AMI, og bør ikke brukes til å indikere spesifikke behandlinger for ACS.5
begrepet «høy følsomhet» bør reserveres for de immunoassays stand til å bestemme p99 med en variasjonskoeffisient (CV) på 6
det er tvil i det vitenskapelige miljøet om bruken av hs-cTn representerer betydelig klinisk forbedring, og om det innebærer flere tester og interconsultations.7 denne studien ble utført for å evaluere diagnostisk ytelse av høy følsomhet troponin t( hs-TnT), avgjøre om det forkorter tiden til diagnose og analysere de kliniske konsekvensene av bruken.
Metode
en prospektiv, longitudinell observasjonsstudie ble utført i sykehusets nødtjenester (HMS) Av Sykehus Clí (Valencia), Sykehus Clí (Má), Sykehus Severo Ochoa (Legané), Sykehus Sant Pau (Barcelona) Og Sykehus Miguel Servet(Zaragoza) (Spania), som involverte pasientene I TUSCA (Troponina Ultrasensible en el SCA) trial8 mellom juni 2009 og April 2010. Studien ble gjennomført i samsvar med Prinsippene I Helsinkideklarasjonen, og ble godkjent av De lokale Etikkomiteene i de deltakende sentrene. Skriftlig informert samtykke ble innhentet fra alle pasienter. Vi inkluderte fortløpende pasienter over 18 år sett i HMS på grunn av brystsmerter som tyder PÅ NSTE-ACS. Pasientinnmelding ble gjort under innledende behandling i HMS, etter vurdering av inklusjons-og eksklusjonskriteriene. Pasientbehandling og anvendt behandling fulgte interne protokoller basert På konsensusguider Fra European Society Of Cardiology, under indikasjoner fra de ansvarlige for pasientene til enhver tid, og med total uavhengighet av deltakelse i studien. Seriell 4g cTn bestemmelser ble gjort for diagnostisering AV ACS, i samsvar med rutinemessig klinisk og immunoassay praksis i hvert senter.
pasientkarakteristikkene ble oppgitt i en saksrapportform og besto av demografiske data, tid som refererte til symptomdebut, tilstedeværelse av risikofaktorer (arteriell hypertensjon, diabetes mellitus, kronisk obstruktiv lungesykdom , hjertesvikt og nyresvikt). VI registrerte OGSÅ EKG-egenskapene med og uten smerte, samt informasjon referert til ledelsen etter første akuttbehandling(kateterisering, angioplastier, bypassoperasjon, etc.), den endelige diagnosen og pasientdestinasjonen.
pasienter med ST-segment elevation ACS ble ekskludert, som de med nylig manifestert venstre buntblokk, defibrillering eller kardioversjon før de første laboratoriebestemmelsene, hjertekirurgi i de tre ukene før opptak, gravide kvinner, pasienter med alvorlig kognitiv svekkelse og personer med kronisk nyresvikt utsatt for hemodialyse.
i løpet av de første 12 timene i HES, Intensivavdelingen (ICU) eller sykehusavdelingen ble det oppnådd serielle blodprøver for måling av hs-TnT, basert på følgende protokoll:
- –
Eksempel T0. På tidspunktet for første assistanse i HMS.
- –
Eksempel T1. To timer etter prøvetakingstidspunkt 0 eller umiddelbart før opptak til noen sykehusenhet(ICU eller avdeling).
- –
Eksempel T2. Mellom 4 og 6 timer etter prøvetakingstidspunkt 0 eller umiddelbart før opptak til noen sykehusenhet.
- –
Eksempel T3. Mellom 8 og 12 timer etter prøvetakingstidspunkt 0 hvis pasienten fortsatt var i tjenesten, eller umiddelbart før opptak til en sykehusenhet, eller på tidspunktet for pasientens utslipp fra HMS.
tilstrekkelig blod ble samlet for å oppnå 5 alikvoter på 0,5 ml heparinisert plasma fra hver av pasientens prøver, i tillegg til prøven som kreves for rutinemessig testing. Aliquotene ble frosset ved -80 hryvnias C, og ble identifisert med koden til hvert senter: tre sifre som tilsvarer pasientnummer og innsamlingstidspunkt (T0, T1, T2 eller T3), i henhold til prøven som er involvert. Et gjennomsnitt på 3,7 prøver per pasient ble oppnådd. Alle prøvene ble overført til kjernelaboratoriet (Hospital Sant Pau, Barcelona) for analyse AV 4G cTn og hs-TnT, med ikke mer enn en måned å gå fra hver samling. Sykehusene utførte alle den rutinemessige 4g cTn-testen som ble brukt på den tiden(2 sentre med cTnT og 3 med cTnI). Den endelige pasientdiagnosen ble etablert av en ekspert, basert på all klinisk informasjon gitt av saksrapportskjemaet utfylt av hovedutforsker i hvert senter, som gjenspeiler kliniske OG EKG-data, og den sentraliserte 4g cTn-bestemmelsen som ble gjort i kjernelaboratoriet. Eksperten ble blindet for hs-cTn-bestemmelsene.
Infarkt ble diagnostisert med en økning eller reduksjon i cTnT-konsentrasjon på > 20% (Δ kriterium) blant flere prøver, med minst en verdi større enn p99 for referansepopulasjonen (≥ 0,01 µ). Diagnosen ustabil angina (UA) ble etablert hos pasienter med klinisk bevis på myokardisk iskemi uten positiv 4g cTn. Pasientene med UA presenterte en historie med hvilende angina, forverring av tidligere kronisk angina, st-segmentendringer som tyder på iskemi uten biomarkørvariasjoner (kinetikk), positive iskemiske deteksjonstester eller stenose>70% av en koronararterie som vist ved koronar angiografi. CTnT-nivåene ble i sin tur målt ved hjelp av en høy følsomhetsteknikk på En Cobas e601 analysator (hs-TnT, Roche Diagnostics, Basel, Sveits). Teknikken har en detekteringsgrense på 5,0 ng / l, og referansen p99, brukt som klinisk beslutningsgrense, var 13,0 ng / l. analytisk unøyaktighet av disse cTn-testene ble evaluert i 20 repetisjoner av 8 grupper av prøver med sluttkonsentrasjoner justert for å dekke området mellom 7 og 928ng / l, fortynning av en høy cTnT-konsentrasjonsprøve med et serumbasseng som presenterte uoppdagbare hs-TnT-nivåer (
ng / l). P99 i cTnT-testen (10ng/l=0,01 µ/l) ble målt med en variasjonskoeffisient (CV) på 15,2%. VERDIEN MED CV 10% var 35ng / l=0.035 µ / l. P99 av hs-TnT-testen (13ng/l) ble målt med EN CV på 6.9%.
Frekvenser og prosenter ble beregnet for deskriptiv analyse av de kvalitative variablene, med sentrale tendensmål for de kvantitative variablene. Dataene ble uttrykt som gjennomsnitt og standardavvik (SD) i nærvær av en normalfordeling, og som median og interkvartilt område (IQR) i tilfelle en ikke-normalfordeling som vist Ved Kolmogorov-Smirnov-testen.
sammenligningen av kvantitative variabler var basert på Studentens t-test Eller Mann–Whitney U-test i nærvær eller fravær av en normal datafordeling, henholdsvis. Sammenligningen av kvalitative variabler i sin tur var basert på chi-squared test eller Fisher exact test, som aktuelt.
i alle tilfeller ble nivået av statistisk signifikans definert som 5% (α=0,05%) i to-tailed testing.
4g cTn-og Hs-TnT-diskrimineringsstudien ble utført ved beregning av arealet (AUC) under roc-kurven ved de forskjellige prøvetakingstidspunktene, med tilsvarende 95% konfidensintervall (KI). Betydningen av disse kurvene ble evaluert ut fra beregning AV KI FOR AUC, og definert som signifikante disse verdiene i areal med en nedre grense på over 0,5%. Sammenligningen av områder under ROC-kurven ble gjort ved å studere overlappingen AV CI-verdier.
Diagnostisk ytelse ble vurdert ved å beregne sensitivitet, spesifisitet og de positive og negative prediktive verdiene. 95% konfidensintervall ble beregnet for klinisk vurdering av omfanget av disse tiltakene-intervallet ble ansett som signifikant i fravær av overlapping av verdiene.
Resultater
studien omfattet totalt 351 pasienter; 234 var menn (67,9%), og gjennomsnittsalderen var 65,7 år. De viktigste demografiske data og kardiovaskulære risikofaktorer er oppsummert I Tabell 1. En endelig diagnose AV AMI ble etablert hos 77 pasienter, MED UA hos 102 pasienter. Totalt 172 pasienter ble diagnostisert med INGEN ACS.
Egenskaper og kardiovaskulære risikofaktorer i studieprøven.
| Variabler | Totalt | Ingen ACS | Ustabil angina | AMI | p |
|---|---|---|---|---|---|
| Nei. pasienter n (%) | 351 | 172 (49) | 102 (29.1) | 77 (21.9) | – |
| alder (median) | 66 (27-93) | 64.4 (27-93) | 71 (31-90) | 73 (36-88) | |
| Menn, % | 67.9 | 61.5 | 73.5 | 74 | |
| Sykdomshistorie n (%) | |||||
| AHT | 220 (62) | 101 (58.7) | 73 (71.6) | 46 (59.6) | NS |
| Diabetes | 92 (26.2) | 38 (22.1) | 35 (34.3) | 19 (24.7) | NS |
| Hjertesvikt | 52 (14.8) | 20 (11.6) | 20 (19.6) | 12 (15.6) | NS |
| Glomerulær filtreringshastighet (ml/min / 1,73 m2) | 79.6 | 81.9 | 80.7 | 72.9 | |
| tnt µ / l (median) | 0.285 (0.01–6.87) | 0.009 (0.001–0.46) | 0.009 (0.009–0.03) | 0.066 (0.009–6.870) | |
| Hs-TnT ng / l (median) | 63.87 (2.99–7.096) | 5.5 (1.2–481.6) | 11.69 (1.99–66) | 90.4 (2.9–7.096) | |
| NT-proBNP pg / ml (median) | 1.130 (5.46255) | 141 (5-13.302) | 238.5 (16.4–9.164) | 589 (41-46.255) | |
| Elektrokardiogram med smerte (70.67%) | |||||
| Normal | 103 (41.1) | 70 (61.4) | 22 (27.5) | 11 (20) | |
| T neg | 57 (23) | 21 (18.6) | 23 (28.8) | 13 (23.6) | |
| ↓ ST | 60 (24.5) | 9 (8) | 26 (32.6) | 25 (45.4) | |
| Utvikling av symptomer (min) (88%) | |||||
| ≤3h (%) | 46 | 63 (42) | 43 (44.8) | 41 (55.4) | 0.16 |
| >3h (%) | 57 | 87 (58) | 53 (55) | 33 (44.6) | NS |
| Catheterization | 36.9 | 12 (7) | 64 (62.7) | 53 (68.8) | |
| Angioplasty | 20.9 | 2 (1.2) | 29 (28.4) | 41 (53.2) | |
| Stent | 18.7 | 1 (0.6) | 28 (27.5) | 35 (45.5) | |
| Bypass | 2.2 | 0 | 4 (3.9) | 4 (5.2) | |
| Emergency service utslipp | 41.1 | 128 (74.7) | 10 (10.9) | 5 (6.6) | |
| Sykehus utslipp | 57.8 | 44 (25.3) | 92 (88.1) | 72 (91) | |
| Døden | 1.1 | 0 | 1 (1.9) | 3 (3.8) | |
AHT: arteriell hypertensjon; AMI: akutt myokardinfarkt; NS: ikke-signifikant; nt-proBNP: hjerne natriuretisk peptid; ACS: akutt koronarsyndrom; TnT: troponin T; hs-TnT: høy følsomhet troponin T.
totalt 55,4% av pasientene med AMI nådde HMS innen de første tre timene, mens en større prosentandel av både DE med UA og de uten ACS ankom etter tre timer. Med hensyn til positivitet av markørene i henhold til den endelige diagnosen, presenterte 87% av pasientene MED en endelig diagnose AV AMI 4G cTn>0,035 µ / l i løpet av de første 12 timene av studien. I tilfelle av ikke-ACS-pasienter og DE med UA ble positivitet registrert i 4% av tilfellene. Hs-TnT-konsentrasjonen var >13ng/l (p99) hos henholdsvis 26,7% og 46% av pasientene diagnostisert med ikke-ACS og UA (Fig . 1). PÅ DEN annen side bruker 4g cTn p99 med et avskjæringspunkt på 0.01µ / l (gullstandarden i studien) viste seg positiv hos 16% av pasientene diagnostisert MED UA og hos 11% av de uten ACS.
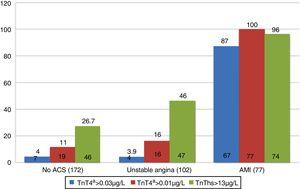
Markør positivitet i henhold til endelig diagnose. AMI: akutt myokardinfarkt; ACS: akutt koronarsyndrom; TnT: troponin T; hs-TnT: høy følsomhet troponin T.
ved bruk av kinetikk blant noen av de fire bestemmelsene (Δ-kriterium) viste 21,5% av pasientene med UA en økning i hs-TnT+Δ (Fig. 2).

Positivitet+Δ av markørene i henhold til endelig diagnose. AMI: akutt myokardinfarkt; ACS: akutt koronarsyndrom; TnT: troponin T; Hs-TnT: høy følsomhet troponin T.
ved første måling (T0) var diagnostisk følsomhet for Hs-TnT signifikant større enn 4G cTn (CV) (87,0%; 83,0–90,3% vs. 42,9%; 37,6–48,2%; p
0,05), noe som resulterte i en negativ prediktiv verdi på 95,1%. Spesifisiteten (71,5%; 66,5-76,2% vs. 97,4%; 95,2-98,8%; p0.05) og positiv prediktiv verdi (46,2% vs. 82,5; p0.05) var klart lavere enn FOR 4g cTn (CV). Ved analyse av området under ROC-kurven ble hs-TnT sett å være overlegen TIL 4G cTn (CV) (0,792; 0,746–0,833 vs. 0,701; 0,650–0,748) (Figs. 3 og 4).
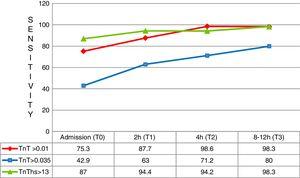
Følsomhet ved de forskjellige testtider. TnT: troponin T; hs-TnT: høy følsomhet troponin T.
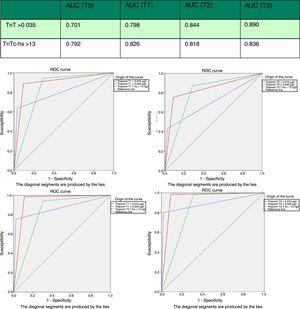
Område under kurven (AUC) av hs-TnT OG TnT 4G i sampling og mottaker driftskarakteristikk (ROC) kurver. AUC: område under kurven; TnT: troponin T; hs-TnT: høy følsomhet troponin T.
To timer etter at pasienten ankom HES (T1), fortsatte Hs-TnT å vise langt høyere diagnostisk sensitivitet enn 4g cTn (94,4%; 91,3-96,6 vs. 63,0%; 57,6-68,2; p0.05). Den negative prediktive verdien av hs-TnT var praktisk talt absolutt (97,9%), og den diagnostiske nøyaktigheten hadde en tendens til å være bedre ENN 4G cTn (ROC 0,826 vs. 0,798). Den lave spesifisiteten til hs-TnT resulterte i en lav positiv prediktiv verdi (46.5%). Resten av prøvetakingsresultatene viste seg å være like, men reflekterer mindre diagnostisk ytelse.
I de første tre timene etter symptomdebut kom totalt 41 pasienter med en endelig DIAGNOSE AV AMI. I disse tilfellene var den overlegne diagnostiske sensitiviteten til Hs-TnT med HENSYN TIL 4g cTn (CV) og OGSÅ 4g cTn (p99) spesielt signifikant, med en sensitivitet på henholdsvis 87,8% versus 36,6% og 73,2% (Fig . 5).
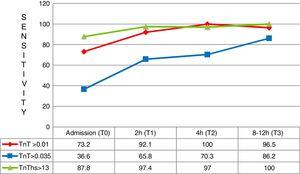
Følsomhet ved ulike testtider for pasienter med symptomdebut min. TnT: troponin T; hs-TnT: høy følsomhet troponin T.
pasientene diagnostisert med hjerteinfarkt uten st-elevasjon (n=36) og med lange utviklingstider (> 3h) viste mindre diagnostisk nøyaktighet med hs-TnT (på grunn av lavere spesifisitet) enn pasientene med kortere tid fra symptomdebut. Ved bruk av kinetikk ble det igjen observert å få i spesifisitet, med en økning i AUC. Når det gjelder Hs-TnT, startet vi derfor med en spesifisitet på 69%, og ved Bruk Av Δ nådde spesifisiteten 85%, med en positiv prediktiv verdi på 55,3%, som forbedret den generelle diagnostiske ytelsen (Tabell 2).
Kinetikk (Δ) av de forskjellige kardiale troponinene hos pasienter med symptomdebut > 180min.
| Følsomhet | Spesifisitet | PPV, % | NPV, % | AUC | |
|---|---|---|---|---|---|
| cTnT> 0.01+Δ | 100% (97.9–100) | 96.4% (92.4–98.6) | 86.8 | 100 | 0.982 |
| cTnT> 0.035+Δ | 81.8% (75.2–87.2) | 97.9% (94.4–99.4) | 90.0 | 95.8 | 0.898 |
| hs-TnT> 13 + Δ | 78.8% (71.9–84.6) | 85.0% (78.8–89.9) | 55.3 | 94.4 | 0.818 |
AUC: område under kurven; cTnT: hjerte troponin T; hs-TnT: høy følsomhet troponin T; PPV: positiv prediktiv verdi; npv: negativ prediktiv verdi.
i tillegg evaluerte vi de optimale cut – off poeng avledet FRA ROC analyse. Det optimale punktet ble etablert som 37ng / l(Hs-TnT-ROC) (Tabell 3). Verdien for hs-TnT-ROC presenterte en følsomhet på 59.7% – langt under hs-TnT, men større enn 4G TnT – CV) – og en spesifisitet på 95,3% i den første målingen. Denne større følsomheten med hensyn TIL 4G TnT (CV) fortsatte i resten av prøvene.
Sammenligning av diagnostisk ytelse av hs-TnT ROC (> 37).
| T0 | Sensitivity, % | Specificity, % | EFF, % | LR+ | LR− | PV+, % | PV−, % |
|---|---|---|---|---|---|---|---|
| cTnT>0.01 | 75.3 | 91.2 | 87.7 | 8.60 | 0.27 | 70.7 | 92.9 |
| cTnT>0.035 | 42.8 | 97.5 | 85.5 | 16.8 | 0.59 | 82.5 | 85.8 |
| Hs-TnT>13 | 87 | 71.5 | 74.9 | 3.1 | 0.18 | 46.2 | 95.1 |
| Hs-TnT>37 | 59.7 | 95.3 | 87.5 | 12.6 | 0.42 | 78 | 89.4 |
cTnT: hjerte troponin T; Hs-TnT: høy følsomhet troponin T.
tidsbesparelsen ved å nå en diagnose ved bruk av hs-TnT versus 4g cTn (CV) var 113min. Besparelsen vil i sin tur være 147min (p0.001) for pasienter innlagt under 3 timer fra symptomdebut, og 63min (p=0,024) for pasienter innlagt over tre timer fra symptomdebut.
Diskusjon
dataene som er oppnådd I denne studien, er i stand til å avklare visse spørsmål om bruk av hs-TnT i beslutningsprosesser, i lys av det sterke beviset på bruken som et diagnostisk og prognostisk verktøy i ACS. Den diagnostiske ytelsen til vår Hs-TnT ble til slutt sett på å være større enn 4G cTn ved hver av de forskjellige prøvetakingstidspunktene. Ytelse i sin tur ble sett å redusere i løpet av timene etter symptomstart. I vår studie brukte vi relative endringer mellom to prøver (spesielt 20%) som diskret forbedret den positive prediktive verdien, men uten å bli praktisk brukt. I denne forbindelse kan En Δ på 20% muligens være for liten, og som foreslått av noen forfattere, kunne det vært tilrådelig å øke Δ til en høyere prosentandel, siden mange tilfeller AV AMI ble funnet å være ved verdier diskret høyere enn den øvre referansegrensen (URL).9,10 andre utprøverne foreslår relative endringer Av Δ (mellom 30 og 250%) for å øke diagnostisk spesifisitet og forbedre DIAGNOSEN AMI.11-14 Mueller et al.15 publiserte resultater som forklarer hvorfor relative endringer av Δ mislykkes ved kjennelse ved hjerteinfarkt uten st-elevasjon. Ved bruk av absolutte endringer av Δ synes en økning eller reduksjon på minst 9,2 ng/l for populasjonen av PASIENTER MED ACS og ikke-ACS, eller på 6,9 ng/l for en populasjon med ACS, å være mer adekvat enn relative endringer Av Δ for å utelukke AMI. I tillegg til disse problemene med reduksjon i spesifisitet, er det forskjeller I URL i henhold til testen som brukes. Dette fremhever betydningen av rase, kjønn,alder eller antall deltakere i studien, 16 og legger til økt vanskeligheter med å nå konsensus i beslutningsprosessen.
i vår studie ble overlegenheten av følsomheten til hs-TnT ved diagnostisering av hjerteinfarkt uten ST-elevasjon funnet å være større hos pasienter med nylig symptomdebut, i samsvar med funnene fra andre forfattere.17,18 for en pasient som rapporterer med brystsmerter i mindre enn tre timer, og med en andre negativ bestemmelse to timer etter ankomst, kan VI utelukke AMI i nesten 100% av tilfellene. Dette, kombinert med kliniske funn og EKG-funn, kan identifisere kandidater for tidlig utskrivning og poliklinisk behandling. På den annen side viser pasienter diagnostisert med ikke-st-elevasjonsinfarkt og som presenterer lange evolutive tider (over 3h) mindre diagnostisk nøyaktighet med hs-TnT, selv når de utfører to serielle bestemmelser. I disse tilfellene bør vi vurdere de optimale cut – off poeng avledet FRA ROC analyse. I vår studie var cut-off punktet 37ng / l, noe som ville tillate oss å «herske i», dvs. pasienter med score over dette cut-off punktet ville ha en svært høy sannsynlighet for å presentere AMI. Det har også blitt hevdet at denne nedgangen i spesifisitet har blitt undervurdert i litteraturen, og at den ikke reflekterer pasientene sett i HMS på våre sykehus, hvor gjennomsnittlig alder, comorbiditeter og cTn høyder har en tendens til å være høy.
tiden til diagnose er sterkt redusert (fra 247 til 71.5min).19,20 i vår studie var tidsbesparelsen for diagnostisering av hjerteinfarkt uten st-elevasjon 147 minutter for pasienter som rapporterte under tre timer etter symptomdebut og 63 minutter ved rapportering etter 3 timer.
tjueto av pasientene (21,5%) med DIAGNOSE AV UA ved utskrivning ville være tilfeller av hjerteinfarkt uten st-elevasjon etter to bestemmelser av hs-TnT med kinetikk på over 20% mellom dem. Opp til 13.9% av ikke-ACS-pasientene (n = 24) ville vise positivitet med hs-TnT ved bruk av slik kinetikk, og ville korrespondere med andre sykdomstilstander som forårsaker progressiv hjerteskade, som myokarditt, lungeemboli eller takotsubo syndrom. Ulike hs-TnT-analyser påviser opptil 27% flere TILFELLER AV AMI enn dagens metode hos pasienter med brystsmerter og lav eller middels SANNSYNLIGHET FOR ACS.20,21 det kan til og med spekuleres i at diagnosen UA ville forsvinne, som understreket Av Sabatine et al.22 hos pasienter med positiv treningstesting evaluert med ultrasensitive teknikker. I denne studien var hs-TnI detekterbar hos alle pasientene før testene; forble uten endring i pasientene uten iskemi; og økte 24% hos de med mild iskemi og 40% hos de med moderat til alvorlig iskemi. Ingen endringer ble observert MED 4g cTn. Følgelig er resultatene referert til diagnosen ikke-st-elevasjonsinfarkt ved bruk av konvensjonell cTn et spørsmål om bekymring, siden myokardskade har et begrenset mål og cTn-verdiene ikke alltid stiger tidlig, eller deres trinn er ikke tilstrekkelige for å tillate tidlig identifisering.
Raske løsningsprotokoller bør innføres, hvor våre pasienter med lav iskemisk risiko og en normal EKG-sporing bare vil bruke 3-4h på sykehus.23,24 det har blitt vurdert om en enkelt hs-TnT-bestemmelse er tilstrekkelig for å utelukke AMI, 25 og andre studier har vurdert muligheten for en enkelt bestemmelse hvis hs-TnT-verdien er
ng / l (dvs.uoppdagelig).24 alle disse situasjonene må vurderes i fremtiden.Konklusjoner
høy følsomhet troponin T-testing forbedrer diagnostisk ytelse, forkorter tiden til diagnose AV AMI, og er i stand til å identifisere et større antall pasienter med mindre infarkter, som tidligere ble diagnostisert SOM UA og som har høy dødelighetsrisiko, sammenlignet med konvensjonell cTn. VIDERE forkorter det tiden for å utelukke tilfeller, SIDEN AMI kunne kasseres innen 2 timer. alt dette innebærer tidligere behandling for pasienter med myokardnekrose og en forkortelse av pasientens opphold i HMS. Men hos de individer som rapporterer TIL HMS etter tre timer med symptomstart, vil hs-TnT ikke kunne forbedre den diagnostiske ytelsen TIL 4G cTn, og beslutningsprosesser må derfor være mer forsiktige. Hs-cTn-testene endrer ledelsen og konseptet til pasienter med brystsmerter som tyder PÅ ACS. Dette gjør det nødvendig for akutt og kritisk omsorg leger å bli kjent med deres rutinemessige bruk.
Interessekonflikter
forfatterne erklærer at de ikke har noen interessekonflikter.