reactie: hydratatie van alkynen
net als bij alkenen vereist hydratatie (toevoeging van water) aan alkynen een sterk zuur,meestal zwavelzuur, en wordt vergemakkelijkt door kwiksulfaat. In tegenstelling tot de toevoegingen aan dubbele bindingen die alcoholproducten opleveren, levert de toevoeging van water aan alkynen ketonproducten op ( behalve acetyleen dat acetaldehyde oplevert ). De verklaring voor deze afwijking ligt in enol-keto tautomerisatie, geïllustreerd door de volgende vergelijking. Het eerste product van de toevoeging van water aan een alkyne is een Enol (een verbinding met een hydroxylsubstituent verbonden aan een dubbele binding), en dit herschikt onmiddellijk naar de stabielere keto tautomeer.
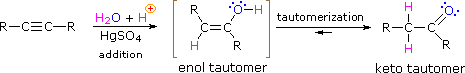
Tautomeren worden gedefinieerd als snel onderling geconverteerde constitutionele isomeren, die gewoonlijk worden onderscheiden door een andere bindingsplaats voor een labiel waterstofatoom (hier rood gekleurd) en een verschillend gelokaliseerde dubbele binding. Het evenwicht tussen tautomeren is niet alleen snel onder normale omstandigheden, maar het is vaak sterk voorstander van een van de isomeren ( aceton, bijvoorbeeld, is 99,999% keto tautomeer ). Zelfs in dergelijke eenzijdige evenwichten komt het bewijs voor de aanwezigheid van de kleine tautomeer uit het chemische gedrag van de verbinding. Tautomere evenwichten worden gekatalyseerd door sporen van zuren of basen die over het algemeen aanwezig zijn in de meeste chemische monsters. De drie onderstaande voorbeelden illustreren deze reacties voor verschillende substituties van de drievoudige binding. De tautomerisatiestap wordt aangegeven door een rode pijl. Voor eindalkynen volgt de toevoeging van water de Markovnikov-regel, zoals in het tweede voorbeeld hieronder, en het eindproduct is een methylketon (behalve voor acetyleen, weergegeven in het eerste voorbeeld). Voor interne alkynen (de drievoudige binding is binnen een langere keten) is de toevoeging van water niet regioselectief. Als de drievoudige binding niet symmetrisch is gelokaliseerd ( d.w.z. als R & R ‘ in de derde vergelijking niet hetzelfde is) worden twee isomere ketonen gevormd.
HC≡CH + H2O + HgSO4 & H2SO4 –> –> H3C-CH=O
RC≡CH + H2O + HgSO4 & H2SO4 –> –> RC(=O)CH3
RC≡CR’ + H2O + HgSO4 & H2SO4 –> –> RCH2-C(=O)R’ + RC(=O)-CH2R’
Met de toevoeging van water, alkynen kan worden gehydrateerd te vormen enols die spontaan tautomerize aan ketonen. De reactie wordt gekatalyseerd door kwikionen. Volgt de regel van Markovnikov: Terminale alkynen geven methylketonen
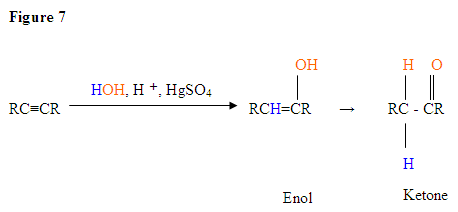
- de eerste stap is een zuur / base reactie waarbij de π elektronen van de drievoudige binding dienst doen als een Lewis base en het proton aanvallen waardoor de koolstof met de meeste waterstofsubstituenten protineert.
- de tweede stap is de aanval van het nucleofiele watermolecuul op de elektrofiele carbocatie, waardoor een oxonium-ion ontstaat.
- vervolgens deprotoneer je door een base, waardoor een alcohol ontstaat die een Enol wordt genoemd, die vervolgens tautomeriseert tot een keton.
- Tautomerisme is een gelijktijdige verschuiving van proton en dubbele binding, die van de enolvorm naar de keto-isomeervorm gaat, zoals hierboven in Figuur 7 wordt getoond.
laten we nu eens kijken naar enkele Hydratatiereacties.
hydratatie van Terminale Alkyne produceert methylketonen
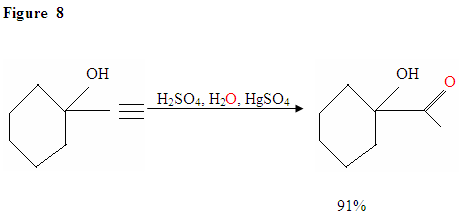
net zoals beschreven in Figuur 7 vallen de elektronen π een proton aan, waardoor een carbocatie ontstaat, die dan wordt aangevallen door de nucleofiele watermoleculen. Na deprotinatie, produceren wij een enol, die dan in de getoonde ketonvorm tautomerizes.
hydratatie van Alkyne
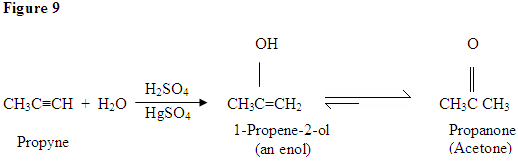
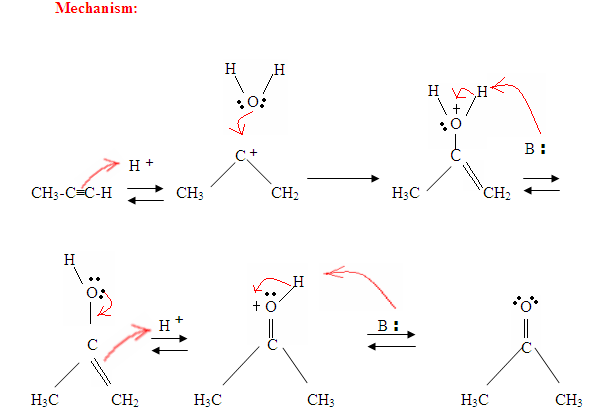
zoals je hier kunt zien vallen De π elektronen van de drievoudige binding het proton aan, dat een covalente binding vormt op de koolstof met de meeste waterstofsubstituenten. Zodra de waterstof is gebonden heb je een carbocatie, die wordt aangevallen door het watermolecuul. Nu heb je een positieve lading op de zuurstof, wat resulteert in een base die binnenkomt en het molecuul deprotineert. Eenmaal gedeproteerd, heb je een enol, die dan wordt tautomerized.
Tautomerisme wordt hier getoond wanneer het proton wordt aangevallen door de dubbele binding π elektronen die een covalente binding vormen tussen de koolstof en de waterstof op de minder gesubstitueerde koolstof. Elektronen uit de zuurstof uiteindelijk verplaatsen naar de koolstof, vormen een dubbele binding met koolstof en geven zichzelf een positieve lading, die dan wordt aangevallen door de basis. De base deprotineert de zuurstof wat resulteert in het stabielere eindproduct bij evenwicht, dat een keton is.
oefening \(\Paginindex{1}\)
- teken de structuur van het product dat wordt gevormd wanneer elk van de onderstaande stoffen wordt behandeld met H2O/H2SO4 in aanwezigheid van HgSO4.
- $ \ ce{\sf{CH3-CH2-C#C-H}}$
-
- teken de structuur van de keto vorm van de verbinding hieronder weergegeven. Welke vorm verwacht je het meest stabiel te zijn?
antwoord
antwoorden:
de keto-vorm moet het meest stabiel zijn.
vragen
Q9.4.1
met welke alkyne zou je beginnen om de volgende producten te verkrijgen, in een oxidatiereactie? Denk aan resonantie.

V9. 4.2
stellen een reactieschema voor voor de volgende verbinding, uitgaande van de alkyne en met de vereiste reagentia en tussenproducten.

Oplossingen
S9.4.1

S9.4.2
