introduktion
adekvat tolkning av myokardiell nekrosmarkörer är avgörande för diagnos, stratifiering och behandling av patienter med misstänkt akut koronarsyndrom (ACS). Protokollen om hjärtmarkörer för akut hjärtinfarkt (AMI) hänvisas till den tredje universella definitionen av AMI.
detta dokument fastställer att hjärt – troponin (cTn) höjning och sänkning är grundläggande för att fastställa diagnosen i samband med ischemiska symtom, elektrokardiografiska förändringar eller nyligen manifesterade segmentförändringar i en bildstudie.1
tekniska framsteg i bestämningen av cTn har förbättrat förmågan att upptäcka och kvantifiera myokardiell cellskada. Kriterierna för höjning av cTn-värdena beror på vilket test som används och måste definieras på grundval av precisionsprofilen för varje test, inklusive den för högkänslighetsprovning.2 förekomsten av olika kommersiella ctn-immunanalyser med olika percentil 99 (p99) koncentrationer; det faktum att vissa laboratorier använder olika referenser till testresultaten för myokardiell skada (”normal”, ”obestämd” eller ”suggestiv”); och den urskillningslösa användningen av cTn-testning i stora populationer med mycket olika sannolikheter för att presentera ACS tenderar att skapa förvirring i samband med klinisk hantering.
det finns ett signifikant antal patienter som i frånvaro av AMI ändå uppvisar ctn-koncentrationer>p99. Dessa patienter har vanligtvis kardiovaskulära riskfaktorer, och sannolikheten för komplikationer hos sådana individer liknar den hos patienter med ACS.3
de senaste europeiska rekommendationerna om hantering av patienter med akut koronarsyndrom utan ST-höjd (NSTE-ACS) förespråkar användning av högkänslig cTn (hs-ctn) jämfört med konventionella eller fjärde generationens (4G) troponiner och överväger upp till två algoritmer (0h/3h, 0h/1h) för bekräftelse (regel in) eller uteslutning (regel ut) av AMI.4
Hjärttroponiner är extremt specifika för myokardiell skada. Men på något sätt är myokardiell skada exklusiv för ACS. Följaktligen understryker de kliniska guiderna att ctn-koncentrationen måste tolkas i förhållande till patientens symtom. I detta avseende ökade ctn-koncentrationer hos patienter med sepsis, hypertensiva kriser, lungemboli etc., indikerar myokardiell skada, men inte av AMI, och bör inte användas för att indikera specifika behandlingar för ACS.5
termen” hög känslighet ” bör reserveras för de immunanalyser som kan bestämma p99 med en variationskoefficient (CV) på 6
det finns tvivel i det vetenskapliga samfundet om huruvida användningen av hs-cTn representerar signifikant klinisk förbättring, och om det innebär fler tester och interkonsultationer.7 föreliggande studie genomfördes för att utvärdera den diagnostiska prestandan hos högkänslig troponin T (hs-TnT), avgöra om det förkortar tiden för diagnos och analysera de kliniska konsekvenserna av dess användning.
metod
en prospektiv, longitudinell observationsstudie genomfördes i sjukhusets akutmottagning (HES) på sjukhus Cl-sjukhuset (Valencia), sjukhus Cl-sjukhuset (m-badet), sjukhus Severo Ochoa (Legan-badet), sjukhus Sant Pau (Barcelona) och sjukhus Miguel Servet (Zaragoza) (Spanien), som involverade patienterna i Tusca-försöket (Troponina Ultrasensible en el SCA) 8 mellan juni 2009 och April 2010. Studien genomfördes i överensstämmelse med principerna i Helsingforsdeklarationen och godkändes av de lokala Etikutskotten för de deltagande centren. Skriftligt informerat samtycke erhölls från alla patienter. Vi inkluderade i följd patienter över 18 år sett i HES på grund av bröstsmärta som tyder på NSTE-ACS. Patientregistrering gjordes under initial vård i HES, efter bedömning av inkluderings-och uteslutningskriterierna. Patienthantering och den tillämpade behandlingen följde interna protokoll baserade på konsensusguiderna från European Society of Cardiology, under indikationerna från de läkare som ansvarar för patienterna hela tiden och med totalt oberoende av deltagande i studien. Seriella 4G cTn-bestämningar gjordes för diagnos av ACS, i enlighet med rutinmässig klinisk och immunanalyspraxis i varje centrum.
patientegenskaperna registrerades i ett fallrapportformulär och omfattade demografiska data, tid hänvisad till symtomdebut, förekomst av riskfaktorer (arteriell hypertoni, diabetes mellitus, kronisk obstruktiv lungsjukdom , hjärtsvikt och njursvikt). Vi registrerade också EKG-egenskaperna med och utan smärta, liksom information som hänvisades till hantering efter initial akutvård (kateterisering, angioplastier, bypassoperation etc.), den slutliga diagnosen och patientens destination.
patienter med ST-segmenthöjning ACS exkluderades, liksom de med nyligen manifesterande vänster buntblock, defibrillering eller kardioversion före de första laboratoriebestämningarna, hjärtkirurgi under de tre veckorna före antagning, gravida kvinnor, patienter med svår kognitiv försämring och patienter med kroniskt njursvikt utsatt för hemodialys.
under de första 12 timmarna av vistelsen i HES, intensivvårdsavdelningen (ICU) eller sjukhusavdelningen erhölls seriella blodprover för mätning av hs-TnT, baserat på följande protokoll:
- –
Prov T0. Vid tidpunkten för första hjälpen i HES.
- –
Prov T1. Två timmar efter provtagningstidenpunkt 0 eller omedelbart före tillträde till någon sjukhusenhet (ICU eller avdelning).
- –
Prov T2. Mellan 4 och 6 timmar efter provtagningstid 0 eller omedelbart före tillträde till någon sjukhusenhet.
- –
Prov T3. Mellan 8 och 12 timmar efter provtagningstidpunkt 0 om patienten fortfarande var i tjänsten, eller omedelbart före tillträde till någon sjukhusenhet, eller vid tidpunkten för patientens urladdning från HES.
tillräckligt med blod uppsamlades för att erhålla 5 alikvoter av 0, 5 ml hepariniserad plasma från vart och ett av patientens prover, förutom det prov som krävs för rutintestning. Alikvoterna frystes vid -80 kcal C och identifierades med koden för varje centrum: tre siffror som motsvarar patientnumret och insamlingstidpunkten (T0, T1, T2 eller T3), enligt det berörda provet. I genomsnitt erhölls 3,7 prover per patient. Alla prover överfördes till kärnlaboratoriet (Hospital Sant Pau, Barcelona) för analys av 4G cTn och hs-TnT, med högst en månad som får gå från varje samling. Sjukhusen utförde alla det rutinmässiga 4G cTn-testet som användes vid den tiden (2 centra med cTnT och 3 med cTnI). Den slutliga patientdiagnosen fastställdes av en expert, baserat på all klinisk information som tillhandahålls av fallrapportformuläret som fyllts i av huvudutredaren i varje centrum, vilket återspeglar kliniska och EKG-data och den centraliserade 4G ctn-bestämningen gjord i kärnlaboratoriet. Experten var blind för HS-cTn-bestämningarna.
infarkt diagnostiserades i närvaro av en höjning eller minskning av cTnT-koncentrationen på >20% (kriteriet för Kakor) bland flera prover, med minst ett värde större än P99 för referenspopulationen (0, 01 kakor i 0,01 kg/l). Diagnosen av instabil angina (UA) fastställdes hos patienter med kliniska bevis på myokardiell ischemi utan positiv 4G cTn. Patienterna med UA presenterade en historia av vilande angina, försämring av tidigare kronisk angina, ST-segmentförändringar som tyder på ischemi utan biomarkörvariationer (kinetik), positiva ischemidetekteringstester eller stenos>70% av en kransartär, vilket framgår av koronarangiografi. CTnT-nivåerna mättes i sin tur med hjälp av en högkänslighetsteknik på en Cobas e601-analysator (hs-TnT, Roche Diagnostics, Basel, Schweiz). Tekniken har en detektionsgräns på 5, 0 ng/l och referensen p99, som användes som klinisk beslutsgräns, var 13, 0 ng/l. den analytiska oprecisionen av dessa cTn-test utvärderades i 20 repetitioner av 8 grupper av prover med slutkoncentrationer justerade för att täcka intervallet mellan 7 och 928ng/l, utspädning av ett högt cTnT-koncentrationsprov med en serumpool som presenterar odetekterbara hs-TnT-nivåer (
ng/l). P99 för cTnT-testet (10ng/l=0,01 occurg / l) mättes med en variationskoefficient (CV) på 15,2%. Värdet med CV 10% var 35ng/l=0,035 osk / l. P99 för HS-TnT-testet (13ng / l) mättes med ett CV på 6, 9%.
frekvenser och procentsatser beräknades för den beskrivande analysen av de kvalitativa variablerna, med centrala tendensmått för de kvantitativa variablerna. Uppgifterna uttrycktes som medel-och standardavvikelse (SD) i närvaro av en normalfördelning och som median–och interkvartilintervallet (IQR) vid en icke-normalfördelning, vilket framgår av Kolmogorov-Smirnov-testet.
jämförelsen av kvantitativa variabler baserades på studentens t-test eller Mann–Whitney U-test i närvaro eller frånvaro av en normal datafördelning. Jämförelsen av kvalitativa variabler baserades i sin tur på chi-squared-testet eller Fisher exact-testet, beroende på vad som är tillämpligt.
i alla fall definierades nivån av statistisk signifikans som 5% (0,05%) i två-tailed testning.
4G ctn-och hs-TnT-diskrimineringsstudien utfördes beräkning av arean (AUC) under mottagaroperationskarakteristiken (ROC) – kurvan vid de olika provtagningstiderna, med motsvarande 95% konfidensintervall (CI). Betydelsen av dessa kurvor utvärderades från beräkningen av CI för AUC och definierade som signifikanta dessa värden i område med en lägre gräns på över 0,5%. Jämförelsen av områden under ROC-kurvan gjordes genom att studera överlappningen av CI-värden.
diagnostisk prestanda bedömdes genom beräkning av känslighet, specificitet och de positiva och negativa prediktiva värdena. 95% konfidensintervallet beräknades för klinisk bedömning av storleken på dessa åtgärder – intervallet betraktas som signifikant i avsaknad av överlappning av värdena.
resultat
studien omfattade totalt 351 patienter; 234 var män (67,9%) och medelåldern var 65,7 år. De viktigaste demografiska data och kardiovaskulära riskfaktorer sammanfattas i Tabell 1. En slutlig diagnos av AMI fastställdes hos 77 patienter, med UA hos 102 patienter. Totalt 172 patienter diagnostiserades som att de inte hade ACS.
egenskaper och kardiovaskulära riskfaktorer för studieprovet.
| variabler | totalt | ingen ACS | instabil angina | AMI | p |
|---|---|---|---|---|---|
| Nej. patienter n (%) | 351 | 172 (49) | 102 (29.1) | 77 (21.9) | – |
| ålder (median) | 66 (27-93) | 64.4 (27-93) | 71 (31-90) | 73 (36-88) | |
| män, % | 67.9 | 61.5 | 73.5 | 74 | |
| sjukdomshistoria n (%) | |||||
| AHT | 220 (62) | 101 (58.7) | 73 (71.6) | 46 (59.6) | NS |
| Diabetes | 92 (26.2) | 38 (22.1) | 35 (34.3) | 19 (24.7) | NS |
| hjärtsvikt | 52 (14.8) | 20 (11.6) | 20 (19.6) | 12 (15.6) | NS |
| glomerulär filtreringshastighet (ml / min / 1. 73m2) | 79.6 | 81.9 | 80.7 | 72.9 | |
| TNT (median)) | 0.285 (0.01–6.87) | 0.009 (0.001–0.46) | 0.009 (0.009–0.03) | 0.066 (0.009–6.870) | |
| Hs-TnT ng / l (median) | 63.87 (2.99–7.096) | 5.5 (1.2–481.6) | 11.69 (1.99–66) | 90.4 (2.9–7.096) | |
| NT-proBNP pg / ml (median) | 1.130 (5.46255) | 141 (5-13.302) | 238.5 (16.4–9.164) | 589 (41-46.255) | |
| elektrokardiogram med smärta (70.67%) | |||||
| Normal | 103 (41.1) | 70 (61.4) | 22 (27.5) | 11 (20) | |
| T neg | 57 (23) | 21 (18.6) | 23 (28.8) | 13 (23.6) | |
| ↓ ST | 60 (24.5) | 9 (8) | 26 (32.6) | 25 (45.4) | |
| utveckling av symtom (min) (88%) | |||||
| ≤3h (%) | 46 | 63 (42) | 43 (44.8) | 41 (55.4) | 0.16 |
| >3h (%) | 57 | 87 (58) | 53 (55) | 33 (44.6) | NS |
| Catheterization | 36.9 | 12 (7) | 64 (62.7) | 53 (68.8) | |
| Angioplasty | 20.9 | 2 (1.2) | 29 (28.4) | 41 (53.2) | |
| Stent | 18.7 | 1 (0.6) | 28 (27.5) | 35 (45.5) | |
| Bypass | 2.2 | 0 | 4 (3.9) | 4 (5.2) | |
| ansvarsfrihet för räddningstjänsten | 41.1 | 128 (74.7) | 10 (10.9) | 5 (6.6) | |
| utskrivning från sjukhus | 57.8 | 44 (25.3) | 92 (88.1) | 72 (91) | |
| död | 1.1 | 0 | 1 (1.9) | 3 (3.8) | |
AHT: arteriell hypertoni; AMI: akut hjärtinfarkt; NS: nonsignificant; NT-proBNP: hjärnnatriuretisk peptid; ACS: akut koronarsyndrom; TnT: troponin T; hs-TnT: högkänslig troponin T.
totalt nådde 55, 4% av patienterna med AMI HES inom de första tre timmarna, medan en större andel av både de med UA och de utan ACS anlände efter tre timmar. När det gäller markörernas positivitet enligt den slutliga diagnosen presenterade 87% av patienterna med en slutgiltig diagnos av AMI 4G cTn>0,035 Kg/l under de första 12 timmarna av studien. När det gäller icke-ACS-patienter och de med UA registrerades positivitet i 4% av fallen. HS-TnT-koncentrationen var >13ng/l (p99) hos 26, 7% respektive 46% av patienterna som diagnostiserades med icke-ACS respektive UA (Fig. 1). Å andra sidan, 4G cTn använder p99 med en brytpunkt på 0.01 UKG / l (studiens guldstandard) visade sig vara positiv hos 16% av patienterna som diagnostiserats med UA och hos 11% av dem utan ACS.
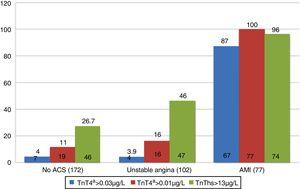
markör positivitet enligt slutlig diagnos. AMI: akut hjärtinfarkt; ACS: akut koronarsyndrom; TnT: troponin T; hs-TnT: högkänslig troponin T.
vid tillämpning av kinetik bland några av de fyra bestämningarna (kriteriet för hCG) visade 21,5% av patienterna med UA en höjning av HS-TNT+qu (Fig. 2).

positivitet+msk markörer enligt den slutliga diagnosen. AMI: akut hjärtinfarkt; ACS: akut koronarsyndrom; TnT: troponin T; hs-TnT: hög känslighet troponin T.
vid första mätningen (T0) var den diagnostiska känsligheten hos hs-TnT signifikant större än den för 4G cTn (CV) (87,0%; 83,0–90,3% mot 42,9%; 37,6–48,2%; p
0,05), vilket resulterade i ett negativt prediktivt värde på 95,1%. Emellertid var dess specificitet (71,5%; 66,5–76,2% mot 97,4%; 95,2–98,8%; p0.05) och positivt prediktivt värde (46,2% mot 82,5; p0.05) klart lägre än 4G cTn (CV). Vid analys av området under ROC-kurvan sågs hs-TnT vara överlägsen 4G cTn (CV) (0.792; 0.746–0.833 vs. 0.701; 0.650–0.748) (Fig. 3 och 4).
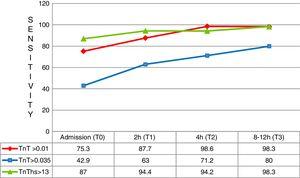
känslighet vid olika testtider. TnT: troponin T; hs-TnT: hög känslighet troponin T.
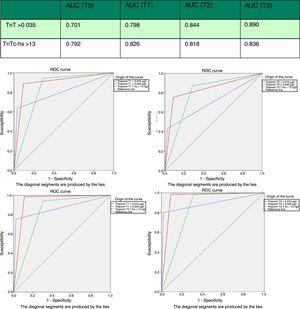
Area under kurvan (AUC) för hs-TnT och TnT 4G i provtagnings-och mottagaroperationskarakteristik (ROC) kurvor. AUC: område under kurvan; TnT: troponin T; hs-TnT: högkänslig troponin T.
två timmar efter patientens ankomst till HES (T1) fortsatte hs-TnT Att visa mycket högre diagnostisk känslighet än 4G cTn (94,4%; 91,3–96,6 mot 63,0%; 57,6–68,2; p0.05). Det negativa prediktiva värdet av hs-TnT var praktiskt taget absolut (97,9%), och dess diagnostiska noggrannhet tenderade att vara överlägsen den för 4G cTn (ROC 0,826 vs. 0,798). Den låga specificiteten hos hs-TnT resulterade i ett lågt positivt prediktivt värde (46,5%). Resten av provtagningsresultaten visade sig vara liknande, men återspeglade mindre diagnostisk prestanda.
under de första tre timmarna efter symtomdebut kom totalt 41 patienter med en slutlig diagnos av AMI. I dessa fall var den överlägsna diagnostiska känsligheten hos hs-TnT med avseende på 4G cTn (CV) och även 4G cTn (p99) särskilt signifikant, med en känslighet på 87, 8% mot 36, 6% respektive 73, 2% (Fig. 5).
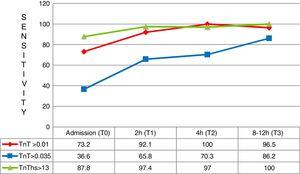
känslighet vid olika testtider för patienter med symtomdebut min. TnT: troponin T; hs-TnT: hög känslighet troponin T.
de patienter som diagnostiserats med hjärtinfarkt utan ST-höjning (n=36) och presenterade långa Evolutiva tider (> 3h) visade mindre diagnostisk noggrannhet med hs-TnT (på grund av lägre specificitet) än patienterna med kortare tid från symtomdebut. Vid applicering av kinetik observerades igen ökad specificitet med en ökning av AUC. Följaktligen, när det gäller hs-TnT, började vi med en specificitet på 69% och, vid tillämpning av XXL, nådde specificiteten 85%, med ett positivt prediktivt värde på 55,3%, vilket förbättrade den totala diagnostiska prestandan (Tabell 2).
kinetik (kg) av de olika hjärt-troponinerna hos patienter med symtomdebut >180 minuter.
| känslighet | specificitet | PPV, % | NPV, % | AUC | |
|---|---|---|---|---|---|
| cTnT> 0,01 + | 100% (97.9–100) | 96.4% (92.4–98.6) | 86.8 | 100 | 0.982 |
| cTnT> 0,035 + | 81.8% (75.2–87.2) | 97.9% (94.4–99.4) | 90.0 | 95.8 | 0.898 |
| hs-TnT> 13 + | 78.8% (71.9–84.6) | 85.0% (78.8–89.9) | 55.3 | 94.4 | 0.818 |
AUC: område under kurvan; cTnT: hjärt troponin T; hs-TnT: hög känslighet troponin T; PPV: positivt prediktivt värde; NPV: negativt prediktivt värde.
dessutom utvärderade vi de optimala avstängningspunkterna som härrör från ROC-analysen. Den optimala punkten fastställdes som 37ng / l (hs-TnT-ROC) (tabell 3). Värdet för hs-TnT-ROC presenterade en känslighet på 59.7% – långt under hs-TnT, men större än 4G TnT (CV) – och en specificitet på 95, 3% i den första mätningen. Denna större känslighet med avseende på 4G TnT (CV) kvarstod i resten av provtagningarna.
jämförelse av diagnostisk prestanda för hs-TnT ROC (> 37).
| T0 | Sensitivity, % | Specificity, % | EFF, % | LR+ | LR− | PV+, % | PV−, % |
|---|---|---|---|---|---|---|---|
| cTnT>0.01 | 75.3 | 91.2 | 87.7 | 8.60 | 0.27 | 70.7 | 92.9 |
| cTnT>0.035 | 42.8 | 97.5 | 85.5 | 16.8 | 0.59 | 82.5 | 85.8 |
| hs-TnT>13 | 87 | 71.5 | 74.9 | 3.1 | 0.18 | 46.2 | 95.1 |
| hs-TnT>37 | 59.7 | 95.3 | 87.5 | 12.6 | 0.42 | 78 | 89.4 |
cTnT: hjärt troponin T; hs-TnT: hög känslighet troponin T.
tidsbesparingen för att nå en diagnos vid användning av hs-TnT kontra 4G cTn (CV) var 113min. Besparingen i sin tur skulle vara 147min (p0.001) när det gäller patienter som tas in under 3 timmar från symtomdebut och 63min (p=0,024) när det gäller patienter som tas in under tre timmar från symtomdebut.
diskussion
de data som erhållits i den aktuella studien kan klargöra vissa frågor angående användningen av hs-TnT i beslutsfattande, med tanke på det starka beviset på dess användbarhet som ett diagnostiskt och prognostiskt verktyg i ACS. Den diagnostiska prestandan hos vår hs-TnT sågs slutligen vara större än den för 4G cTn vid var och en av de olika provtagningstiderna. Prestanda i sin tur sågs minska under timmarna efter symptomstart. I vår studie använde vi relativa förändringar mellan två prover (specifikt 20%) som diskret förbättrade det positiva prediktiva värdet, men utan att bli praktisk användning. I detta avseende kan eventuellt ett 20% – IGT år vara för litet och, som föreslagits av vissa författare, kunde det ha varit tillrådligt att öka antalet år till en högre procentsats, eftersom många fall av AMI befanns ha värden som är diskret högre än den övre referensgränsen (URL).9,10 andra utredare föreslår relativa förändringar av hCG (mellan 30 och 250%) för att öka diagnostisk specificitet och förbättra diagnosen AMI.11-14 Mueller et al.15 publicerade resultat som förklarar varför relativa förändringar av Macau misslyckas för att härska i icke-st höjd hjärtinfarkt. Med användning av absoluta förändringar av vanilj, en ökning eller minskning av minst 9,2 ng/l för populationen av patienter med ACS och icke-ACS, eller av 6,9 ng/l för en population med apelsinjuice, verkar vara mer adekvat än relativa förändringar av apelsinjuice för att utesluta AMI. Förutom dessa problem med minskningen av specificiteten finns det skillnader i URL enligt det använda testet. Detta belyser vikten av ras, kön, ålder eller antalet deltagare i studien,16 och lägger till ökad svårighet att nå enighet i beslutsfattandet.
i vår studie visade sig överlägsenheten av känsligheten hos hs-TnT vid diagnos av icke-ST-höjning av hjärtinfarkt vara större hos patienter med nya symtom, i överensstämmelse med resultaten från andra författare.17,18 för en patient som rapporterar med bröstsmärta i mindre än tre timmar, och med en andra negativ bestämning två timmar efter ankomst kan vi utesluta AMI i nästan 100% av fallen. Detta, i kombination med kliniska och EKG-fynd, kan identifiera kandidater för tidig urladdning och öppenvård. Å andra sidan visar patienter som diagnostiserats med hjärtinfarkt utan ST-höjd och presenterar långa Evolutiva tider (över 3h) mindre diagnostisk noggrannhet med hs-TnT, även när de utför två seriella bestämningar. I dessa fall bör vi utvärdera de optimala brytpunkterna som härrör från ROC-analysen. I vår studie var brytpunkten 37ng / l, vilket skulle göra det möjligt för oss att ”styra in”, dvs patienter med poäng över denna Brytpunkt skulle ha en mycket hög sannolikhet att presentera AMI. Det har också hävdats att denna minskning av specificiteten har underskattats i litteraturen och att den inte återspeglar patienterna som ses på våra sjukhus, där medelåldern, comorbiditeter och ctn-höjningar tenderar att vara höga.
tiden till diagnos har minskat kraftigt (från 247 till 71.5min).19,20 i vår studie var tidsbesparingen för diagnos av hjärtinfarkt utan ST-höjning 147 Min när det gäller patienter som rapporterade under tre timmar efter symtomdebut och 63 min vid rapportering efter 3h.
tjugotvå av patienterna (21,5%) med diagnos av UA vid urladdning skulle vara fall av hjärtinfarkt utan ST-höjning efter två bestämningar av hs-TnT med kinetik på över 20% mellan dem. Upp till 13.9% av icke-ACS-patienterna (n = 24) skulle uppvisa positivitet med hs-TnT vid applicering av sådan kinetik och skulle motsvara andra sjukdomstillstånd som orsakar progressiv hjärtskada, såsom myokardit, lungemboli eller takotsubo syndrom. Olika HS-TNT-analyser upptäcker upp till 27% fler fall av AMI än den nuvarande metoden hos patienter med bröstsmärta och låg eller mellanliggande Sannolikhet för ACS.20,21 det kunde till och med spekuleras i att diagnosen UA skulle försvinna, vilket betonades av Sabatine et al.22 hos patienter med positiv träningstestning utvärderad med ultrakänsliga tekniker. I denna studie var hs-TnI detekterbar hos alla patienter före testen; förblev utan förändring hos patienterna utan ischemi; och ökade 24% hos dem med mild ischemi och 40% hos dem med måttlig till svår ischemi. Inga förändringar observerades med 4G cTn. Följaktligen är resultaten som hänvisas till diagnosen icke-st-höjd hjärtinfarkt med konventionell cTn en fråga om oro, eftersom myokardskada har ett begränsat mått och cTn-värdena inte alltid stiger tidigt, eller deras steg är inte tillräckliga för att möjliggöra tidig identifiering.
snabba lösningsprotokoll bör införas, varigenom våra patienter med låg ischemisk risk och en normal EKG–spårning bara skulle spendera 3-4 timmar på sjukhus.23,24 det har undersökts om en enda HS-TnT-bestämning räcker för att utesluta AMI,25 och andra studier har bedömt möjligheten till en enda bestämning om hs-TnT-värdet är
ng/l (dvs. odetekterbart).24 Alla dessa situationer måste övervägas i framtiden.Slutsatser
troponin T-testning med hög känslighet förbättrar diagnostisk prestanda, förkortar tiden för diagnos av AMI och kan identifiera ett större antal patienter med mindre infarkter, som tidigare diagnostiserades som UA och som har en hög mortalitetsrisk jämfört med konventionell cTn. Dessutom förkortar det tiden för att utesluta fall, eftersom AMI kan kasseras inom 2 timmar. allt detta innebär tidigare behandling för patienter med myokardnekros och en förkortning av patientens vistelse i HES. Men hos de individer som rapporterar till HES efter tre timmars symtomdebut skulle hs-TnT inte kunna förbättra den diagnostiska prestandan för 4G cTn, och beslutsfattandet skulle därför behöva vara mer försiktig. HS-cTn-testerna förändrar hanteringen och konceptet för patienter med bröstsmärta som tyder på ACS. Detta gör det nödvändigt för akut-och kritisk vårdläkare att bekanta sig med sin rutinmässiga användning.
intressekonflikt
författarna förklarar att de inte har några intressekonflikter.