introduktion
den enzymatiska verkan av typ 5-fosfodiesteras (PDE5) är den primära mekanismen för inaktivering av cGMP, nedströms mediator för vasodilaterande medel kväveoxid (NO) (Lugnier, 2006).
under erektil dysfunktion (ED) kan den försämrade produktionen av NO från endotelkavernösa kärl farmakologiskt övervinnas genom användning av PDE5-hämmare (PDE5i) för att förlänga cGMP-halveringstiden och för att förbättra den kvarvarande vasodilaterande funktionen (Hawksworth och Burnett, 2015). Flera molekyler med hämmande aktivitet på PDE5 har sedan projicerats och släppts ut på marknaden, vilket visar olika inverkan och effektens varaktighet. För närvarande är PDE5i det första valet läkemedel som används för behandling av ED (Mehrotra et al., 2007).
trots en erkänd effekt hos nästan 80% av icke-valda ED-patienter (Eardley et al., 2010; Hatzimouratidis et al., 2010; Porst et al., 2013) har ett anmärkningsvärt bortfall från behandlingen med PDE5i nyligen rapporterats. I kvantitativa termer har en genomsnittlig avbrytningsfrekvens på 4% per månad rapporterats, med en total övergivande av behandlingen i 50% fall på årsbasis (Carvalheira et al., 2012; Corona et al., 2016). Bland de främsta orsakerna som patienterna ger för att motivera övergivandet av terapi kallas bristen på effekt och biverkningar som den vanligaste (Corona et al., 2016). Det kan särskiljas två typer av biverkningar: de som är strikt relaterade till PDE5-hämning, såsom huvudvärk, rodnad och dyspepsi, och de som är associerade med kvarvarande hämmande aktivitet av läkemedel på andra PDE, såsom vasodilatation och takykardi (PDE1), synstörningar (PDE6) och ryggsmärta (PDE11) (Bischoff, 2004; Gupta et al., 2005). Eftersom förekomsten av biverkningar ökar med både serumnivåer och tidsexponering för läkemedlet (Gupta et al., 2005; Taylor et al., 2009) kan säkerhets – /effektprofilen för ett läkemedel alternativt förbättras genom ett farmakokinetiskt tillvägagångssätt genom utformningen av en ny läkemedelsformulering (Mehrotra et al., 2007). Detta tillvägagångssätt har framgångsrikt tillämpats på PDE5i i fallet med Vardenafil. Faktum är att denna molekyl lider av en relativt låg biotillgänglighet (15% av 2003, centrum för läkemedelsutvärdering och forskning). Jämfört med den filmdragerade tabletten (FCT), den ursprungliga formuleringen för klassisk administrering per os, ökade formuleringen av oro-dispergerbara tabletter (ODT) för Vardenafil signifikant läkemedlets biotillgänglighet genom att gynna den sublinguala absorptionen, en väg som erkändes vara mindre påverkad av första-pass metabolism (Heinig et al., 2011).
Sildenafil (Sild) var den första selektiva PDE5-hämmaren godkänd för behandling av ED (Boolell et al., 1996). Det är en relativt lipofil molekyl och efter oral administrering uppnås maximal plasmakoncentration på en tid som varierar från 0,5 till 2 timmar. Sild visar en relativt låg oral biotillgänglighet (38-41%), främst på grund av omfattande tarm-och första passmetabolism (Gupta et al., 2005). Trots den långa närvaron på marknaden har utvecklingen av nya formuleringar av läkemedel dåligt drivit fram till den senaste utgåvan på den italienska marknaden av en ny formulering: den oro-dispergerbara filmen (ODF). Faktum är att ODF godkändes som en bioekvivalent form av FCT (Leoni et al., 2013). Emellertid kan Oralt sönderfallande formuleringar representera lämpliga system för att gynna trans-mukosal, och i synnerhet subspråkig absorption (Kathpalia och Gupte, 2013).
i denna studie utvärderade vi farmakokinetiken för Sild associerad med sublingual administrering av antingen ODF eller ODT, jämfört med FCT som original per os-formulering. För detta ändamål undersökte vi frisättnings-/permeationsprofilen för de olika Sild-formuleringarna genom in vitro-system som är specifikt utvecklade för att utvärdera trans-mukosal absorption av läkemedel. Dessutom kvantifierade vi serumprofilerna för Sild-farmakokinetiken efter administrering av per os FCT och sublingual ODT och ODF hos patienter med ED.
material och metoder
kemikalier och läkemedelsformuleringar
Hank ’ s balance salts solution pH 7.4 (HBSS), HEPES solution, bensanilid och Sild citrate köptes alla från Sigma–Aldrich (Milano, Italien). För att undvika eventuella förvirrande resultat som härrör från användningen av alternativa bioekvivalenta produkter som finns tillgängliga på marknaden användes följande produkter: Viagra( Pfizer, Milano, Italien), Viagra (Pfizer) och Rabestrom (Ibsa, Lodi, Italien). Läkemedel ordinerades till patienter under poliklinisk utvärdering för privat bruk. För in vitro-tester och in vivo-utvärdering av farmakokinetiken (se nedan) köptes läkemedel specifikt av personal som var involverad i studien på lokala apoteksfaciliteter och hanterades/lagrades sedan under optimala förhållanden.
Disaggregeringstest
in vitro-disaggregeringstesterna utfördes enligt European Pharmacopoeia (2016) med användning av Tablettnedbrytningstestaren (Sotax DT 2, kompletterande figur S1A), med användning av vatten som nedsänkningsvätska vid 37 0,5 0,5 C. tiden för disaggregering kontrollerades vid fullständig upplösning av doseringsformen. Fullständig sönderdelning definieras som det tillstånd där eventuella rester av enheten som finns kvar på testapparatens skärm eller vidhäftar skivans nedre yta är en mjuk massa som inte har någon påtagligt fast kärna. Tester utfördes i tre exemplar och resultaten rapporterades som medelvärde för standardavvikelse för genomsnittsvärde för den.
Upplösningstest
in vitro-läkemedelsupplösningstester utfördes enligt European Pharmacopeia . Upplösningstesterna utfördes med användning av en paddelapparat, paddelhastighet 50 rpm och HBSS pH 7,4 användes som upplösningsmediumvolym (900 ml vid 37 0,5 0,5 C).
under frisättningstesterna, 2 ml upplösningsmediumprov, vid 0, 2, 4, 6, 10, 20, 30, och 40 min, avlägsnades och filtrerades genom 0,45 kcal cellulosaestrar filter och därmed utspädes. Därefter utfördes Sild-kvantifiering genom högpresterande vätskekromatografi (HPLC)-UV. Den borttagna volymen ersattes varje gång med färskt medium. Tester utfördes i tre exemplar och resultaten rapporterades som medelvärde för standardavvikelse för genomsnittsvärde för den. Data normaliserades på läkemedelsinnehållet i formuleringen.
Trans-mucosal Permeation Test
Trans-mucosal permeation profil av Sild utvärderades in vitro med användning av en specifik anordning enligt Delvadia et al. (2012) ändras på lämpligt sätt. I korthet bestod anordningen i ett vertikalt diffusionssystem som presenterades av donator–mottagarkammare separerade av ett engångscellulosa–acetatmembran (pore 0,45 kcal). Donatorcellen innehöll 1,5 ml HBSS, medan mottagarkammaren var en del av en sluten recirkulationskrets på 30 ml inklusive volymerna av rör och behållare. Provtagning utfördes från mottagarens kammarreservoar vid tidsintervallen för 0, 5, 10, 20, 30, och 40 min och ersättas med en ekvivalent volym av färsk HBSS. Proverna analyserades med HPLC-UV för läkemedelsinnehåll (fej Asics et al., 2014). Data normaliserades på den högsta genomträngda Sild-koncentrationen som observerades för rent Sildcitrat. Tester utfördes i tre exemplar och resultaten rapporterades som medelvärde för standardavvikelse för genomsnittsvärde för den.
farmakokinetisk studie på frivilliga psykogena ED-patienter
studien genomfördes i enheten för andrologi och reproduktiv medicin (Universitetssjukhuset i Padova, Italien), mellan maj och September 2017, enligt Helsingforsdeklarationen under godkännande av Padova Universitetssjukhusets Etikutskott (protokollnummer 3982/AO/16 och successiva ändringar). För att undvika förvirrande resultat registrerades ämnen med psykogen ED eftersom den lägre förekomsten av organiska störningar associerar till ED (Ludwig och Phillips, 2014).
provstorleken beräknades för att uppnå en effektstorlek på minst 0,5 med en statistisk effekt på 0,8 och en signifikansnivå på 0,05 för en jämförelse med tre grupper (se effektkalkylator – enkelriktad oberoende ANOVA).
tjugo patienter (medelålder 31,4 5,7 år) inkluderades i följd genom frisläppande av undertecknat informerat samtycke. Patienter deltog i poliklinisk utvärdering och rapporterade den konsekventa oförmågan att få och upprätthålla erektion för tillfredsställande samlag under de senaste 6 månaderna eller mer. Efterföljande klinisk utvärdering utfördes hos alla patienter för att fastställa frånvaron av sjukdomar relaterade till ED, såsom diabetes mellitus, hypertoni, neurologisk störning och användning av antidepressiva medel. Diagnos av psykogen ED bekräftades genom uppfyllandet av ett indexpoäng < 26 vid administrationen av det internationella indexet för erektil funktion-15 (IIEF-15) frågeformulär (Lotti et al., 2016) och upprätthållandet av nattliga spontana erektioner, bedömd genom nattlig penis Tumescence och Styvhetsövervakning genom RigiScan Plus Styvhetsbedömningssystem (Dacomed, USA) i två på varandra följande nätter som tidigare beskrivits (Munoz et al., 1993; Caretta et al., 2005). Exklusions kriterier var diagnos av maligniteter, onormala hormonplasmanivåer (respektive luteiniserande hormon >8 UI/l, totalt testosteron <10, 4 nmol/l, tyrotropin >4, 5 mUI/l, prolaktin >20 ng/ml) och ökad intima-media tjocklek vid supra-aorta trunkar (>0.9 mm) och/eller cavernösa artärer (>0,3 mm), bedömd med färgdoppler-ultraljud som tidigare beskrivits (Caretta et al., 2005, 2009).
patienter gick med på att följa en enda dos, trevägs crossover öppen studie. Läkemedelsdoseringsschema rapporteras i Figur 1. Doseringen av Sild valdes som 50 mg, i överensstämmelse med tidigare rapporter om behandling av psykogen ED (Banner och Anderson, 2007). Patienterna ombads att inte ta några droger eller alkohol i 1 vecka före och under studiens gång. Vidare uppmanades patienterna under dagen för läkemedelsdosering att ha en fettfri frukost (ingen mjölk eller annan fet mat) minst 2 timmar före testet. FCT, betraktad som referensformulering, administrerades klassiskt per os genom att svälja den orala tabletten med ett glas vatten. För ODT och ODF instruerades patienterna att hålla formuleringen under tungan i 15 minuter utan antagande av vatten, följt av att svälja. Venösa blodprover samlades i standardrör (Vacutainer, BD Biosciences, Milano, Italien) vid 0, 5, 10, 15, 30, 60, 90, 120, och 240 min efter läkemedelsadministration. Kompensation genom kontinuerlig infusion av steril saltlösning utfördes. Efter doseringen hölls försökspersonerna tills blodprovtagningen slutfördes. Ett ytterligare bloduttag utfördes vid 24 timmar från dosering av kontrollskäl för att fastställa fullständig läkemedelsclearance. Som tvättperioder tilläts 7 dagar mellan en dosering och följande. Efter blodinsamling isolerades plasma omedelbart och lagrades vid -80 kcal C tills användning.
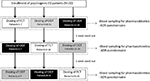
FIGUR 1. Doseringsschema och bedömningar för utvärdering av farmakokinetiska parametrar hos 20 patienter med psykogen erektil dysfunktion (ED), indelad i tre grupper (respektive patienter 1-7; patienter 8-14; och patienter 15-20). Varje patientgrupp fick alternativt per os Filmdragerad tablett (FCT), sublingual oro-dispergerbar tablett (ODT) eller sublingual oro-dispergerbar film (ODF) med minst 1 veckas tvätt från varje dosering. Alla formuleringar innehöll 50 mg sildenafil (Sild).
under bostaden ombads patienterna också att registrera biverkningar (ADR) i en specifikt utformad form, anpassad från ADR-rapporteringsformen för Agenzia Italiana del Farmaco (AIFA1). En översatt version av frågeformuläret finns som tilläggsmaterial (se Tilläggsdatablad S1). Patienterna ombads att ange typen av biverkningar, den totala intensiteten (i en subjektiv bedömningsskala från 1, mycket svag, till 5, mycket intensiv), tidpunkten för början och total varaktighet.
kvantifiering av Sildenafil i humant Serum
för kvantifiering av serumnivåer av Sild tillsattes 400 kg serumprov av 500 kg metanol kompletterat med den interna standarden (IS) bensanilid (5 kg/ml). Därefter tillsattes 5 ml etylacetat till blandningen, proverna vortexerades för att utföra flytande–flytande extraktion, de två faserna separerades genom centrifugering. Den organiska delen indunstades sedan under vakuumcentrifug vid 40 kcal C. Den erhållna återstoden löstes upp med 200 kg metanol och användes slutligen för högpresterande vätskekromatografi-tandem masspektrometri (HPLC-MS/MS) analys.
högpresterande vätskekromatografi-MS/MS-analys använde ett system Agilent-Varian 1260 och den tredubbla fyrdubbla detektorn Agilent-Varian 320 MS.Kromatografisk separation utfördes på en kolonn Phenomenex C-18 Evo 3 100, och en mobil fas bestående av acetonitril med 0,1% myrsyra i vatten med en gradient som beskrivs i kompletterande figur S2A. Ett positivt detekteringsläge applicerades för övergången 198 > 105 Da av IS, erhållen med en kapillärspänning på 40 V och en kollisionsenergi på 16 V medan 475 > 100 Da för Sild med kapillärspänning på 40 V respektive en kollisionsenergi på 22,5 V. Representativa kromatogram av IS och Sild i reella prover rapporteras i Tilläggsfigur S2B.
statistisk analys
farmakokinetiska parametrar (Pk), såsom maximal serumkoncentration (Cmax), tid till maximal serumkoncentration (Tmax) och area under kurvan (AUC) vid olika tidpunkter, beräknades med specifika rutiner för applikationer med GraphPad-programvara (La Jolla, CA, USA). Statistisk analys av data utfördes med SPSS 21.0 för Windows (SPSS, Chicago, IL, USA). Kolmogorov-Smirnov-testet användes för att kontrollera om distributionen var normal. Variabler som inte visar normalfördelning log transformerades. Baslinjeegenskaper hos patienter, PKs och data från in vitro-experiment jämfördes med oparade studenters T–test med Bonferroni-Holm-korrigering för multipla jämförelser. Upprepade åtgärder ANOVA utfördes för att testa skillnader i läkemedelsfrisättning och Sild-serumkoncentration. Levenes test användes för att testa variansens homogenitet mellan grupper. Om homogenitet av variansantagandet kränktes utfördes Welch-testet och respektive P-värde rapporterades. Andelen ADR jämfördes med det exakta testet för XB2. P-värden < 0.05 ansågs vara statistiskt signifikanta.
resultat
in Vitro-analys av frisättning/Permeation av Sildenafil från de olika Läkemedelsformuleringarna
dynamiken för frisättning och permeation av Sild från de tre läkemedelsformuleringarna undersöktes tidigare in vitro (Figur 2). Tiden för fullständig disaggregering för FCT, ODT och ODF utvärderades genom ett standardtest som beskrivs i European Pharmacopoeia (2016; Figur 2a). ODF visade den högsta tiden till uppdelning jämfört med både FCT och ODT (respektive P = 0,017 och P = 0,008).
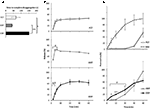
FIGUR 2. In vitro-utvärdering av biotekniska egenskaper hos FCT, ODT ochodf som innehåller 50 mg Sild. Resultaten är representativa för tre oberoende experiment och rapporteras som medelvärden för standardavvikelse för bord. A) resultat från disaggregeringstestet, rapportering av tiden (i sekunder) till fullständig disaggregering av formuleringen. Betydelse: mellan de angivna formuleringarna är p < 0,05 och p < 0,01. (B) resultat av upplösningstestet, som rapporterar mängden Sild som frigörs av varje formulering i procent av läkemedlets dosering. Betydelse: aP < 0,01 vs. FCT; bP < 0,001 vs. ODT. C) resultat från genomträngningstestet (beskrivs i avsnittet ”material och metoder”) som rapporterar mängden Sild som genomträngts genom ett cellulosaacetatmembran, i procent av det högsta värde som uppnåtts med 50 mg rent Sildpulver (diskontinuerlig linje i den övre panelen). Betydelse: PAC p < 0,05 vs. ODT; PAC p < 0,01 vs. ODT; PAC < 0,01 vs. FCT.
för att utvärdera påverkan av detta bevis på läkemedelsfrisättningen från formuleringen utfördes ett standardupplösningstest (European Pharmacopoeia, 2016; Figur 2B). Jämfört med referensformuleringen FCT visade ODT en snabbare frisättning av läkemedlet vars maximala utsträckning uppnåddes även efter endast 2 minuter från testets början (P = 0,006 vs. FCT). Å andra sidan var andelen läkemedel som släpptes från ODF inom de första 4 minuterna av analysen lägre jämfört med både FCT och ODT (respektive P = 0,004 och P < 0,001). I synnerhet visade ODF en mer progressiv frisättning av läkemedlet jämfört med FCT, vilket uppnådde maximal utsträckning efter 20 minuter från början av testet.
på grundval av detta bedömdes Trans-slemhinnepermeationen av Sild från varje formulering med en specifikt utvecklad anordning (figur 2C). För referensändamål utvärderades rent Sildcitrat, som användes i en vikt motsvarande 50 mg Sild, för trans-slemhinnepermeation och visade fri och snabb diffusion mellan de två kamrarna. En nästan motsatt profil observerades för FCT, vilket visar en försumbar permeation fram till 30 min från testets början. Genomträngningsprofilerna för ODT och ODF visade ett mellanliggande beteende jämfört med de två tidigare förhållandena. Inom de första 20 min av analysen visade ODF en signifikant högre grad av permeation jämfört med ODT (respektive P = 0,033 vid 5 min, P = 0,003 vid 10 min och P = 0,041 vid 20 min). Till skillnad från FCT och ODT som helt disaggregerades i givarkammaren kvarstod en kvarvarande mjukgelmassa av ODF på cellulosaacetatmembran även i slutet av analysen (kompletterande figur S2C).
differentiell Farmakokinetik för Sildenafil
tjugo manliga försökspersoner som drabbats av psykogen de accepterade att få alternativt FCT, ODT eller ODF, åtskilda av en veckas tvätt. Som beskrivs i avsnittet ”material och metoder” svaldes FCT klassiskt för att tillåta den klassiska per os-administrationen medan ODT och ODF bibehölls under tungan i 15 minuter för att främja den sublinguala vägen. Kliniska egenskaper hos patienter rapporteras i Tabell 1. Serumnivåer av Sild motsvarande de tre doseringsförhållandena rapporteras i Figur 3. En avsevärd variation innehöll läkemedelsserumprofilen för de tre formuleringarna. Jämfört med FCT visade ODT en uppenbar tidig ökning av Sild-serumnivåerna; denna trend var dock inte statistiskt signifikant. Å andra sidan observerades ett snabbare sönderfall av Sild-nivåer vid 120 och 240 min från dosering för ODT-formuleringen (respektive P = 0,044 och P = 0,024 vs. FCT).
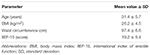
TABELL 1. Kliniska egenskaper hos studiedeltagarna (N = 20).
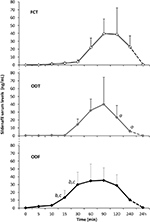
FIGUR 3. In vivo utvärdering av serumnivåer av Sild, hos 20 patienter som drabbats av psykogen ED, alternativt antingen FCT per os eller sublingual ODT eller sublingual ODF som beskrivs i avsnittet ”material och metoder.”Data rapporteras som medelvärden för standardavvikelse i genomsnitt: aP < 0,05 vs. FCT; bP < 0,01 vs. FCT; cP < 0,05 vs. ODT.
läkemedelsserumprofilen för ODF-formuleringen visade en snabbare ökning av Sild-nivåer jämfört med både FCT (P = 0, 001 och P = 0, 003) respektive ODT (P = 0, 048 respektive P = 0, 041) vid 15 respektive 30 min från dosering. I överensstämmelse med dess långsamma disaggregationstid in vitro (Figur 2B) var ODF–medelkoncentration-tidskurva in vivo mjukare än FCT och ODT (Figur 3).
farmakokinetiska parametrar för de tre formuleringarna, erhållna från analysen av Sild-serumnivåer, sammanfattas i Tabell 2. Trots att ingen signifikant skillnad observerades mellan de tre formuleringarna i termer av Cmax, Tmax och AUC0-240 min, visade ODF det lägsta värdet av Cmax (38,2 23,7 ng/ml) och det kortaste tmax (70,0 24,5 min). I synnerhet visade ODF ett signifikant högre värde av AUC0-60 min jämfört med både FCT och ODT (respektive P = 0,005 och P = 0.043), vilket resulterar i en ökad relativ biotillgänglighet av Sild inom den första timmen från dosering av ODF genom den sublinguala vägen.

TABELL 2. Farmakokinetiska parametrar för sildenafilformuleringar.
biverkningar
resultat erhållna från det självadministrerade frågeformuläret om typen och egenskaperna hos ADR som deltagarna upplevde sammanfattas i tabell 3. Bland de kända ADR rapporterade för Sild (Taylor et al., 2009) var de vanligaste registrerade huvudvärk, rodnad och nästäppa. En patient rapporterade låggradig muskelsmärta (grad 1 vid subjektiv bedömningsskala) efter dosering av FCT. Ingen av patienterna rapporterade förändrad syn, takykardi, svaghet eller förändrad hörsel.

TABELL 3. Biverkningar registrerade av studiedeltagarna (N = 20).
jämfört med FCT som referensformulering visade ODT oförändrad prevalens av ADR. Den personliga uppfattningen om spolningsintensitet var emellertid signifikant lägre (P = 0, 031). Å andra sidan visade ODF en minskad förekomst av huvudvärk jämfört med FCT (P = 0,043). Vidare uppfattades varaktigheten och intensiteten av spolning och nästäppa vid lägre nivåer jämfört med både FCT (respektive P = 0,011 och p = 0,015) och ODT (respektive P = 0,026 och P = 0,037).
diskussion
i denna studie ger vi bevis för att den sublinguala vägen för Sild-administrering associerar med en ökad tidig läkemedelsbiotillgänglighet och förbättrad toleransprofil. Detta bevis stöds av båda in vitro-undersökningarna, vilket visar att Sild-formuleringen Presenteras av en längre tid till disaggregation men signifikant gynnad trans-mukosal absorption och in vivo bevis.
fosfodiesterashämmare är det första valet terapeutiskt alternativ för behandling av ED; emellertid erkänns biverkningar som patienter upplever som den vanligaste orsaken till att behandlingen avbryts (Corona et al., 2016). Modifiering av farmakokinetik genom utformning av ny läkemedelsformulering kan representera en attraktiv strategi för att förbättra läkemedlets säkerhet/effektprofil (Mehrotra et al., 2007). I detta avseende gjorde 2013-patentet på Sild-citrat i flera europeiska länder möjlighet att släppa ut ett antal nya formuleringar av Sild. Det bör noteras att de flesta Sild-formuleringar som finns tillgängliga på marknaden idag faktiskt är godkända som bioekvivalenta former av den ursprungliga FCT (Leoni et al., 2013). Intressant är att Oralt sönderfallande formuleringar, som presenteras genom snabb uppdelning i patientens mun utan behov av att svälja med vatten, har utvecklats (Goel et al., 2008). Dessa nya formuleringar finner förbättrad efterlevnad hos de populationer av patienter med svårigheter att svälja konventionella fasta doser, såsom barn, geriatriska patienter och dysfagiska patienter. Dessutom, genom att tillhandahålla högre oral läkemedelstillgänglighet, kan Oralt sönderfallande formuleringar representera värderade system för att gynna trans-slemhinnor, och i synnerhet subspråkig absorption (Kathpalia och Gupte, 2013). Särskilt i Italien finns två Oralt sönderfallande formuleringar av Sild officiellt tillgängliga på apoteksfaciliteter: ODTs och ODFs.
i denna studie syftade vi till att utvärdera de möjliga farmakokinetiska variationerna och motsvarande mönster av ADR, som härrör från att gynna Trans-mukosal absorption av Sild genom subspråkig administrering av de två tillgängliga Oralt sönderfallande formuleringarna av läkemedlet. Resultaten jämfördes med den ursprungliga formuleringen av Sild, nämligen FCTs. Intressant nog fann vi en strikt korrelation, både in vitro och in vitro, mellan de biotekniska egenskaperna och PKs för de olika formuleringarna. I synnerhet, trots en lika läkemedelsdosering (50 mg) och något reducerad hastighet av läkemedelsfrisättning i upplösningstestet, kännetecknades ODF av en längre tid till disaggregering och högre permeationshastighet i trans-mukosalmodellen å ena sidan och av en ökad läkemedelsbiotillgänglighet inom den första timmen från doseringen å andra sidan. Vi kan då anta att subspråkig Sildabsorption gynnas av en långvarig kontakt med läkemedelsslemhinnan. Faktum är att detta fenomen i allmänhet bedrivs för orala trans-mukosala läkemedel, där användningen av mukoadhesiva polymerer rekommenderas för att säkerställa långvarig kontaktperiod mellan formuleringen och munslemhinnan (Lam et al., 2014), särskilt från dessa läkemedel, som Sild, som påverkas av låg vattenlöslighet (Zayed et al., 2012; Sun et al., 2014). Dessa preliminära resultat tyder också på en möjlig förbättring av den kliniska effekten för denna klass av läkemedel jämfört med ursprungliga formuleringar. Ytterligare studier är motiverade för att klargöra dessa aspekter.
det mest slående beviset på den aktuella studien är en signifikant minskning av biverkningarna av subspråkig administrering av ODF jämfört med ODT och FCT administrerat i samma dos, vilket i sin tur kan leda till ökad patienters efterlevnad. Detta bevis kan tolkas mot bakgrund av principen att förekomsten av en läkemedelsbiverkning ökar genom att öka serumnivåerna och exponeringstiden för själva läkemedlet (Gupta et al., 2005; Taylor et al., 2009). Trots en oförändrad Global biotillgänglighet jämfört med de andra analyserade formuleringarna visade den subspråkiga administreringen av ODF ett lägre värde av Cmax och en kortare tmax, vilket resulterade i en signifikant högre andel Sild bio-tillgänglig inom den första timmen från dosering. Således kan vi spekulera i att den subspråkiga administreringen av ODF kombinerar en effektiv absorption av läkemedlet med uppnåendet av genomsnittliga lägre serumnivåer av Sild och en därmed lägre risk för biverkningar. Vi erkänner dock den låga provstorleken som den största nackdelen med studien. Ytterligare undersökning av större kohorter och med olika doser krävs för att bekräfta detta problem.
Sammanfattningsvis rapporterar vi i denna studie att sublingual administrering av Sild ODF förbättrar läkemedelstoleransprofilen genom sannolikt involvering av en modifierad farmakokinetik jämfört med generator FCT. Även om ODF ursprungligen inte var tänkt för detta ändamål, representerar detta en attraktiv strategi för att förbättra patientens efterlevnad av terapi. Vi utvecklar ytterligare jämförande studier för att bedöma den kliniska effekten hos psykogena och organiska ED-patienter.
Författarbidrag
LDT och CF samordnade studien och utarbetade manuskriptet. MDRP utvärderade och registrerade patienterna. EF utförs in vitro-analys. SDA utförde serumanalysen. RP utförde farmakokinetikjämförelsen. RP, nr och AG reviderade och slutförde manuskriptet kritiskt.
intressekonflikt uttalande
författarna förklarar att forskningen genomfördes i avsaknad av kommersiella eller finansiella relationer som kan tolkas som en potentiell intressekonflikt.
bekräftelser
vi tackar Dr.Alberto Barosso, Dr. Giuseppe Maggioni och Dr. Dimitri Portale för patientrådgivning, Dr. Flavia Rosano och Dr. Alice Passadore för patienter som hanterar och all personal vid Enheten för andrologi och reproduktiv medicin.
tilläggsmaterial
Tilläggsmaterialet för denna artikel finns online på: https://www.frontiersin.org/articles/10.3389/fphar.2018.00059/full#supplementary-material
figur S1 / representativa bilder av tablettens Sönderdelningstestare (A) och Upplösningsapparaten (B) som används för disaggregeringstest respektive upplösningstest.
figur S2 |(a) detaljer om den mobila fasgradienten som används för högpresterande vätskekromatografi-tandem masspektrometri (HPLC-MS/MS) analys av serumnivåer av sildenafil (Sild). Representativa kromatogram och masspektra av både Sild vid den interna standarden bensanilid i verkliga prover rapporteras (B). C) representativ bild av kvarvarande orodispergerbar film (markerad med en diskontinuerlig linje) som kvarstår efter genomträngningstestet i den anordning som används för in vitro-uppskattning av trans-mukosal absorption genom ett cellulosaacetatmembran.
datablad S1 | frågeformulär för biverkningar.
fotnot
- ^http://www.aifa.gov.it/en/content/reporting-adverse-reaction
Banner, L. L. och Anderson, R. U. (2007). Integrerad sildenafil och kognitiv beteendesexterapi för psykogen erektil dysfunktion: en pilotstudie. J. Sex. Med. 4, 1117–1125. doi: 10.1111 / j. 1743-6109. 2007.00535.X
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Bischoff, E. (2004). Styrka, selektivitet och konsekvenser av icke-selektivitet av PDE-hämning. Int. J. Impot. Res Suppl. 1, S11-S14. doi: 10.1038 / sj.ijir.3901208
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Boolell, M., Allen, M. J., Ballard, S. A., Gepi-Attee, S., Muirhead, G. J., Naylor, A. M., et al. (1996). Sildenafil: en oralt aktiv typ 5 cyklisk GMP-specifik fosfodiesterashämmare för behandling av erektil dysfunktion i penis. Int. J. Impot. Res 8, 47-52.
PubMed Abstrakt / Google Scholar
Caretta, N., Palego, P., Ferlin, A., Garolla, A., Bettella, A., Selice, R., et al. (2005). Återupptagande av spontana erektioner hos utvalda patienter som drabbats av erektil dysfunktion och olika grader av karotidväggförändring: tadalafils Roll. EUR. Urol. 48, 326–331. doi: 10.1016 / j. eururo.2005.01.013
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Caretta, N., Palego, P., Schipilliti, M., Ferlin, A., Di Mambro, A. och Foresta, C. (2009). Cavernous artär intima-media tjocklek: en ny parameter vid diagnos av vaskulär erektil dysfunktion. J. Sex. Med. 6, 1117–1126. doi: 10.1111 / j. 1743-6109.2008. 01112.X
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Carvalheira, A. A., Pereira, N. M., Maroco, J. och Forjaz, V. (2012). Dropout vid behandling av erektil dysfunktion med PDE5: en studie om prediktorer och en kvalitativ analys av orsakerna till avbrytande. J. Sex. Med. 9, 2361–2369. doi: 10.1111 / j. 1743-6109.2012. 02787.X
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Centrum för läkemedelsutvärdering och forskning (2003). Nda 021400 Levitra (Vardenafilhydroklorid) tabletter: Klinisk Farmakologi / Biopharmaceutics Review. Rockville, Md: Institutionen för hälsa och mänskliga tjänster. Silver Spring, MD: Food and Drug Administration.
Google Scholar
Corona, G., Rastrelli, G., Burri, A., Serra, E., Gianfrilli, D., Mannucci, E., et al. (2016). Första generationens fosfodiesteras typ 5-hämmare dropout: en omfattande granskning och metaanalys. Andrologi 4, 1002-1009. doi: 10.1111 / andr.12255
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Delvadia, P. R., Barr, W. H. och Karnes, H. T. (2012). A biorelevant in vitro release/permeation system for oral transmucosal dosage forms. Int. J. Pharm. 430, 104–113. doi: 10.1016/j.ijpharm.2012.03.050
PubMed Abstract | CrossRef Full Text | Google Scholar
Eardley, I., Donatucci, C., Corbin, J., El-Meliegy, A., Hatzimouratidis, K., McVary, K., et al. (2010). Pharmacotherapy for erectile dysfunction. J. Sex. Med. 7, 524–540. doi: 10.1111/j.1743-6109.2009.01627.x
PubMed Abstract | CrossRef Full Text | Google Scholar
European Pharmacopoeia (2016). Europeiska direktoratet för läkemedelskvalitet & sjukvård (EDQM), 9: e Edn. Strasbourg: Europarådet.
Google Scholar
fej Ubics, I., Neumajer, G., B Ubicni, S. och Jankovics, P. (2014). Kvalitativ och kvantitativ analys av PDE-5-hämmare i förfalskade läkemedel och kosttillskott av HPLC-UV med sildenafil som enda referens. J. Pharm. Biomed. Anal. 98, 327–333. doi: 10.1016/j.jpba.2014.06.010
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Goel, H., Rai, P., Rana, V. och Tiwary, A. K. (2008). Oralt sönderdelningssystem: innovationer inom formulering och teknik. Senaste Pat. Drog Deliv. Formel. 2, 258–274. doi: 10.2174/187221108786241660
CrossRef fulltext / Google Scholar
Gupta, M., Kovar, A. och Meibohm, B. (2005). Den kliniska farmakokinetiken för fosfodiesteras-5-hämmare för erektil dysfunktion. J. Clin. Pharmacol. 45, 987–1003. doi: 10.1177/0091270005276847
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Hatzimouratidis, K., Amar, E., Eardley, I., Giuliano, F. Han var en av de mest kända. (2010). European Association of Urology. Riktlinjer för manlig sexuell dysfunktion: erektil dysfunktion och för tidig utlösning. EUR. Urol. 57, 804–814. doi: 10.1016 / j. eururo.2010.02.020
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Hawksworth, D. J. och Burnett, A. L. (2015). Farmakoterapeutisk hantering av erektil dysfunktion. Clin. Pharmacol. Där. 98, 602–610. doi: 10.1002 / cpt.261
PubMed Abstrakt / CrossRef Fulltext / Google Scholar
Heinig, R., Weimann, B., Dietrich, H., och B. Jacobttcher, M. F. (2011). Farmakokinetik för en ny munsönderfallande tablettformulering av vardenafil: resultat från tre kliniska prövningar. Clin. Läkemedel Investig. 31, 27–41. doi: 10.2165/11584950-000000000-00000
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Kathpalia, H. och Gupte, A. (2013). En introduktion till snabbupplösande orala tunnfilmsdrogleveranssystem: en recension. Curr. Drog Deliv. 10, 667–684. doi: 10.2174/156720181006131125150249
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Lam, JK, Xu, Y., Worsley, A. och Wong, IC (2014). Oral transmukosal läkemedelsleverans för pediatrisk användning. Adv. Drog Deliv. 73, 50-62. doi: 10.1016 / j. addr.2013.08.011
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Leoni, La, Leite, GS, Wichi, RB och Rodrigues, B. (2013). Sildenafil: två decennier av fördelar eller risker? Åldrande Hane 16, 85-91. doi: 10.3109 / 13685538.2013.801952
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Lotti, F., Corona, G., Castellini, G., Maseroli, E., Fino, M. G., Cozzolino, M., et al. (2016). Semenkvalitetsförsämring är förknippad med sexuell dysfunktion beroende på dess svårighetsgrad. Brum. Reprod. 31, 2668–2680. doi: 10.1093 / humrep / dew246
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Ludwig, W. och Phillips, M. (2014). Organiska orsaker till erektil dysfunktion hos män under 40 år. Urol. Int. 92, 1–6. doi: 10.1159/000354931
PubMed Abstrakt / CrossRef Fulltext / Google Scholar
Lugnier, C. (2006). Cyklisk nukleotidfosfodiesteras (PDE) superfamilj: ett nytt mål för utveckling av specifika terapeutiska medel. Pharmacol. Där. 109, 366–398. doi: 10.1016 / j. pharmthera.2005.07.003
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Mehrotra, N., Gupta, M., Kovar, A. och Meibohm, B. (2007). Rollen av farmakokinetik och farmakodynamik vid fosfodiesteras-5-hämmarbehandling. Int. J. Impot. Res 19, 253-264. doi: 10.1038 / sj.ijir.3901522
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Munoz, M., Bancroft, J. och Marshall, I. (1993). Rigiscans prestanda vid mätning av penis tumescence och styvhet. Int. J. Impot. Res. 5, 69-76.
Google Scholar
han är en av de mest kända och mest kända i världen. (2013). ISSM Standards Committee för sexuell medicin. Sop konservativ (medicinsk och mekanisk) behandling av erektil dysfunktion. J. Sex. Med. 10, 130–171. doi: 10.1111 / jsm.12023
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Sun, D., Wei, X., Xue, X., Fang, Z., Ren, M., Lou, H., et al. (2014). Förbättrad oral absorption och terapeutisk effekt av acetylpuerarin baserat på D-AA-tokoferyl polyetylenglykol 1000 succinat nanoemulsioner. Int. J. Nanomedicine 9, 3413-3423. doi: 10.2147/IJN.S63777
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Taylor, J., Baldo, O. B., Storey, A., Cartledge, J. och Eardley, I. (2009). Skillnader i biverkningsvaraktighet och relaterade störningsnivåer mellan fosfodiesteras typ 5-hämmare. BJU Int. 103, 1392–1395. doi: 10.1111 / j. 1464-410X.2008.08328.X
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Zayed, R., Kamel, A. O., Shukr, M. och El-Shamy, A. H. (2012). En jämförande studie in vitro och in vivo av direkt komprimerade fasta dispersioner och frystorkade sublinguala tabletter av sildenafilcitrat för hantering av pulmonell arteriell hypertoni. Acta Pharm. 62, 411–432. doi: 10.2478/v10007-012-0027-9
PubMed Abstract | CrossRef Full Text | Google Scholar