reaktion: hydrering af alkyner
som med alkener kræver hydrering (tilsætning af vand) til alkyner en stærk syre,normalt svovlsyre, og lettes af kviksølvsulfat. I modsætning til tilsætningerne til dobbeltbindinger, der giver alkoholprodukter, giver tilsætning af vand til alkyner ketonprodukter ( undtagen acetylen, der giver acetaldehyd ). Forklaringen på denne afvigelse ligger i Enol-keto tautomerisering, illustreret ved følgende ligning. Det oprindelige produkt fra tilsætningen af vand til en alkyn er en Enol (en forbindelse med en hydroksylsubstituent bundet til en dobbeltbinding), og dette omarrangeres straks til den mere stabile keto-tautomer.
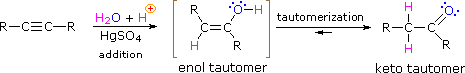
Tautomerer defineres som hurtigt interkonverterede forfatningsmæssige isomerer, der normalt skelnes af et andet bindingssted for et labilt hydrogenatom (farvet rødt her) og en forskelligt placeret dobbeltbinding. Ligevægten mellem tautomerer er ikke kun hurtig under normale forhold, men det favoriserer ofte stærkt en af isomererne ( acetone er for eksempel 99,999% keto tautomer ). Selv i sådanne ensidige ligevægte kommer bevis for tilstedeværelsen af den mindre tautomer fra forbindelsens kemiske opførsel. Tautomere ligevægte katalyseres af spor af syrer eller baser, der generelt er til stede i de fleste kemiske prøver. De tre eksempler vist nedenfor illustrerer disse reaktioner for forskellige substitutioner af triple-bond. Tautomeriseringstrinnet er angivet med en rød pil. For terminale alkyner følger tilsætningen af vand Markovnikov-reglen, som i det andet eksempel nedenfor, og slutproduktet ia en methylketon ( undtagen acetylen, vist i det første eksempel ). For interne alkyner (triple-bindingen er inden for en længere kæde ) er tilsætningen af vand ikke regioselektiv. Hvis triple-bindingen ikke er symmetrisk placeret ( dvs.hvis R & R’ i den tredje ligning ikke er den samme ) dannes to isomere ketoner.
HC-CH + H2O + HgSO4 & H2SO4 –> –> H3C-CH=O
RC-CH + H2O + HgSO4 & H2SO4 –> –> RC(=O)CH3
RC-CR’ + H2O + HgSO4 & H2SO4 –> –> RCH2-C(=O)R’ + RC(=O) – CH2R’
med tilsætning af vand kan alkyner hydreres til dannelse af enoler, der spontant tautomeriseres til ketoner. Reaktionen katalyseres af kviksølvioner. Følger Markovnikovs regel: Terminale alkyner giver methylketoner
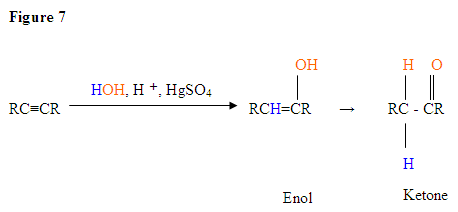
- det første trin er en syre / base-reaktion, hvor Triple-elektronerne i triple-bindingen fungerer som en uvis-base og angriber protonen, der derfor protinerer carbonet med de fleste hydrogensubstituenter.
- det andet trin er angrebet af det nukleofile vandmolekyle på den elektrofile carbokation, som skaber en oksoniumion.
- dernæst deprotonerer du af en base og genererer en alkohol kaldet Enol, som derefter tautomeriseres til en keton.
- tautomerisme er en samtidig proton-og dobbeltbindingsskift, der går fra enolformen til keto-isomerformen som vist ovenfor i Figur 7.
lad os nu se på nogle Hydratiseringsreaktioner.
hydrering af Terminal Alkyne producerer methylketoner
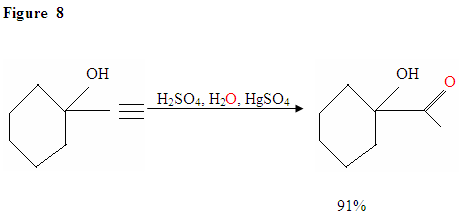
ligesom beskrevet i Figur 7 vil de primære elektroner angribe en proton og danne en carbocation, som derefter bliver angrebet af de nukleofile vandmolekyler. Efter deprotination genererer vi en enol, som derefter tautomeriseres i den viste ketonform.
hydrering af Alkyne
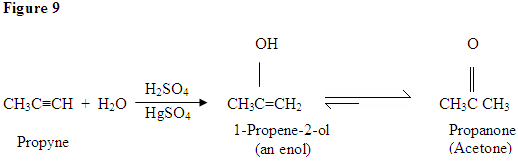
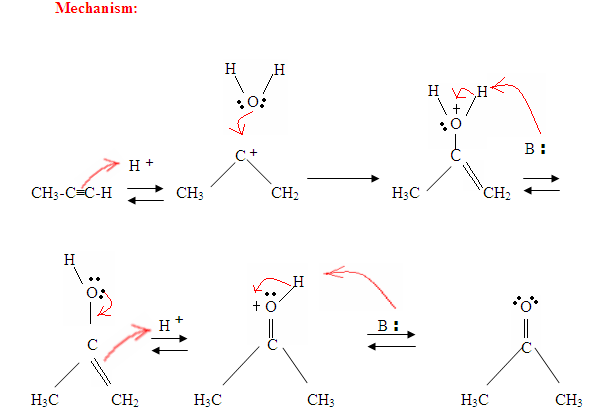
som du kan se her, angriber Triple-elektronerne i den tredobbelte binding protonen, som danner en kovalent binding på carbonet med de fleste hydrogensubstituenter. Når brintet er bundet, har du en carbocation, som bliver angrebet af vandmolekylet. Nu har du en positiv ladning på iltet, hvilket resulterer i, at en base kommer ind og deprotinerer molekylet. Når du er deprotineret, har du en enol, som derefter bliver tautomeriseret.
tautomerisme er vist her, når protonen bliver angrebet af dobbeltbindingen, der danner en kovalent binding mellem kulstof og brint på det mindre substituerede kulstof. Elektroner fra iltet ender med at bevæge sig til kulstof, danner en dobbeltbinding med kulstof og giver sig selv en positiv ladning, som derefter bliver angrebet af basen. Basen deprotinerer iltet, hvilket resulterer i det mere stabile slutprodukt ved ligevægt, som er en keton.
øvelse \(\Sideindeks{1}\)
- tegn strukturen af det dannede produkt, når hvert af nedenstående stoffer behandles med H2O/H2SO4 i nærværelse af HgSO4.
- $ \ ce {\sf{CH3-CH2-C#C-H}}$
-
- tegn strukturen af ketoformen af forbindelsen vist nedenfor. Hvilken form ville du forvente at være den mest stabile?
svar
svar:

spørgsmål 9.4.2
foreslå en reaktionsplan for følgende forbindelse, der starter fra alkynet og viser krævede reagenser og mellemprodukter.

Løsninger
S9.4.1

S9.4.2
