Pancreascyster repræsenterer en lille, men stadig mere detekteret enhed af pancreasabnormiteter. 70% af cystiske læsioner i bugspytkirtlen opdages tilfældigt. De hyppigst forekommende neoplastiske bugspytkirtelcyster inkluderer intraduktal papillær mucinøs neoplasma (IPMN), serøs cystadenom (SCA), mucinøs cystisk neoplasma med ovariestroma (MCN) og fast pseudopapillær epitel-neoplasma. IPMN er yderligere opdelt i grenkanal (BD), hovedkanal og kombinerede former. Tilsammen udgør disse 90% af premalign pancreas, primært cystiske tumorer. I modsætning hertil har pseudocyst, ægte epitelcyst, lymfoepitelial cyste og mucinøs ikke-neoplastisk cyste intet malignt potentiale.
malignitet forekommer kun i mucinøse cyster. SCA betragtes som en ikke-malign læsion, og ondartede serøse tumorer rapporteret i litteraturen har ikke vist sig at opfylde hvem-kriterierne for SCN. IPMN kan udvikle sig fra lavere til højere grader af dysplasi og i sidste ende pancreasduktalt adenocarcinom (PDAC). Ipmn ‘er, der involverer hovedkanalen, har en højere malignitetsrate end dem i grenene, med risikoen for malignitet anslået til at være 62%; risikoen for malignitet af MCN’ er er mindre end 15%. Andre, sjældnere cystiske læsioner, såsom fast pseudopapillær epitel-neoplasma og cystisk pankreatisk neuroendokrin tumor (cPNET), har tendens til at have funktioner, der antyder en specifik diagnose, som normalt fører til kirurgisk fjernelse.
for at undersøge hyppigheden af tilfældige bugspytkirtelcyster hos asymptomatiske individer udførte Kromrey en magnetisk resonans cholangiopancreatography (MRCP) undersøgelse hos 1077 deltagere tilmeldt en populationsbaseret kohortestudie. Af den oprindelige gruppe gennemgik 676 personer en gentagelsesundersøgelse 5 år senere. På tidspunktet for den indledende undersøgelse havde 49% mindst en cyste på 2 mm i diameter. Forekomsten af nye cyster i opfølgningsperioden var 2,6% om året. Cyste tilstedeværelse var stærkt relateret til alder; ved 75 år havde 75% af deltagerne en eller flere cyster. Diskriminationen mellem godartede og premaligne eller ondartede bugspytkirtelcyster er af stor betydning for at undgå unødvendige procedurer, såsom radiologiske opfølgningsundersøgelser eller kirurgisk resektion.
mucinøs cystisk neoplasma med ovariestroma (MCN)
MCN ‘ er er almindelige hos middelaldrende kvinder, er normalt veldefinerede og er overvejende i halen i bugspytkirtlen (> 90%). Sammenlignet med serøse cystiske tumorer er MCN ‘ er større (>20 mm i diameter) og mindre talrige (normalt < 6). Den biologiske opførsel af MCN ‘ er er variabel, og forskellige histologiske mønstre eksisterer ofte sammen i den samme tumor. Tumorerne kan være helt godartede, ligesom mucinøse cystadenomer eller intraduktale papillære mucinøse adenomer. Nogle tumorer er borderline, der viser cellulær dysplasi, mens andre er ærligt ondartede. Malignt cystadenocarcinom og intramedullære mucinøse carcinomer kan yderligere opdeles i ikke-invasive og invasive typer.
(de radiologiske egenskaber ved MCN ‘ er er demonstreret på billederne nedenfor.)
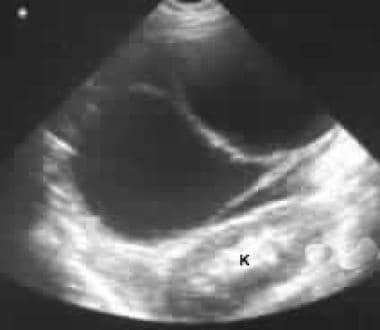 Sonogram gennem venstre hypokondrium viser en stor septatmasse foran nyrerne (K).
Sonogram gennem venstre hypokondrium viser en stor septatmasse foran nyrerne (K). 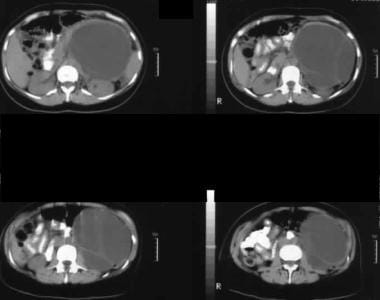 ikke-forbedrede aksiale CT-scanninger. Billede 1 viser en stor septatmasse i venstre hypokondrium. Bemærk den glatte ydre kontur, der er typisk for en mucinøs cystisk neoplasma.
ikke-forbedrede aksiale CT-scanninger. Billede 1 viser en stor septatmasse i venstre hypokondrium. Bemærk den glatte ydre kontur, der er typisk for en mucinøs cystisk neoplasma. intraduktal papillær mucinøs neoplasma (IPMN)
på grundlag af involvering af bugspytkirtelkanalen klassificeres Ipmn ‘ er som enten hovedkanal IPMN, sidegren IPMN eller blandet variant IPMN, der involverer både hovedpankreatisk kanal og sidegrenene. Ipmn ‘er med hovedkanal har ofte epitel af tarmtype, og ipmn’ er med sidegren har normalt epitel af gastrisk type. Selvom alle morfologiske varianter af IPMN kan udvikle sig til kræft, invasivt adenocarcinom med oprindelse i gastrisk Type IPMNs er forbundet med en signifikant dårligere overlevelsesrate end den, der stammer fra andre typer IPMNs. Imidlertid, billeddannelsesfunktionerne er ikke specifikke til differentiering af de forskellige histologiske varianter af Ipmn ‘ er.
sidegren Ipmn ‘ er opdages almindeligvis hos ældre mænd og er hyppigere placeret i den proksimale bugspytkirtel (hoved og uncinate proces). En vigtig differentierende funktion mellem MCN og IPMN er visualisering af pancreas ductal kommunikation. Hvis en klar kommunikationskanal med bugspytkirtelkanalen visualiseres, er diagnosen sidegren IPMN næsten sikker, fordi SCAs og MCN ‘ er ikke kommunikerer med bugspytkirtelkanalsystemet.
på trods af den lave forekomst af aggressivitet af slimhindecystiske læsioner 3 cm og mindre er forekomsten ikke lav nok til at afvise læsionerne helt, og omhyggelig gennemgang af billeddannelsesfunktionerne er mandat. Derudover har patienter, hvis tilstand viser sig ikke at være egnet til kirurgisk behandling, ofte brug for hyppige vurderinger for vækst og ændring i billeddannelsesfunktioner.
(Ipmn ‘ er ses på billederne nedenfor.)
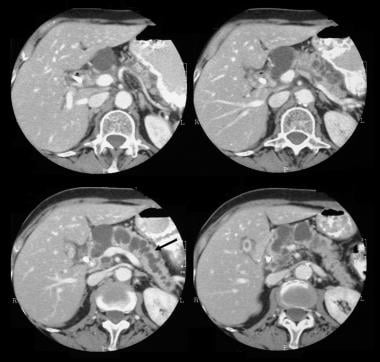 pancreas intraduktal papillær mucinøs tumor (IPMT). Kontrastforstærkede aksiale CT-scanninger gennem bugspytkirtlen viser en 5,5 cm cystisk tumor i bugspytkirtelhovedet. Bemærk opstrøms, grov dilatation af bugspytkirtelkanalen. Tilbehørspankreatisk kanal er også udvidet.
pancreas intraduktal papillær mucinøs tumor (IPMT). Kontrastforstærkede aksiale CT-scanninger gennem bugspytkirtlen viser en 5,5 cm cystisk tumor i bugspytkirtelhovedet. Bemærk opstrøms, grov dilatation af bugspytkirtelkanalen. Tilbehørspankreatisk kanal er også udvidet. 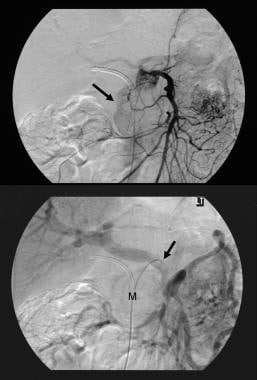 pancreas intraduktal papillær mucinøs tumor (IPMT). (Top) overlegen mesenterisk angiogram viser kapillær vaskularitet i massen i bugspytkirtelhovedet i den arterielle fase. (Nederst) billedet af portalens venøse fase viser forskydning af portalens venøse grene og indkapsling af krydset mellem den overlegne mesenteriske vene og portalvenen. M betegner bugspytkirtelmassen.
pancreas intraduktal papillær mucinøs tumor (IPMT). (Top) overlegen mesenterisk angiogram viser kapillær vaskularitet i massen i bugspytkirtelhovedet i den arterielle fase. (Nederst) billedet af portalens venøse fase viser forskydning af portalens venøse grene og indkapsling af krydset mellem den overlegne mesenteriske vene og portalvenen. M betegner bugspytkirtelmassen. 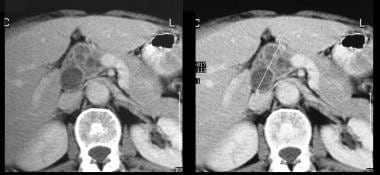 pancreas intraduktal papillær mucinøs tumor (IPMT). Kontrastforstærkede aksiale CT-scanninger gennem bugspytkirtlen viser en multiseptat tumor i hovedet af bugspytkirtlen.
pancreas intraduktal papillær mucinøs tumor (IPMT). Kontrastforstærkede aksiale CT-scanninger gennem bugspytkirtlen viser en multiseptat tumor i hovedet af bugspytkirtlen. 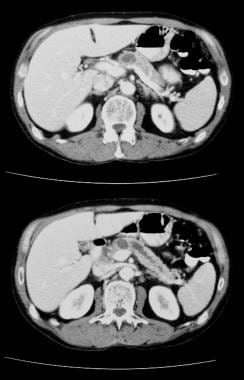 pancreas intraduktal papillær mucinøs tumor (IPMT). Kontrastforstærkede CT-scanninger gennem bugspytkirtlen viser grov dilatation af bugspytkirtelkanalen. Ved operationen blev IPMT bekræftet.
pancreas intraduktal papillær mucinøs tumor (IPMT). Kontrastforstærkede CT-scanninger gennem bugspytkirtlen viser grov dilatation af bugspytkirtelkanalen. Ved operationen blev IPMT bekræftet. serøse cystadenomer
serøse cystadenomer (mikrocystiske adenomer) (se billederne nedenfor) er de næst mest almindelige cystiske tumorer i bugspytkirtlen. Den kliniske præsentation af serøse cystadenomer svarer til den for mucinøse cystiske bugspytkirteltumorer.
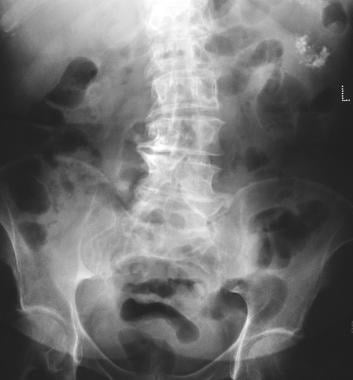 Mikrocystisk adenom i bugspytkirtlen. Almindelig røntgenbillede viser tumorforkalkning i et mikrocystisk adenom (venstre øvre kvadrant). Forkalkning i det mikrocystiske adenom præsenterer som en central klynge arrangeret i et sunburst-eller stellatarrangement. Central forkalkning vurderes bedre med CT end med radiografi.
Mikrocystisk adenom i bugspytkirtlen. Almindelig røntgenbillede viser tumorforkalkning i et mikrocystisk adenom (venstre øvre kvadrant). Forkalkning i det mikrocystiske adenom præsenterer som en central klynge arrangeret i et sunburst-eller stellatarrangement. Central forkalkning vurderes bedre med CT end med radiografi. 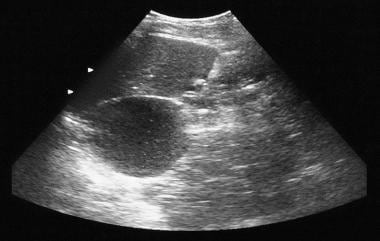 pankreatisk mikrocystisk adenom. Sonogram viser en cystisk masse i området af halen af bugspytkirtlen.
pankreatisk mikrocystisk adenom. Sonogram viser en cystisk masse i området af halen af bugspytkirtlen. 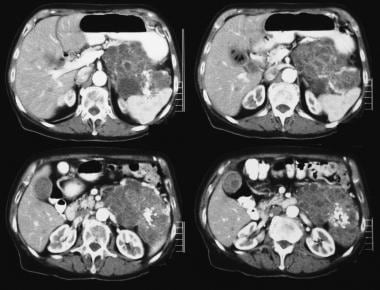 pankreatisk mikrocystisk adenom. Kontrastforstærkede aksiale CT-scanninger viser en hypervaskulær tumor i bugspytkirtlen med forkalkning af sunburst. Bemærk den svenske osteforøgelse.
pankreatisk mikrocystisk adenom. Kontrastforstærkede aksiale CT-scanninger viser en hypervaskulær tumor i bugspytkirtlen med forkalkning af sunburst. Bemærk den svenske osteforøgelse. på grund af stigende brug af tværsnitsbilleddannelse opdages mange af disse tumorer som et tilfældigt, asymptomatisk fund.
på tværsnitsbilleder vises serøse cystadenomer som adskillige små cyster adskilt af delikat fibrøs septa, som giver dem et bikageudseende. Cysterne er fyldt med klar, vandig væske og er ofte arrangeret omkring et centralt stellatarr, som kan forkalkes. Ved CT-scanninger er Sunburst central forkalkning i en svampet masse patognomonisk for denne tumor, men dette fund forekommer hos kun 10% af patienterne.
endoskopisk ultralyd (EUS) tillader bedre opløsning af bikagestrukturen end CT. Til tider kan cysterne være store, en funktion, der gør det vanskeligt at differentiere disse cyster fra MCN ‘ er.
Hypervaskularitet kan påvises på angiogrammer, og nogle tumorer forekommer med intra-abdominal blødning.
differentielle diagnoser
pankreatisk pseudocyst-eller bugspytkirtelvæskesamlinger
Væskesamlinger forekommer i så mange som 50% af tilfældene med akut pancreatitis. Pseudocyster ses normalt som anekoiske væskerum på sonogrammer, men de kan vise interne ekkoer, hvis de indeholder nekrotisk væv eller blodprop.
billeddannelsesresultater, der antyder en diagnose af pseudocyst snarere end af cystisk neoplasma, inkluderer følgende: mangel på septae, lokaliseringer, faste komponenter eller cystevæg forkalkninger på computertomografi (CT) scanninger; hypovaskularitet på angiogrammer; og kommunikation mellem cyste og bugspytkirtelkanaler på endoskopisk retrograd cholangiopancreatografi (ERCP). De fleste pseudocyster er ekstrapancreatiske, mens cystiske neoplasmer i bugspytkirtlen er intrapancreatiske.
pankreatisk abscess
pancreatisk abscess er normalt sekundær til infektion af en pseudocyst, men i sjældne tilfælde kan den forekomme som et resultat af direkte spredning fra nyre-eller koloninfektion. Typisk forekommer en bugspytkirtelabces 2-4 uger efter en episode af akut pancreatitis.
på billeder kan disse abscesser ligne pseudocyster. Generelt afhænger udseendet af deres alder. I den akutte fase kan ændringerne være subtile med kun tab af normal bugspytkirtelkontur forbundet med udslettelse af bugspytkirtelkonturen og de peripancreatiske vaskulære og andre bløde vævsrum. Disse ændringer kan ikke skelnes fra dem, der findes i svær akut pancreatitis. I de subakutte og kroniske stadier, når central nekrose forekommer, ses der normalt en anekoisk eller kompleks cystisk masse. Et affaldsniveau kan observeres i den afhængige del af abscessen. I den subakutte eller kroniske fase er gennem transmission normalt god, undtagen når der er gas i abscessen. I nærvær af gas kan abscessen blive ekkogen og kan skygge.
væggene i subakut og kronisk pankreatisk abscess har variable træk. Væggene kan være tykke, uregelmæssige og veldefinerede, eller abscessen kan slet ikke have nogen definerbar væg. De sonografiske fund er uspecifikke, men i den passende kliniske indstilling kan en diagnose af en abscess foreslås og bekræftes ved hjælp af perkutan aspiration eller CT.
parasitære cyster
Echinococcus granulosis cyster og multilocularis cyster i bugspytkirtlen er blevet beskrevet, selvom bugspytkirtelinddragelse er usædvanligt sjælden. E. granulosecyster kan være unilokulære, multilokulære eller komplekse cystiske.
ved billeddannelse alene er differentiering af disse og andre cystiske masser vanskelig. Serologiske tests kan være nyttige i passende kliniske omgivelser. E. multilocularis cyster viser et ekkogent infiltrativt mønster. Denne diagnose skal underholdes i endemiske regioner, når et sådant mønster ses.
faste og papillære epitheliale bugspytkirteltumorer
FAST og papillær epitel-neoplasma i bugspytkirtlen kan være fast eller cystisk. Disse er sjældne tumorer, der ofte forveksles med mucin-udskillende tumorer eller ikke-fungerende adenomer.
faste og papillære epitheliale bugspytkirteltumorer er oftest placeret i bugspytkirtlen. De er store, godt indkapslede masser med områder med blødning og nekrose. På sonogrammer fremstår de som heterogene, runde, faste masser med et cystisk nekrotisk center og dystrofisk forkalkning, som kan skygge.
Dysontogene cyster
Dysontogene cyster er hamartomatøse cyster, der ofte er forbundet med nyrecyster, cerebellare angiomer og encephaloceler. Imaging afslører en stor, tyndvægget cyste med en morbærkonfiguration.
Pseudoaneurysmer
Pseudoaneurysmer er normalt ikke rigtig intrapancreatiske, og de kan forveksles med en bugspytkirtelcyst. Disse aneurismer er en komplikation af pancreatitis hos 3,5-10% af patienterne. Doppler-sonografi kan vise turbulent arteriel strømning inden for en pseudoaneurysm, hvorimod farvestrømsdoppler-sonografi viser tovejsstrøm og hvirvler inden i den anekoiske masse. Doppler-billeddannelse kan muliggøre foreløbig identifikation af arterien, der fodrer pseudoaneurysmen.
Retroperitoneal neurofibroma eller schvannoma
disse tumorer kan være hyperekoiske eller hypoechoiske/cystiske læsioner med sporadiske indre ekkoer. Dette er et almindeligt træk ved større tumorer, hvor cystisk degeneration og blødning er forekommet. Tumorerne er retroperitoneale, men kan efterligne bugspytkirtelmasser.
pancreas sarkom
pancreas sarkom er en sjælden tumor i de mesenkymale understøttende strukturer i bugspytkirtlen. Det er en relativt sonolucent masse og kan forveksles med en væskeopsamling eller pseudocyst. Sonografiske resultater kan være normale, eller sonogrammer kan demonstrere en retroperitoneal masse, som er relativt sonolucent sammenlignet med de omgivende væv. Derfor kan denne læsion forveksles med en cystisk bugspytkirtelmasse.
Pancreaslymfom
primært pancreaslymfom er sjældent. Den kliniske præsentation er ikke ulig den for bugspytkirtelkarcinom. Sonografi kan afsløre en homogen, sonolucent eller kompleks masse. Disse masser er normalt ekko-fattige og kan efterligne cystiske læsioner. Da prognosen for et bugspytkirtellymfom er gunstigt, er dets differentiering fra et karcinom afgørende. Korrelationen mellem sonografiske, CT og angiografiske fund kan resultere i en korrekt diagnose. Men hvis der er tvivl, kan sonografi-styret biopsi afsløre massens sande natur.
Acinarcellekarcinom i bugspytkirtlen
Pancreascellekarcinomer (PACC ‘ er) udgør cirka 1% af eksokrine bugspytkirteltumorer. PACC er en epithelial neoplasma med tegn på acinar differentiering. Patienter med acinarcellekarcinom har en bedre prognose end patienter med adenocarcinomer af duktaltypen, men en dårligere prognose end patienter med endokrine tumorer i bugspytkirtlen. På CT er PACC blevet beskrevet på forskellige måder, herunder som en dårligt defineret tæt masse; som en veldefineret masse med central nekrose; og som en cystisk masse omgivet af en tyk hypervaskulær væg.
foretrukken undersøgelse
MR er den foretrukne teknik til diagnose af cystiske bugspytkirteltumorer. MR ‘ er er normalt nyttige til at skelne mellem pseudocyster og cystiske neoplasmer. Magnetisk resonans cholangiopancreatography (MRCP) kan skildre galde-og bugspytkirtelkanalanatomi ikke-invasivt, og det hjælper med at diagnosticere intraduktale tumorer.
ultrasonografi er generelt den første teknik hos en patient med epigastriske symptomer. Dette er en fremragende modalitet til diagnosticering af cystiske bugspytkirtelmasser. Sonografi giver også mulighed for guidet intervention, såsom aspiration og biopsi. Doppler-sonografi giver en ekstra fordel ved evalueringen af hypervaskulære tumorer og vaskulær trombose/okklusion forbundet med bugspytkirteltumorer. Ekko-forbedret effekt Doppler-sonografi har høj følsomhed og specificitet i den differentielle diagnose af bugspytkirteltumorer.
i tvetydige tilfælde eller i tilfælde, hvor malignitet er stærkt mistænkt, giver EUS-FNA det bedste diagnostiske udbytte, da det tillader erhvervelse af cytologiske prøver og cystisk væske til analyse af forskellige tumormarkører.
lejlighedsvis, på trods af fuldstændig evaluering af en cystisk masse, kan typen af cyste forblive ubestemt. Selvom dyre og invasive, laparoskopisk sonografi, biopsi af cystevæggen og analyse af det cystiske aspirat bidrager væsentligt til den differentielle diagnose af cystiske læsioner i bugspytkirtlen.
CT viser tumorforkalkning og er en fremragende modalitet til påvisning af lokale og fjerne metastaser. Selvom CT og MR ikke kan bruges til at differentiere mucinindhold fra bugspytkirtelsaft, er kommunikation mellem den cystiske læsion og den udvidede MPD og en svulmende papilla med en patuløs åbning karakteristika ved IPMT. Den interne arkitektur af slimhindetumorer vises mindst lige så godt på MR-scanninger som på CT-scanninger med undtagelse af forkalkning inden for læsionen (som MR kun har en begrænset evne til at afsløre).
Spiral og/eller multisektion CT er fremragende teknikker til billeddannelse af bugspytkirtlen, hvilket giver fremragende rumlig opløsning og anatomiske detaljer. Med tynd kollimation og arterielle og venøse faser og multiplanære og/eller 3-dimensionelle (3D) rekonstruktioner er fremragende detaljer i den vaskulære anatomi afbildet; de fleste centre bruger nu sjældent angiografi til at vurdere bugspytkirteltumorer.
almindelige røntgenbilleder opnås ofte for at se efter forkalkning i bugspytkirtlen. Øvre GI-bariumundersøgelser kan udføres i sammenhæng med epigastrisk smerte. Med bugspytkirteltumorer kan bariumundersøgelser skildre ekstrinsisk forskydning af maven og tolvfingertarmen.
begrænsninger af teknikker
MR er ikke universelt tilgængelig, er dyr og udgør et problem for patienter med klaustrofobi. ACG-retningslinjerne anbefaler forsigtighed, når du bruger billeddannelse til at diagnosticere cystetype eller samtidig malignitet; nøjagtigheden af MR eller MRCP ved diagnosticering af cystetype er 40-50% og er 55-76% ved bestemmelse af godartede vs. ondartede tumorer.
Visceral gas, patient habitus og operatørafhængighed begrænser værdien af sonografi. Laparoskopisk ultralyd er invasiv. EUS-billeddannelse kan ikke pålideligt skelne godartet fra ondartet IPMNs, og det er uklart, om billeddannelsesfunktioner ved slimhindelæsioner med øget malignt potentiale er tilstrækkeligt forudsigelige til at påvirke klinisk behandling. Når kirurgisk histologi anvendes som referencestandard, varierer den diagnostiske nøjagtighed af EUS-billeddannelse fra 40 til 96%. En enkelt prospektiv undersøgelse viste, at følsomheden (56%) og specificiteten (45%) af EUS-morfologi alene til differentiering af mucinøse cyster (mucinøse cystiske neoplasmer og IPMNs) fra ikke-mucinøse cyster var lave, hvilket resulterede i dårlig samlet nøjagtighed (51%).
almindelige røntgenbilleder og øvre GI-bariumundersøgelser er uspecifikke, og lignende fund kan forekomme i en række patologier. CT bærer en betydelig ioniserende strålingsbyrde og bruger joderet kontrastmateriale med risiko for anafylaksi og nefrotoksicitet.
tværsnitsundersøgelser, herunder ultralyd, CT og MR, kan ikke bruges til at skelne mellem slimhindigt cystadenom og cystadenocarcinom, medmindre tumoren har metastaseret eller invaderet naboorganer. Angiografi er uspecifik og invasiv. Det kræver også joderet kontrastmedium med risiko for anafylaksi og nefrotoksicitet.
Opfølgningsbilleddannelse
ACG-retningslinjer anbefaler, at cysteovervågning tilbydes kirurgisk fit kandidater med asymptomatiske cyster, der formodes at være IPMNs eller MCNs. Alle kirurgisk resekterede Ipmn ‘er kræver postoperativ overvågning, men resekterede MCN’ er uden kræft i bugspytkirtlen gør det ikke. MRCP er den foretrukne modalitet til overvågning; EUS kan også være det primære overvågningsværktøj, når MR-scanninger er kontraindiceret. I mangel af vedrørende funktioner, der berettiger øget overvågning eller henvisning til yderligere evaluering, cystestørrelse styrer overvågningsintervaller for formodede IPMNs og MCNs.
retningslinjer
retningslinjer for diagnose og håndtering af bugspytkirtelcyster er blevet offentliggjort af følgende organisationer:
-
American College of Gastroenterology (ACG)
-
europæisk studiegruppe om cystiske tumorer i bugspytkirtlen
-
American College of Radiology (ACR)
ACG-retningslinjerne fra 2018 anbefaler magnetisk resonansbilleddannelse (MRI) eller magnetisk resonans cholangiopancreatography (MRCP) som den foretrukne diagnostiske modalitet på grund af deres ikke-invasivitet, mangel på stråling og større nøjagtighed i vurderingen af kommunikation mellem hovedpankreatisk kanal og cyste (som er et kendetegn ved sidegren IPMNs). Pancreasprotokol computertomografi (CT) eller endoskopisk ultralyd (EUS) blev betragtet som “fremragende alternativer”, hvis MR er kontraindiceret. EUs finnålsaspiration (FNA) og cystevæskeanalyse bør overvejes i cyster, hvor diagnosen er uklar, og hvor resultaterne sandsynligvis vil ændre behandlingen.
analyse af cystevæske CEA kan anses for at differentiere IPMNs og MCNs fra andre cystetyper, men det kan ikke bruges til at identificere IPMNs og MCNs med høj grad af dysplasi eller kræft i bugspytkirtlen. IPMNs eller MCNs med en af følgende funktioner skal gennemgå EUS med eller uden FNA og/eller henvises til en tværfaglig gruppe til yderligere evaluering :
-
et af følgende symptomer eller tegn: gulsot sekundært til cysten, akut pancreatitis sekundært til cysten, signifikant forhøjet serum CA 19-9
-
enhver af følgende billeddannelsesresultater: tilstedeværelsen af en vægmaleriknude eller fast komponent enten i cysten eller i bugspytkirtlen parenchyma, udvidelse af hovedpankreatisk kanal på >5 mm, en fokal udvidelse af bugspytkirtelkanalen, der vedrører hovedkanalen IPMN eller en hindrende læsion eller mucinproducerende cyster, der måler 3 cm i diameter
-
tilstedeværelsen af høj grad dysplasi eller kræft i bugspytkirtlen på cytologi
de europæiske retningslinjer fra 2018 anbefaler også MR som den foretrukne metode til diagnose af cystiske neoplasmer i bugspytkirtlen (PCN). Multimodalitetsbilleddannelse bør overvejes i tilfælde, hvor identifikation af forkalkning er vigtig, til tumorstaging eller til diagnosticering af postoperativ tilbagevendende sygdom. Imidlertid, nøjagtigheden forbliver relativt lav til identifikation af den specifikke type PCN, til differentiering af lille PCN fra ikke-neoplastiske eller ikke-epiteliale cyster, eller til forbindelse til duktalsystemet. CT bør overvejes i følgende kliniske situationer :
-
til påvisning af parenkymal, vægmaleri eller central forkalkning, og især ved differentiering af pseudocyster forbundet med kronisk pankreatitis fra cystiske neoplasmer i bugspytkirtlen
-
når der er mistanke om malignitet eller samtidig kræft i bugspytkirtlen, og når vurdering af vaskulær involvering, peritoneal sygdom eller metastatisk sygdom er påkrævet.
-
når der er mistanke om postoperativ gentagelse af kræft i bugspytkirtlen.
de europæiske retningslinjer finder EUS nyttige til at identificere PCN med funktioner, der bør overvejes til kirurgisk resektion. I lighed med MR og CT har EUS lav nøjagtighed til at identificere den nøjagtige type PCN. EUS-FNA forbedrer diagnostisk nøjagtighed til differentiering af mucinøs versus ikke-mucinøs PCN såvel som ondartet versus godartet PCN i tilfælde, hvor CT-eller MR-fund er uklare. Yderligere anbefalinger til brug af EUS-FNA omfatter følgende:
-
EUS-FNA bør kun udføres, når resultaterne forventes at ændre klinisk behandling
-
EUS-FNA bør ikke udføres, hvis diagnosen allerede er etableret ved tværsnitsbilleddannelse, eller hvor der er en klar indikation for operation
-
Relative kontraindikationer for EUS-FNA i PCN er en afstand på >10 mm mellem cysten og transduceren, tilstedeværelsen af en høj risiko for blødning på grund af blødningsforstyrrelse eller brugen af dobbelt blodplader