introduktion
tilstrækkelig fortolkning af myokardienekrosemarkører er afgørende for diagnose, stratificering og behandling af patienter med mistanke om akut koronarsyndrom (ACS). Protokollerne om hjertemarkører for akut myokardieinfarkt (AMI) henvises til den tredje universelle definition af AMI.
dette dokument fastslår, at hjerte troponin (cTn) forhøjelse og sænkning er grundlæggende for at etablere diagnosen i forbindelse med iskæmiske symptomer, elektrokardiografiske ændringer eller nyligt manifesterende segmentale ændringer i en billeddannelsesundersøgelse.1
teknologiske fremskridt inden for bestemmelse af cTn har forbedret kapaciteten til at detektere og kvantificere myocardial celleskade. Kriterierne for forhøjelse af cTn-værdierne afhænger af den anvendte test og skal defineres på grundlag af præcisionsprofilen for hver test, herunder højfølsomhedsprøvning.2 eksistensen af forskellige kommercielle ctn-immunoassays med forskellige percentil 99 (p99) koncentrationer; det faktum, at nogle laboratorier bruger forskellige referencer til resultaterne af myokardiebeskadigelsestest (“normal”, “ubestemt” eller “suggestiv”); og den vilkårlige anvendelse af cTn-test i store populationer med meget forskellige sandsynligheder for at præsentere ACS, har tendens til at skabe forvirring i forbindelse med klinisk ledelse.
der er et betydeligt antal patienter, der i fravær af AMI alligevel udviser ctn-koncentrationer> p99. Disse patienter har normalt kardiovaskulære risikofaktorer, og sandsynligheden for komplikationer hos sådanne personer svarer til den hos patienter med ACS.3
de seneste europæiske anbefalinger om behandling af patienter med ikke-ST elevation akut koronarsyndrom (NSTE-ACS) går ind for brugen af høj følsomhed cTn (hs-cTn) versus konventionelle eller fjerde generation (4G) troponiner og overveje op til to algoritmer (0h/3h, 0h/1h) til bekræftelse (regel i) eller udelukkelse (udelukke) af AMI.4
Hjertetroponiner er ekstremt specifikke for myokardiebeskadigelse. Imidlertid er myokardiebeskadigelse på ingen måde eksklusiv ACS. Derfor understreger de kliniske vejledninger, at ctn-koncentration skal fortolkes i forhold til patientens symptomer. I denne henseende forhøjede ctn-koncentrationer hos patienter med sepsis, hypertensive kriser, lungeemboli osv., er tegn på myocardial skade, men ikke af AMI, og bør ikke bruges til at indikere specifikke behandlinger for ACS.5
udtrykket “høj følsomhed” bør forbeholdes de immunanalyser, der er i stand til at bestemme p99 med en variationskoefficient (CV) på 6
der er tvivl i det videnskabelige samfund om, hvorvidt brugen af hs-cTn repræsenterer signifikant klinisk forbedring, og om det indebærer flere tests og interkonsultationer.7 Denne undersøgelse blev udført for at evaluere den diagnostiske ydeevne af troponin T med høj følsomhed (hs-TnT), bestemme, om det forkorter tiden til diagnose og analysere de kliniske konsekvenser af dets anvendelse.
metode
en prospektiv, langsgående observationsundersøgelse blev udført i hospitalets beredskabstjenester (HES) på Hospital Cl Kursnico (Valencia), Hospital Cl Kursnico (m Kurstlaga), Hospital Severo Ochoa (Legan Kriss), Hospital Sant Pau (Barcelona) og Hospital Miguel Servet(Spanien), der involverede patienterne i TUSCA (Troponina Ultrasensible en el SCA) trial8 mellem juni 2009 og April 2010. Undersøgelsen blev udført i overensstemmelse med principperne i Helsinki-erklæringen og blev godkendt af de lokale etiske udvalg i de deltagende Centre. Der blev indhentet skriftligt informeret samtykke fra alle patienter. Vi inkluderede fortløbende patienter over 18 år set i HES på grund af brystsmerter, der tyder på nste-ACS. Patienttilmelding blev foretaget under indledende pleje i HES efter vurdering af inklusions-og eksklusionskriterierne. Patientstyring og den anvendte behandling fulgte interne protokoller baseret på konsensusvejledningerne fra European Society of Cardiology under indikationerne fra de læger, der til enhver tid var ansvarlige for patienterne, og med total uafhængighed af deltagelse i undersøgelsen. Serielle 4G cTn-bestemmelser blev foretaget til diagnose af ACS i overensstemmelse med rutinemæssig klinisk og immunoassay praksis i hvert center.
patientkarakteristika blev indtastet i en sagsrapportformular og omfattede demografiske data, tid henvist til symptomdebut, tilstedeværelsen af risikofaktorer (arteriel hypertension, diabetes mellitus, kronisk obstruktiv lungesygdom , hjertesvigt og nyresvigt). Vi registrerede også EKG-karakteristika med og uden smerte samt information, der henvises til ledelse efter indledende akutpleje (kateterisering, angioplastier, bypass-operation osv.), den endelige diagnose og patientdestination.
patienter med ST-segment elevation ACS blev udelukket, ligesom dem med nyligt manifesterende venstre bundblok, defibrillering eller kardioversion før de første laboratoriebestemmelser, hjertekirurgi i de tre uger før indlæggelse, gravide kvinder, patienter med svær kognitiv svækkelse og personer med kronisk nyresvigt udsat for hæmodialyse.
i løbet af de første 12 timers ophold i HES, intensivafdeling (ICU) eller hospitalsafdeling blev der opnået serielle blodprøver til måling af hs-TnT, baseret på følgende protokol:
- –
Prøve T0. På tidspunktet for første hjælp i HES.
- –
Prøve T1. To timer efter prøveudtagningstidspunktet 0 eller umiddelbart før indlæggelse på en Hospitalsenhed (ICU eller afdeling).
- –
Prøve T2. Mellem 4 og 6 timer efter prøveudtagningstidspunkt 0 eller umiddelbart før indlæggelse på en Hospitalsenhed.
- –
Prøve T3. Mellem 8 og 12 timer efter prøveudtagningstidspunkt 0, hvis patienten stadig var i tjenesten eller umiddelbart før indlæggelse på en Hospitalsenhed eller på tidspunktet for patientens udskrivning fra HES.
der blev opsamlet tilstrækkeligt blod til at opnå 5 alikvoter på 0,5 ml hepariniseret plasma fra hver af patientens prøver ud over den prøve, der kræves til rutinemæssig test. Alikvoterne blev frosset ved -80 kr. C og blev identificeret med koden for hvert center: tre cifre svarende til patientnummeret og indsamlingstidspunktet (T0, T1, T2 eller T3) ifølge den involverede prøve. Der blev i gennemsnit opnået 3,7 prøver pr. Alle prøverne blev overført til kernelaboratoriet (Hospital Sant Pau, Barcelona) til analyse af 4G cTn og hs-TnT, hvor der ikke måtte gå mere end en måned fra hver samling. Hospitalerne udførte alle den rutinemæssige 4G cTn-test, der blev brugt på det tidspunkt (2 centre med cTnT og 3 med cTnI). Den endelige patientdiagnose blev oprettet af en ekspert baseret på alle de kliniske oplysninger, der leveres af sagsrapportformularen udfyldt af hovedundersøgeren i hvert center, hvilket afspejler de kliniske data og EKG-data og den centraliserede 4G cTn-bestemmelse foretaget i kernelaboratoriet. Eksperten blev blindet for HS-cTn-bestemmelserne.
infarkt blev diagnosticeret i nærvær af en forhøjelse eller reduktion i ctnt-koncentration på > 20% (kriteriet om en kur) blandt flere prøver, hvor mindst en værdi var større end p99 for referencepopulationen (0,01 kurg/l). Diagnosen ustabil angina (UA) blev etableret hos patienter med klinisk bevis for myokardisk iskæmi uden positiv 4G cTn. Patienterne med UA præsenterede en historie med hvilende angina, forværring af tidligere kronisk angina, ST-segmentændringer, der tyder på iskæmi uden biomarkørvariationer (kinetik), positive iskæmi-detektionstest eller stenose>70% af en koronararterie som det fremgår af koronar angiografi. Ctnt-niveauerne blev igen målt ved hjælp af en Højfølsomhedsteknik på en Cobas e601-analysator (hs-TnT, Roche Diagnostics, Basel, Sverige). Teknikken har en detektionsgrænse på 5,0 ng/l, og referencen p99, anvendt som den kliniske beslutningsgrænse, var 13,0 ng/l. den analytiske upræcision af disse cTn-test blev evalueret i 20 gentagelser af 8 grupper af prøver med slutkoncentrationer justeret til at dække området mellem 7 og 928ng/l, fortynding af en høj ctnt-koncentrationsprøve med en serumpool, der præsenterer ikke-detekterbare HS-TnT-niveauer (
ng / l). P99 af ctnt-testen (10ng/l=0,01 liter / l) blev målt med en variationskoefficient (CV) på 15,2%. Værdien med CV 10% var 35ng/l=0,035 liter/l. P99 af HS-TnT-testen (13ng/l) blev målt med et CV på 6,9%.
frekvenser og procenter blev beregnet til den beskrivende analyse af de kvalitative variabler med centrale tendensmålinger for de kvantitative variabler. Dataene blev udtrykt som middel – og standardafvigelsen (SD) i nærvær af en normalfordeling og som median-og interkvartilområdet (IKR) i tilfælde af en ikke–normalfordeling, som det fremgår af Kolmogorov-Smirnov-testen.
sammenligningen af kvantitative variabler var baseret på den studerendes t-test eller Mann–Hvidney U-test i nærvær eller fravær af en normal datafordeling, henholdsvis. Sammenligningen af kvalitative variabler var igen baseret på chi-kvadreret test eller Fisher nøjagtig test, alt efter hvad der var relevant.
i alle tilfælde blev niveauet af statistisk signifikans defineret som 5% (kur=0,05%) i to-tailed test.
4G ctn-og HS-TnT-diskriminationsundersøgelsen blev udført med beregning af arealet (AUC) under receiverens driftskarakteristik (ROC) – kurve ved de forskellige prøvetagningstidspunkter med det tilsvarende 95% konfidensinterval (CI). Betydningen af disse kurver blev evalueret ud fra beregningen af AUC ‘ s CI, idet værdierne i areal med en nedre grænse på over 0,5% blev defineret som signifikante. Sammenligningen af områder under ROC-kurven blev foretaget ved at studere overlapningen af CI-værdier.
diagnostisk ydeevne blev vurderet ved beregning af følsomhed, specificitet og de positive og negative prædiktive værdier. 95% konfidensintervallet blev beregnet til klinisk vurdering af størrelsen af disse mål – intervallet betragtes som signifikant i fravær af overlapning af værdierne.
resultater
undersøgelsen omfattede i alt 351 patienter; 234 var mænd (67,9%), og gennemsnitsalderen var 65,7 år. De vigtigste demografiske data og kardiovaskulære risikofaktorer er opsummeret i tabel 1. En endelig diagnose af AMI blev etableret hos 77 patienter, med UA hos 102 patienter. I alt 172 patienter blev diagnosticeret som uden ACS.
karakteristika og kardiovaskulære risikofaktorer for undersøgelsen prøve.
| variabler | i alt | ingen ACS | ustabil angina | AMI | p |
|---|---|---|---|---|---|
| Nej. patienter n (%) | 351 | 172 (49) | 102 (29.1) | 77 (21.9) | – |
| alder (median) | 66 (27-93) | 64.4 (27-93) | 71 (31-90) | 73 (36-88) | |
| mænd, % | 67.9 | 61.5 | 73.5 | 74 | |
| sygdomshistorie n (%) | |||||
| AHT | 220 (62) | 101 (58.7) | 73 (71.6) | 46 (59.6) | NS |
| Diabetes | 92 (26.2) | 38 (22.1) | 35 (34.3) | 19 (24.7) | NS |
| hjertesvigt | 52 (14.8) | 20 (11.6) | 20 (19.6) | 12 (15.6) | NS |
| glomerulær filtreringshastighed (ml / min / 1,73 m2) | 79.6 | 81.9 | 80.7 | 72.9 | |
| TnT kurstg / l (median) | 0.285 (0.01–6.87) | 0.009 (0.001–0.46) | 0.009 (0.009–0.03) | 0.066 (0.009–6.870) | |
| Hs-TnT ng / l (median) | 63.87 (2.99–7.096) | 5.5 (1.2–481.6) | 11.69 (1.99–66) | 90.4 (2.9–7.096) | |
| NT-proBNP pg / ml (median) | 1.130 (5.46255) | 141 (5-13.302) | 238.5 (16.4–9.164) | 589 (41-46.255) | |
| elektrokardiogram med smerte (70.67%) | |||||
| Normal | 103 (41.1) | 70 (61.4) | 22 (27.5) | 11 (20) | |
| T neg | 57 (23) | 21 (18.6) | 23 (28.8) | 13 (23.6) | |
| ↓ ST | 60 (24.5) | 9 (8) | 26 (32.6) | 25 (45.4) | |
| udvikling af symptomer (min) (88%) | |||||
| ≤3h (%) | 46 | 63 (42) | 43 (44.8) | 41 (55.4) | 0.16 |
| >3h (%) | 57 | 87 (58) | 53 (55) | 33 (44.6) | NS |
| Catheterization | 36.9 | 12 (7) | 64 (62.7) | 53 (68.8) | |
| Angioplasty | 20.9 | 2 (1.2) | 29 (28.4) | 41 (53.2) | |
| Stent | 18.7 | 1 (0.6) | 28 (27.5) | 35 (45.5) | |
| Bypass | 2.2 | 0 | 4 (3.9) | 4 (5.2) | |
| decharge for nødtjeneste | 41.1 | 128 (74.7) | 10 (10.9) | 5 (6.6) | |
| udskrivning på hospitalet | 57.8 | 44 (25.3) | 92 (88.1) | 72 (91) | |
| død | 1.1 | 0 | 1 (1.9) | 3 (3.8) | |
AHT: arteriel hypertension; AMI: akut myokardieinfarkt; NS: ikke-signifikant; NT-proBNP: hjerne natriuretisk peptid; ACS: akut koronarsyndrom; TnT: troponin T; hs-TnT: høj følsomhed troponin T.
i alt 55,4% af patienterne med AMI nåede HES inden for de første tre timer, mens en større procentdel af både dem med UA og dem uden ACS ankom efter tre timer. Med hensyn til markørernes positivitet i henhold til den endelige diagnose præsenterede 87% af patienterne med en endelig diagnose af AMI 4G ctn>0,035 larg/l i løbet af de første 12 timer af undersøgelsen. I tilfælde af ikke-ACS-patienter og patienter med UA blev positivitet registreret i 4% af tilfældene. HS-TnT-koncentrationen var > 13ng/l (p99) hos henholdsvis 26,7% og 46% af de patienter, der blev diagnosticeret med ikke-ACS og UA (Fig. 1). På den anden side 4G cTn ved hjælp af p99 med et afskæringspunkt på 0.01 L (undersøgelsens guldstandard) viste sig at være positiv hos 16% af de patienter, der blev diagnosticeret med UA, og hos 11% af dem uden ACS.
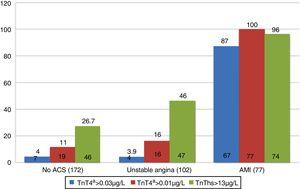
Markørpositivitet i henhold til den endelige diagnose. AMI: akut myokardieinfarkt; ACS: akut koronarsyndrom; TNT: troponin T; hs-TnT: høj følsomhed troponin T.
ved anvendelse af kinetik blandt nogle af de fire bestemmelser (Kurskriterium) viste 21,5% af patienterne med UA forhøjelse af hs-TnT+Karrus (Fig. 2).

positivitet+prist af markørerne i henhold til den endelige diagnose. AMI: akut myokardieinfarkt; ACS: akut koronarsyndrom; TnT: troponin T; hs-TnT: troponin T.
ved første måling (T0) var den diagnostiske følsomhed for hs-TnT signifikant større end for 4G cTn (CV) (87,0%; 83,0–90,3% mod 42,9%; 37,6–48,2%; p
0,05), hvilket resulterede i en negativ forudsigelsesværdi på 95,1%. Imidlertid var dens specificitet (71,5%; 66,5–76,2% vs. 97,4%; 95,2–98,8%; p0.05) og positiv forudsigelsesværdi (46,2% vs. 82,5; p0.05) klart lavere end 4G cTn (CV). Ved analyse af området under ROC-kurven blev hs–TnT set at være bedre end 4g cTn (CV) (0,792; 0,746–0,833 vs. 0,701; 0,650-0,748) (Fig. 3 og 4).
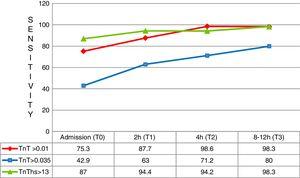
følsomhed ved de forskellige testtider. TNT: troponin T; hs-TNT: høj følsomhed troponin T.
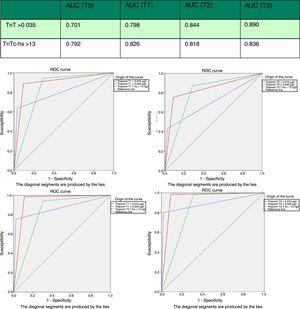
areal under kurven (AUC) for hs-TnT og TnT 4G i prøveudtagnings-og modtageroperationskarakteristika (ROC) kurver. AUC: areal under kurven; TNT: troponin T; hs-TnT: troponin T.
to timer efter patientens ankomst til HES (T1) fortsatte hs-TnT med at vise langt højere diagnostisk følsomhed end 4g cTn (94,4%; 91,3–96,6 vs. 63,0%; 57,6–68,2; p0.05). Den negative prædiktive værdi af hs-TnT var praktisk talt absolut (97,9%), og dens diagnostiske nøjagtighed havde tendens til at være bedre end 4G cTn (ROC 0,826 vs. 0,798). Den lave specificitet af hs-TnT resulterede i en lav positiv prædiktiv værdi (46,5%). Resten af prøveudtagningsresultaterne viste sig at være ens, men afspejler mindre diagnostisk ydeevne.
i de første tre timer efter symptomdebut ankom i alt 41 patienter med en endelig diagnose af AMI. I disse tilfælde var den overlegne diagnostiske følsomhed af hs-TnT med hensyn til 4G cTn (CV) og også 4G cTn (p99) særlig signifikant med en følsomhed på henholdsvis 87, 8% versus 36, 6% og 73, 2% (Fig. 5).
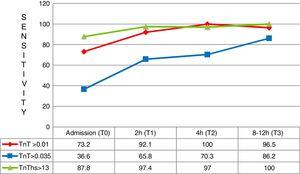
følsomhed ved de forskellige testtider for patienter med symptomdebut min. TNT: troponin T; hs-TNT: høj følsomhed troponin T.
patienterne diagnosticeret med ikke-ST elevation myokardieinfarkt (n=36) og præsenterede lange evolutive tider (> 3h) viste mindre diagnostisk nøjagtighed med hs-TnT (på grund af den lavere specificitet) end patienterne med kortere tid fra symptomdebut. Ved anvendelse af kinetik blev der igen observeret specificitet med en stigning i AUC. I tilfælde af hs-TnT startede vi derfor med en specificitet på 69%, og ved anvendelse af Kurr nåede specificiteten 85% med en positiv forudsigelsesværdi på 55,3%, der forbedrede den samlede diagnostiske ydeevne (tabel 2).
kinetik (Kurt) af de forskellige hjertetroponiner hos patienter med symptomdebut >180min.
| følsomhed | specificitet | PPV, % | NPV, % | AUC | |
|---|---|---|---|---|---|
| cTnT> 0.01 + en | 100% (97.9–100) | 96.4% (92.4–98.6) | 86.8 | 100 | 0.982 |
| cTnT> 0.035 + hvis | 81.8% (75.2–87.2) | 97.9% (94.4–99.4) | 90.0 | 95.8 | 0.898 |
| hs-TnT>13 + Hvis | 78.8% (71.9–84.6) | 85.0% (78.8–89.9) | 55.3 | 94.4 | 0.818 |
AUC: område under kurven; cTnT: hjertetroponin T; hs-TnT: troponin T med høj følsomhed; PPV: positiv forudsigelsesværdi; NPV: negativ forudsigelsesværdi.
derudover vurderede vi de optimale afskæringspunkter afledt af ROC-analysen. Det optimale punkt blev fastlagt som 37ng / l (HS-TnT-ROC) (tabel 3). Værdien for hs-TnT-ROC præsenterede en følsomhed på 59.7%-langt under hs-TnT, men større end 4G TnT (CV) – og en specificitet på 95, 3% i den første måling. Denne større følsomhed med hensyn til 4G TnT (CV) fortsatte i resten af prøveudtagningerne.
sammenligning af den diagnostiske ydeevne af HS-TnT ROC (> 37).
| T0 | Sensitivity, % | Specificity, % | EFF, % | LR+ | LR− | PV+, % | PV−, % |
|---|---|---|---|---|---|---|---|
| cTnT>0.01 | 75.3 | 91.2 | 87.7 | 8.60 | 0.27 | 70.7 | 92.9 |
| cTnT>0.035 | 42.8 | 97.5 | 85.5 | 16.8 | 0.59 | 82.5 | 85.8 |
| hs-TnT>13 | 87 | 71.5 | 74.9 | 3.1 | 0.18 | 46.2 | 95.1 |
| hs-TnT>37 | 59.7 | 95.3 | 87.5 | 12.6 | 0.42 | 78 | 89.4 |
ctnt: hjerte troponin T; hs-TnT: høj følsomhed troponin T.
tidsbesparelsen ved at nå en diagnose ved brug af hs-TnT versus 4G cTn (CV) var 113min. Besparelsen ville igen være 147min (p0.001) i tilfælde af patienter indlagt på under 3 timer fra symptomdebut og 63min (p=0, 024) i tilfælde af patienter indlagt over tre timer fra symptomdebut.
Diskussion
de data, der er opnået i denne undersøgelse, er i stand til at afklare visse spørgsmål vedrørende brugen af hs-TnT i beslutningsprocessen i betragtning af det stærke bevis for dets anvendelighed som et diagnostisk og prognostisk værktøj i ACS. Den diagnostiske ydeevne for vores hs-TnT blev i sidste ende set at være større end 4G cTn ved hvert af de forskellige prøvetagningstidspunkter. Præstationen blev igen set at falde i løbet af timerne efter symptomdebut. I vores undersøgelse brugte vi relative ændringer mellem to prøver (specifikt 20%), der diskret forbedrede den positive forudsigelsesværdi, dog uden at blive praktisk brug. I denne henseende kan en krus på 20% muligvis være for lille, og som foreslået af nogle forfattere kunne det have været tilrådeligt at øge krus til en højere procentdel, da mange tilfælde af AMI viste sig at være på værdier diskret højere end den øvre referencegrænse (URL).9,10 andre efterforskere foreslår relative ændringer af Karrus (mellem 30 og 250%) for at øge diagnostisk specificitet og forbedre diagnosen AMI.11-14 Mueller et al.15 offentliggjorte resultater, der forklarer, hvorfor relative ændringer af kur mislykkes for at herske i ikke-ST elevation myokardieinfarkt. Ved anvendelse af absolutte ændringer af Kross synes en stigning eller et fald på mindst 9,2 ng/l for populationen af patienter med ACS og ikke-ACS eller på 6,9 ng/l for en population med ACS at være mere passende end relative ændringer af Kross for at udelukke AMI. Ud over disse problemer med faldet i specificitet er der forskelle i URL i henhold til den anvendte test. Dette fremhæver vigtigheden af race, køn, alder eller antallet af deltagere i undersøgelsen,16 og tilføjer øget vanskelighed med at nå til enighed i beslutningsprocessen.
i vores undersøgelse viste overlegenheden af følsomheden af hs-TnT ved diagnosticering af ikke-ST-elevation myokardieinfarkt at være større hos patienter med nylige symptomdebut i overensstemmelse med resultaterne fra andre forfattere.17,18 For en patient, der rapporterer med brystsmerter i mindre end tre timer, og med en anden negativ bestemmelse to timer efter ankomst, kan vi udelukke AMI i næsten 100% af tilfældene. Dette kombineret med de kliniske og EKG-fund kan identificere kandidater til tidlig udskrivning og ambulant behandling. På den anden side viser patienter, der er diagnosticeret med ikke-ST elevation myokardieinfarkt og præsenterer lange evolutive tider (over 3 timer), mindre diagnostisk nøjagtighed med hs-TnT, selv når de udfører to serielle bestemmelser. I disse tilfælde bør vi evaluere de optimale afskæringspunkter, der stammer fra ROC-analysen. I vores undersøgelse var afskæringspunktet 37ng/l, hvilket ville give os mulighed for at “herske ind”, dvs.patienter med score over dette afskæringspunkt ville have en meget høj sandsynlighed for at præsentere AMI. Det er også blevet hævdet, at dette fald i specificitet er blevet undervurderet i litteraturen, og at det ikke afspejler de patienter, der ses i HES på vores hospitaler, hvor gennemsnitsalderen, comorbiditeter og ctn-forhøjelser har tendens til at være høje.
tiden til diagnose er blevet kraftigt reduceret (fra 247 til 71.5min).19,20 I vores undersøgelse var tidsbesparelsen for diagnosen ikke-ST elevation myokardieinfarkt 147min i tilfælde af patienter, der rapporterede under tre timer efter symptomdebut og 63min, når de rapporterede efter 3 timer.
toogtyve af patienterne (21,5%) med en diagnose af UA ved udskrivning ville være ikke-ST elevation myokardieinfarkt tilfælde efter to bestemmelser af hs-TnT med kinetik på over 20% mellem dem. Op til 13.9% af de ikke-ACS-patienter (n=24) ville udvise positivitet med hs-TnT ved anvendelse af sådan kinetik og ville svare til andre sygdomsbetingelser, der forårsager progressiv hjerteskade, såsom myocarditis, lungeemboli eller takotsubo-syndrom. Forskellige HS-TnT-analyser registrerer op til 27% flere tilfælde af AMI end den nuværende metode hos patienter med brystsmerter og en lav eller mellemliggende Sandsynlighed for ACS.20,21 det kunne endda spekuleres i, at diagnosen UA ville forsvinde, som understreget af Sabatine et al.22 hos patienter med positiv træningstest evalueret med ultrasensitive teknikker. I denne undersøgelse kunne hs-TnI påvises hos alle patienter før testene; forblev uden ændring hos patienterne uden iskæmi; og steg 24% hos dem med mild iskæmi og 40% hos dem med moderat til svær iskæmi. Der blev ikke observeret ændringer med 4G cTn. Følgelig er de resultater, der henvises til diagnosen ikke-ST-elevation myokardieinfarkt ved anvendelse af konventionel ctn, et spørgsmål om bekymring, da myokardieskade har en begrænset foranstaltning, og cTn-værdierne ikke altid stiger tidligt, eller deres trin er ikke tilstrækkelige til at muliggøre tidlig identifikation.
hurtige opløsningsprotokoller bør indføres, hvorved vores patienter med lav iskæmisk risiko og en normal EKG–sporing kun bruger 3-4 timer på hospitalet.23,24 det er blevet overvejet,om en enkelt HS-TnT-bestemmelse er tilstrækkelig til at udelukke AMI, 25 og andre undersøgelser har vurderet muligheden for en enkelt bestemmelse, hvis HS-TnT-værdien er
ng/l (dvs.ikke detekterbar).24 alle disse situationer skal overvejes i fremtiden.Konklusioner
troponin T-test med høj følsomhed forbedrer diagnostisk ydeevne, forkorter tiden til diagnose af AMI og er i stand til at identificere et større antal patienter med mindre infarkt, som tidligere blev diagnosticeret som UA, og som har en høj dødelighedsrisiko sammenlignet med konventionel ctn. Desuden forkorter det tiden til at udelukke sager, da AMI kunne kasseres inden for 2 timer. alt dette indebærer tidligere behandling for patienter med myokardienekrose og en forkortelse af patientens ophold i HES. Hos de personer, der rapporterer til HES efter tre timers symptomdebut, ville hs-TnT imidlertid ikke være i stand til at forbedre den diagnostiske ydeevne for 4G cTn, og beslutningstagning skulle derfor være mere forsigtig. HS-cTn-testene ændrer ledelsen og konceptet for patienter med brystsmerter, der tyder på ACS. Dette gør det nødvendigt for akut og kritisk pleje læger at blive fortrolig med deres rutinemæssige brug.
interessekonflikt
forfatterne erklærer, at de ikke har nogen interessekonflikter.