Los quistes pancreáticos representan una entidad pequeña pero cada vez más detectada de anomalías pancreáticas. Aproximadamente el 70% de las lesiones quísticas pancreáticas se descubren de forma accidental. Los quistes pancreáticos neoplásicos encontrados con más frecuencia incluyen neoplasia mucinosa papilar intraductal (MMI), cistadenoma seroso (SCA), neoplasia quística mucinosa con estroma ovárico (NCM) y neoplasia epitelial pseudopapilar sólida. IPMN se subdivide en conductos de derivación (BD), conductos principales y formas combinadas. En conjunto, constituyen el 90% de los tumores pancreáticos premalignos, principalmente quísticos. Por el contrario, el seudoquiste, el quiste epitelial verdadero, el quiste linfoepitelial y el quiste mucinoso no neoplásico no tienen potencial maligno.
La neoplasia maligna ocurre solo en quistes mucinosos. El SCA se considera una lesión no maligna y no se ha encontrado que los tumores serosos malignos notificados en la literatura cumplan con los criterios de la OMS para el NCG. La MIPM puede progresar de grados más bajos a más altos de displasia y, en última instancia, adenocarcinoma ductal pancreático (PDAC). Las IPMN que comprometen el conducto principal tienen una tasa de malignidad más alta que las de las ramas, con un riesgo de malignidad estimado en 62%; el riesgo de malignidad de los MCN es menor de 15%. Otras lesiones quísticas más raras, como la neoplasia epitelial seudopapilar sólida y el tumor neuroendocrino pancreático quístico (cPNET, por sus siglas en inglés), tienden a albergar características que sugieren un diagnóstico específico, que generalmente conducen a la extirpación quirúrgica.
Para estudiar la frecuencia de quistes pancreáticos incidentales en individuos asintomáticos, Kromrey realizó un examen de colangiopancreatografía por resonancia magnética (CPRM) en 1.077 participantes inscritos en un estudio de cohorte poblacional. Del grupo original, 676 personas se sometieron a un examen repetido 5 años después. En el momento del examen inicial, el 49% tenía al menos un quiste ≥2 mm de diámetro. La incidencia de nuevos quistes durante el periodo de seguimiento fue del 2,6% por año. La presencia de quistes estuvo fuertemente relacionada con la edad; a los 75 años de edad, el 75% de los participantes tenían uno o más quistes. La discriminación entre quistes pancreáticos benignos y premalignos o malignos es de gran importancia para evitar procedimientos innecesarios, como exámenes radiológicos de seguimiento o resección quirúrgica.
La neoplasia quística mucinosa con estroma ovárico (NCM)
Las NCM son comunes en mujeres de mediana edad, por lo general están bien definidas y se encuentran predominantemente en la cola del páncreas (>90%). En comparación con los tumores quísticos serosos, los NCM son más grandes (>20 mm de diámetro) y menos numerosos (generalmente < 6). El comportamiento biológico de los NCM es variable y con frecuencia coexisten diferentes patrones histológicos en el mismo tumor. Los tumores pueden ser completamente benignos, al igual que los cistadenomas mucinosos o los adenomas mucinosos papilares intraductales. Algunos tumores son limítrofes, mostrando displasia celular, mientras que otros son francamente malignos. El cistadenocarcinoma maligno y los carcinomas mucinosos intramedulares se pueden subdividir en tipos no invasivos e invasivos.
(Las características radiológicas de los NCM se demuestran en las imágenes a continuación.)
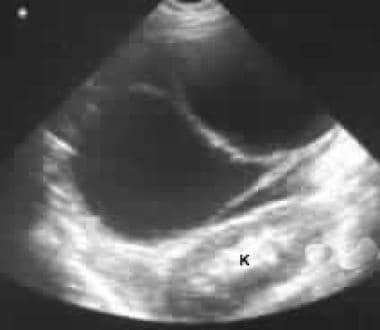 La ecografía a través del hipocondrio izquierdo muestra una gran masa septada anterior al riñón (K).
La ecografía a través del hipocondrio izquierdo muestra una gran masa septada anterior al riñón (K). 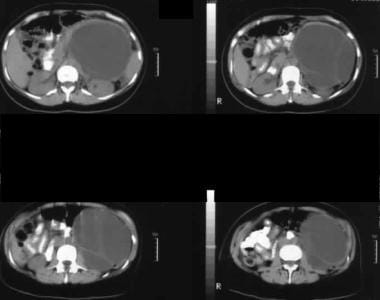 no reforzada. La imagen 1 muestra una gran masa septada en el hipocondrio izquierdo. Observe el contorno externo liso típico de una neoplasia quística mucinosa.
no reforzada. La imagen 1 muestra una gran masa septada en el hipocondrio izquierdo. Observe el contorno externo liso típico de una neoplasia quística mucinosa. Neoplasia mucinosa papilar intraductal (IPMN)
Sobre la base de la afectación del conducto pancreático, las IPMN se clasifican como IPMN del conducto principal, IPMN de rama lateral o IPMN variante mixta que involucra tanto el conducto pancreático principal como las ramas laterales. Las IPMNs de conducto principal a menudo tienen epitelio de tipo intestinal, y las IPMNs de rama lateral generalmente tienen epitelio de tipo gástrico. Aunque todas las variantes morfológicas de la MIPN pueden progresar a cáncer, el adenocarcinoma invasivo que se origina en la MIPN de tipo gástrico se relaciona con una tasa de supervivencia significativamente peor que la que se origina en otros tipos de MIPN. Sin embargo, las características de las imágenes no son específicas para diferenciar las diversas variantes histológicas de la NIPM.
Los IPMN de rama lateral se detectan comúnmente en hombres mayores y se localizan con mayor frecuencia en el páncreas proximal (proceso de cabeza y uncinado). Una característica diferenciadora importante entre MCN e IPMN es la visualización de la comunicación ductal pancreática. Si se visualiza un canal de comunicación claro con el conducto pancreático, el diagnóstico de MPI de rama lateral es casi seguro porque los SCA y los MCN no se comunican con el sistema ductal pancreático.
A pesar de la baja incidencia de agresividad de las lesiones quísticas mucinosas de 3 cm o menos, la incidencia no es lo suficientemente baja como para descartar las lesiones por completo, y se requiere una revisión cuidadosa de las características de imagen. Además, los pacientes cuya afección no se considera adecuada para el tratamiento quirúrgico a menudo necesitan evaluaciones frecuentes para determinar el crecimiento y el cambio en las características de las imágenes.
(las IPMN se ven en las imágenes de abajo.)
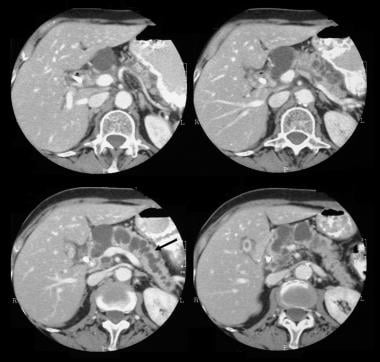 Tumor mucinoso papilar intraductal pancreático (TMPI). Las TC axiales con contraste a través del páncreas muestran un tumor quístico de 5,5 cm en la cabeza pancreática. Observe la dilatación macroscópica del conducto pancreático. El conducto pancreático accesorio también está dilatado.
Tumor mucinoso papilar intraductal pancreático (TMPI). Las TC axiales con contraste a través del páncreas muestran un tumor quístico de 5,5 cm en la cabeza pancreática. Observe la dilatación macroscópica del conducto pancreático. El conducto pancreático accesorio también está dilatado. 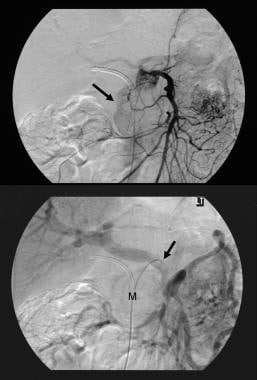 Tumor mucinoso papilar intraductal pancreático (TMPI). (Arriba) El angiograma mesentérico superior muestra vascularización capilar en la masa de la cabeza pancreática durante la fase arterial. (Abajo) La imagen de la fase venosa portal muestra el desplazamiento de las ramas venosas portal y el encapsulado de la unión de la vena mesentérica superior y la vena portal. M denota la masa pancreática.
Tumor mucinoso papilar intraductal pancreático (TMPI). (Arriba) El angiograma mesentérico superior muestra vascularización capilar en la masa de la cabeza pancreática durante la fase arterial. (Abajo) La imagen de la fase venosa portal muestra el desplazamiento de las ramas venosas portal y el encapsulado de la unión de la vena mesentérica superior y la vena portal. M denota la masa pancreática. 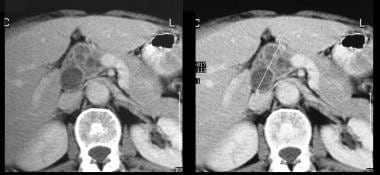 Tumor mucinoso papilar intraductal pancreático (TMPI). Las tomografías computarizadas axiales con contraste a través del páncreas muestran un tumor multiseptato en la cabeza del páncreas.
Tumor mucinoso papilar intraductal pancreático (TMPI). Las tomografías computarizadas axiales con contraste a través del páncreas muestran un tumor multiseptato en la cabeza del páncreas. 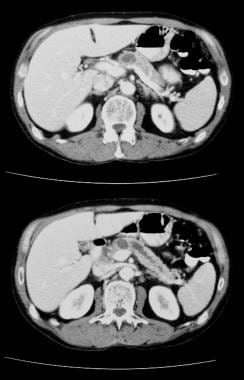 Tumor mucinoso papilar intraductal pancreático (TMPI). Las tomografías computarizadas con contraste a través del páncreas muestran dilatación macroscópica del conducto pancreático. En la cirugía, se confirmó la TMPI.
Tumor mucinoso papilar intraductal pancreático (TMPI). Las tomografías computarizadas con contraste a través del páncreas muestran dilatación macroscópica del conducto pancreático. En la cirugía, se confirmó la TMPI. Cistadenomas serosos
Los cistadenomas serosos (adenomas microquísticos) (vea las imágenes a continuación) son los segundos tumores quísticos más comunes del páncreas. La presentación clínica de los cistadenomas serosos es similar a la de los tumores pancreáticos quísticos mucinosos.
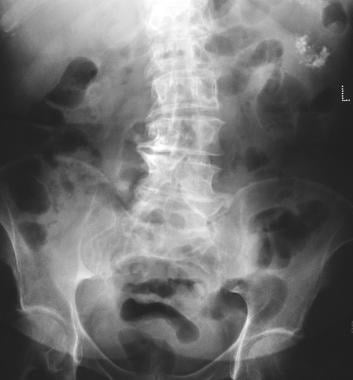 Pancreático microquística adenoma. La radiografía simple muestra calcificación tumoral en un adenoma microquístico (cuadrante superior izquierdo). La calcificación en el adenoma microquístico se presenta como un cúmulo central dispuesto en una quemadura solar o disposición estrellada. La calcificación central se evalúa mejor con TC que con radiografía.
Pancreático microquística adenoma. La radiografía simple muestra calcificación tumoral en un adenoma microquístico (cuadrante superior izquierdo). La calcificación en el adenoma microquístico se presenta como un cúmulo central dispuesto en una quemadura solar o disposición estrellada. La calcificación central se evalúa mejor con TC que con radiografía. 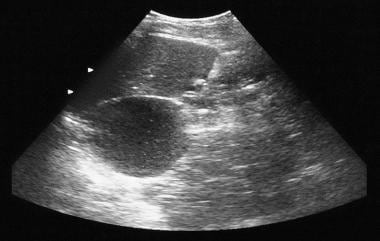 . Ecografía muestra una masa quística en la región de la cola del páncreas.
. Ecografía muestra una masa quística en la región de la cola del páncreas. 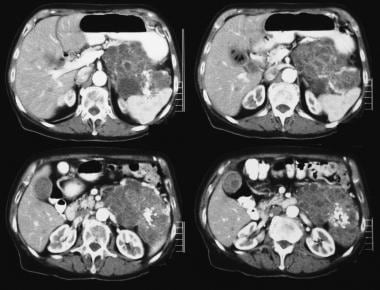 Pancreático microquística adenoma. Las tomografías axiales con contraste muestran un tumor hipervascular en la cola pancreática con calcificación por quemaduras solares. Tenga en cuenta la mejora de queso suizo.
Pancreático microquística adenoma. Las tomografías axiales con contraste muestran un tumor hipervascular en la cola pancreática con calcificación por quemaduras solares. Tenga en cuenta la mejora de queso suizo. Debido al uso creciente de imágenes transversales, muchos de estos tumores se detectan como un hallazgo incidental y asintomático.
En imágenes transversales, los cistadenomas serosos aparecen como numerosos quistes diminutos separados por delicados septos fibrosos, que les dan un aspecto de panal. Los quistes están llenos de líquido transparente y acuoso y, a menudo, están dispuestos alrededor de una cicatriz central estrellada, que puede estar calcificada. En las tomografías computarizadas, la calcificación central por quemaduras solares en una masa esponjosa es patognomónica de este tumor, pero este hallazgo ocurre solo en el 10% de los pacientes.
La ecografía endoscópica (USE) permite una mejor resolución de la estructura de panal que la TC. A veces, los quistes pueden ser grandes, una característica que dificulta la diferenciación de estos quistes de los MCN.
La hipervascularización se puede demostrar en angiogramas, y algunos tumores se presentan con hemorragia intraabdominal.
Diagnósticos diferenciales
Seudoquistes pancreáticos o colecciones de líquido pancreático
Las colecciones de líquido se producen en hasta el 50% de los casos de pancreatitis aguda. Los pseudoquistes generalmente se ven como espacios de líquido anecoico en las ecografías, pero pueden mostrar ecos internos si contienen tejido necrótico o coágulo.
Los hallazgos por imágenes que sugieren un diagnóstico de seudoquiste en lugar de neoplasia quística incluyen los siguientes: falta de septos, loculaciones, componentes sólidos o calcificaciones de la pared quística en tomografías computarizadas (TC); hipovascularización en angiogramas; y comunicación entre el quiste y los conductos pancreáticos en colangiopancreatografía retrógrada endoscópica (CPRE). La mayoría de los pseudoquistes son extrapancreáticos, mientras que las neoplasias quísticas pancreáticas son intrapancreáticas.
Absceso pancreático
El absceso pancreático es generalmente secundario a la infección de un seudoquiste, pero en casos raros, puede ocurrir como resultado de la propagación directa de una infección renal o de colon. Por lo general, un absceso pancreático ocurre de 2 a 4 semanas después de un episodio de pancreatitis aguda.
En las imágenes, estos abscesos pueden parecer similares a los pseudoquistes. En general, la apariencia depende de su edad. En la fase aguda, los cambios pueden ser sutiles, con solo la pérdida del contorno pancreático normal asociada con la obliteración del contorno pancreático y los espacios vasculares peripancreáticos y otros tejidos blandos. Estos cambios pueden ser indistinguibles de los que se encuentran en la pancreatitis aguda grave. En las etapas subaguda y crónica, cuando se produce necrosis central, generalmente se observa una masa quística anecoica o compleja. Se puede observar un nivel de escombros en la parte dependiente del absceso. En la fase subaguda o crónica, la transmisión a través del absceso suele ser buena, excepto cuando el gas está presente dentro del absceso. En presencia de gas, el absceso puede volverse ecogénico y sombrear.
Las paredes del absceso pancreático subagudo y crónico tienen características variables. Las paredes pueden ser gruesas, irregulares y bien definidas, o el absceso puede no tener ninguna pared definible. Los hallazgos ecográficos son inespecíficos, pero en el entorno clínico apropiado, se puede sugerir y confirmar un diagnóstico de absceso mediante aspiración percutánea o TC.
Quistes parasitarios
Se han descrito quistes de granulosis de Echinococcus y quistes multiloculares del páncreas, aunque la afectación pancreática es excepcionalmente rara. E. Los quistes de granulosis pueden ser uniloculares, multiloculares o quísticos complejos.
Solo en imágenes, la diferenciación de estas y otras masas quísticas es difícil. Las pruebas serológicas pueden ser útiles en el entorno clínico apropiado. Los quistes de E. multilocularis muestran un patrón infiltrativo ecogénico. Este diagnóstico debe realizarse en regiones endémicas cuando se observa un patrón de este tipo.
Tumores pancreáticos epiteliales sólidos y papilares
La neoplasia epitelial sólida y papilar del páncreas puede ser sólida o quística. Estos son tumores poco frecuentes que a menudo se confunden con tumores secretores de mucina o adenomas que no funcionan.
Los tumores pancreáticos epiteliales sólidos y papilares se localizan con mayor frecuencia en la cola pancreática. Son masas grandes y bien encapsuladas con áreas de hemorragia y necrosis. En las ecografías, aparecen como masas sólidas, redondas y heterogéneas con un centro necrótico quístico y calcificación distrófica, que puede sombrear.
Quistes disontogénicos
Los quistes disontogénicos son quistes hamartomatosos que a menudo se asocian con quistes renales, angiomas cerebelosos y encefaloceles. Las imágenes revelan un quiste grande de paredes delgadas con una configuración de morera.
Los pseudoaneurismas
Los pseudoaneurismas generalmente no son realmente intrapancreáticos, y pueden confundirse con un quiste pancreático. Estos aneurismas son una complicación de la pancreatitis en el 3,5-10% de los pacientes. La ecografía doppler puede mostrar flujo arterial turbulento dentro de un seudoaneurisma, mientras que la ecografía Doppler de flujo de color muestra flujo bidireccional y remolino dentro de la masa anecoica. Las imágenes doppler pueden permitir la identificación tentativa de la arteria que alimenta el seudoaneurisma.
Neurofibroma retroperitoneal o schwannoma
Estos tumores pueden ser lesiones hiperecoicas o hipoecoicas/quísticas con ecos internos esporádicos. Esta es una característica común en tumores más grandes en los que se han producido degeneración quística y hemorragia. Los tumores son retroperitoneales, pero pueden imitar masas pancreáticas.
Sarcoma pancreático
El sarcoma pancreático es un tumor poco frecuente de las estructuras mesenquimatosas de apoyo del páncreas. Es una masa relativamente sonolucente y puede confundirse con una colección de líquido o seudoquiste. Los resultados ecográficos pueden ser normales, o las ecografías pueden demostrar una masa retroperitoneal, que es relativamente sonolucente en comparación con los tejidos circundantes. Por lo tanto, esta lesión puede confundirse con una masa pancreática quística.
Linfoma pancreático
El linfoma pancreático primario es poco frecuente. La presentación clínica no es diferente de la del carcinoma pancreático. La ecografía puede revelar una masa homogénea, sonolúcida o compleja. Estas masas son generalmente pobres en eco y pueden imitar lesiones quísticas. Como el pronóstico de un linfoma pancreático es favorable, su diferenciación de un carcinoma es crucial. La correlación de los hallazgos ecográficos, TAC y angiográficos puede resultar en un diagnóstico correcto. Sin embargo, si existen dudas, la biopsia guiada por ecografía puede revelar la verdadera naturaleza de la masa.
Carcinoma de células acinares pancreáticas
Los carcinomas de células pancreáticas (PACC) constituyen aproximadamente el 1% de los tumores pancreáticos exocrinos. La PACC es una neoplasia epitelial con evidencia de diferenciación acinar. Los pacientes con carcinoma de células acinares tienen un mejor pronóstico que los pacientes con adenocarcinomas de tipo ductal, pero un pronóstico peor que los pacientes con tumores endocrinos pancreáticos. En la TC, la PACC se ha descrito de varias maneras, incluso como una masa densa mal definida; como una masa bien definida con necrosis central; y como una masa quística rodeada por una gruesa pared hipervascular.
Examen preferido
La RMN es la técnica preferida para el diagnóstico de tumores pancreáticos quísticos. Las resonancias magnéticas suelen ser útiles para diferenciar entre seudoquistes y neoplasias quísticas. La colangiopancreatografía por resonancia magnética (CPRM) puede representar la anatomía de los conductos biliares y pancreáticos de forma no invasiva, y ayuda en el diagnóstico de tumores intraductales.
La ecografía es generalmente la primera técnica en un paciente con síntomas epigástricos. Esta es una excelente modalidad para el diagnóstico de masas pancreáticas quísticas. La ecografía también brinda la oportunidad de realizar intervenciones guiadas, como aspiración y biopsia. La ecografía doppler proporciona un beneficio adicional en la evaluación de tumores hipervasculares y trombosis/oclusión vascular asociados con tumores pancreáticos. La ecografía doppler de potencia mejorada con eco tiene alta sensibilidad y especificidad en el diagnóstico diferencial de tumores pancreáticos.
En casos equívocos o en casos en los que se sospecha de malignidad, el EUS-FNA proporciona el mejor rendimiento diagnóstico, ya que permite la adquisición de muestras citológicas y líquido quístico para el análisis de varios marcadores tumorales.
Ocasionalmente, a pesar de la evaluación completa de una masa quística, el tipo de quiste puede permanecer indeterminado. Aunque la ecografía laparoscópica, la biopsia de la pared del quiste y el análisis del aspirado quístico son costosos e invasivos, contribuyen significativamente al diagnóstico diferencial de las lesiones quísticas pancreáticas.
La TC muestra calcificación tumoral y es una excelente modalidad para la detección de metástasis locales y a distancia. Aunque la TC y la RMN no se pueden utilizar para diferenciar el contenido de mucina del jugo pancreático, la comunicación entre la lesión quística y la DPM dilatada y una papila abultada con un orificio patuloso son características de la TMPI. La arquitectura interna de los tumores mucinosos se muestra al menos tan bien en las IRM como en las TC, con la excepción de la calcificación dentro de la lesión (que la IRM solo tiene una capacidad limitada de revelar).
La TC en espiral y/o multisección son técnicas excelentes para obtener imágenes del páncreas, que proporcionan una resolución espacial y un detalle anatómico excelentes. Con colimación fina, fases arteriales y venosas y reconstrucciones multiplanares y/o tridimensionales (3D), se representa un excelente detalle de la anatomía vascular; la mayoría de los centros ahora rara vez usan la angiografía para evaluar los tumores pancreáticos.
A menudo se obtienen radiografías simples para buscar calcificación pancreática. Los estudios de bario gastrointestinal superior se pueden realizar en el contexto del dolor epigástrico. En el caso de los tumores pancreáticos, los estudios con bario pueden representar un desplazamiento extrínseco del estómago y el duodeno.
Limitaciones de las técnicas
La RMN no está disponible universalmente, es costosa y plantea un problema para los pacientes con claustrofobia. Las pautas de ACG recomiendan precaución cuando se usan imágenes para diagnosticar el tipo de quiste o la malignidad concomitante; la precisión de la RMN o la CPRM en el diagnóstico del tipo de quiste es de 40 a 50% y de 55 a 76% para determinar tumores benignos frente a tumores malignos.
El gas visceral, el hábito del paciente y la dependencia del operador limitan el valor de la ecografía. La ecografía laparoscópica es invasiva. Las imágenes por el uso de la UE no pueden distinguir de manera confiable las IPMN benignas de las malignas, y no está claro si las características de las imágenes de lesiones mucinosas con aumento de potencial maligno son lo suficientemente predictivas para influir en el tratamiento clínico. Cuando se utiliza la histología quirúrgica como estándar de referencia, la precisión diagnóstica de las imágenes de EUS oscila entre el 40% y el 96%. En un solo estudio prospectivo se demostró que la sensibilidad (56%) y la especificidad (45%) de la morfología de la EUS sola para diferenciar los quistes mucinosos (neoplasias quísticas mucinosas e IPMNs) de los quistes no mucinosos fueron bajas, lo que dio lugar a una precisión general deficiente (51%).
Las radiografías simples y los estudios de bario gastrointestinal superior no son específicos, y se pueden encontrar hallazgos similares en una variedad de patologías. La TC conlleva una carga de radiación ionizante significativa y utiliza material de contraste yodado con riesgo de anafilaxia y nefrotoxicidad.
Los estudios transversales, como la ecografía, la TC y la RMN, no se pueden utilizar para distinguir entre el cistadenoma mucinoso y el cistadenocarcinoma, a menos que el tumor haya hecho metástasis o invadido órganos vecinos. La angiografía es inespecífica e invasiva. También requiere medio de contraste yodado, con el riesgo de anafilaxia y nefrotoxicidad.
Imágenes de seguimiento
Las directrices del ACG recomiendan que se ofrezca vigilancia de quistes a candidatos aptos quirúrgicamente con quistes asintomáticos que se presume que son NPI o NCM. Todas las NPI resecadas quirúrgicamente requieren vigilancia posoperatoria, pero las NCM resecadas sin cáncer de páncreas no lo hacen. La CPRM es la modalidad preferida para la vigilancia; la EUS también puede ser la principal herramienta de vigilancia cuando las IRM están contraindicadas. En ausencia de características preocupantes que justifiquen un aumento de la vigilancia o la remisión para una evaluación adicional, el tamaño de los quistes guía los intervalos de vigilancia para los supuestos NPI y NCM.
Directrices
Las siguientes organizaciones han publicado directrices para el diagnóstico y el tratamiento de los quistes pancreáticos:
-
Colegio Americano de Gastroenterología (ACG)
-
Grupo de Estudio Europeo sobre Tumores Quísticos del Páncreas
-
Colegio Americano de Radiología (ACR)
Las pautas de ACG de 2018 recomiendan la resonancia magnética (RMN) o la colangiopancreatografía por resonancia magnética (CPRM) como la modalidad de diagnóstico preferida debido a su ausencia de invasibilidad, la falta de radiación y una mayor precisión en la evaluación de la comunicación entre el conducto pancreático principal y el quiste (que es una característica de las NIPM de rama lateral). La tomografía computarizada de protocolo pancreático (TC) o el ultrasonido endoscópico (USE) se consideraron «alternativas excelentes» si la RMN está contraindicada. Se debe considerar la aspiración con aguja fina (AAF) y el análisis del líquido quístico de la EUS en quistes en los que el diagnóstico no es claro y en los que es probable que los resultados alteren el manejo.
Se puede considerar el análisis de ACE del líquido quístico para diferenciar los NMPI y los NCM de otros tipos de quistes, pero no se puede usar para identificar los NMPI y los NCM con displasia de grado alto o cáncer de páncreas. Las IPMN o MCN con cualquiera de las siguientes características deben someterse a EUS con o sin FNA y / o ser remitidas a un grupo multidisciplinario para una evaluación posterior:
-
Cualquiera de los siguientes síntomas o signos: ictericia secundaria al quiste, pancreatitis aguda secundaria al quiste, CA sérica significativamente elevada 19-9
-
Cualquiera de los siguientes hallazgos de imágenes: la presencia de un nódulo mural o componente sólido dentro del quiste o en el parénquima pancreático, dilatación del conducto pancreático principal de >5 mm, una dilatación focal del conducto pancreático que es preocupante para la NPI del conducto principal o una lesión obstructiva, o quistes productores de mucina de ≥3 cm de diámetro
-
La presencia de displasia de alto grado o cáncer de páncreas en citología
Las directrices europeas de 2018 también recomiendan la RMN como el método preferido para el diagnóstico de neoplasias quísticas pancreáticas (NCP). Se deben considerar las imágenes multimodales en los casos en que la identificación de la calcificación es importante, para la estadificación del tumor o para el diagnóstico de la enfermedad recidivante posoperatoria. Sin embargo, la precisión sigue siendo relativamente baja para identificar el tipo específico de NCP, para diferenciar los NCP pequeños de los quistes no neoplásicos o no epiteliales, o para la conexión al sistema ductal. Se debe considerar la TC en las siguientes situaciones clínicas :
-
Para la detección de calcificación parenquimatosa, mural o central, y especialmente al diferenciar seudoquistes asociados a pancreatitis crónica de neoplasias quísticas pancreáticas
-
Cuando hay sospecha de malignidad o cáncer pancreático concomitante y cuando se requiere una evaluación de compromiso vascular, enfermedad peritoneal o enfermedad metastásica.
-
Cuando hay sospecha de recurrencia postoperatoria de cáncer de páncreas.
Las directrices europeas consideran que la EUS es útil para identificar el NCP con características que deben considerarse para la resección quirúrgica. Al igual que la RMN y la TC, la EUS tiene poca precisión para identificar el tipo exacto de NCP. El USAF mejora la precisión diagnóstica para diferenciar el NCP mucinoso frente al NCP no mucinoso, así como el NCP maligno frente al benigno, en los casos en que los hallazgos de TC o RM no están claros. Las recomendaciones adicionales para el uso de EUS-FNA incluyen las siguientes:
-
La FNA-EUS solo se debe realizar cuando se espera que los resultados cambien el manejo clínico
-
EUS-FNA no se debe realizar si el diagnóstico ya está establecido por imágenes transversales o si hay una clara indicación de cirugía
-
Las contraindicaciones relativas para el USAF en el NCP son una distancia de >10 mm entre el quiste y el transductor, la presencia de un alto riesgo de sangrado debido a un trastorno hemorrágico o el uso de medicamentos antiagregantes plaquetarios dobles