introduktion
den ensymatiske virkning af type 5 phosphodiesterase (PDE5) er den primære mekanisme til inaktivering af cGMP, nedstrøms mediator af det vasodilaterende middel (no) (Lugnier, 2006).
i løbet af erektil dysfunktion (ED) kan den nedsatte produktion af NO fra de endotel-kavernøse kar overvindes farmakologisk ved brug af PDE5-hæmmere (PDE5i) for at forlænge cGMP-halveringstiden og for at forbedre den resterende vasodilaterende funktion (Høg og Burnett, 2015). Flere molekyler med hæmmende aktivitet på PDE5 er derefter projiceret og frigivet på markedet, hvilket viser forskellig begyndelse og virkningsvarighed. I øjeblikket er PDE5i de førstevalgslægemidler, der anvendes til behandling af ED (Mehrotra et al., 2007).
på trods af en anerkendt effekt hos næsten 80% af ikke-valgte ED-patienter (Eardley et al., 2010; et al., 2010; Porst et al., 2013), er der for nylig rapporteret om et bemærkelsesværdigt Frafald fra behandlingen med PDE5i. Kvantitativt er der rapporteret om en gennemsnitlig seponeringsrate på 4% pr.måned med en samlet ophør af behandlingen i 50% tilfælde på årsbasis (Carvalheira et al., 2012; Corona et al., 2016). Blandt de vigtigste grunde, som patienterne har givet for at retfærdiggøre ophør af terapi, betegnes manglen på effektivitet og bivirkninger som den mest udbredte (Corona et al., 2016). Der kan skelnes mellem to slags bivirkninger: dem, der er strengt relateret til PDE5-hæmning, såsom hovedpine, rødme og dyspepsi, og dem, der er forbundet med resterende hæmmende aktivitet af lægemidler på anden PDE, såsom vasodilatation og takykardi (PDE1), synsforstyrrelser (PDE6) og rygsmerter (Pde11) (Bischoff, 2004; Gupta et al., 2005). Da forekomsten af bivirkninger stiger med både serumniveauer og tidseksponering for lægemidlet (Gupta et al., 2005; Taylor et al., 2009), kan et lægemiddels sikkerhed/effektivitetsprofil alternativt forbedres gennem en farmakokinetisk tilgang ved design af en ny lægemiddelformulering (Mehrotra et al., 2007). Denne tilgang er blevet anvendt med succes på PDE5i i tilfælde af Vardenafil. Faktisk lider dette molekyle af en relativt lav biotilgængelighed (prist 15%, Center for Drug Evaluation and Research, 2003). Sammenlignet med den filmovertrukne tablet (FCT), den originale formulering til klassisk per os-administration, formuleringen af oro-dispergerbare tabletter (ODT) til Vardenafil øgede lægemidlets biotilgængelighed signifikant ved at favorisere den sublinguale absorption, en rute, der erkendes at være mindre påvirket af first-pass metabolisme (Heinig et al., 2011).
Sildenafil (Sild) var den første selektive PDE5-hæmmer, der blev godkendt til behandling af ED (Boolell et al., 1996). Det er et relativt lipoilt molekyle, og efter oral administration opnås den maksimale plasmakoncentration i en tid, der varierer fra 0,5 til 2 timer. Sild viser en relativt lav oral biotilgængelighed (38-41%), hovedsageligt på grund af omfattende tarm-og førstepassemetabolisme (Gupta et al., 2005). På trods af den lange tilstedeværelse på markedet har udviklingen af nye formuleringer af lægemiddel Dårligt forfulgt, indtil den nylige frigivelse på det italienske marked af en ny formulering: Den oro-dispergerbare film (ODF). Faktisk blev ODF godkendt som en bioækvivalent form for FCT (Leoni et al., 2013). Imidlertid kan oralt desintegrerende formuleringer repræsentere egnede systemer til fordel for trans-slimhinde, og især sub-lingual, absorption (Kathpalia og Gupte, 2013).
i denne undersøgelse evaluerede vi Sild-farmakokinetikken forbundet med sublingual administration af enten ODF eller ODT i sammenligning med FCT som original pr.os-formulering. Til dette mål undersøgte vi frigivelses-/gennemtrængningsprofilen for de forskellige Sildformuleringer ved in vitro-systemer, der er specielt udviklet til at evaluere trans-slimhindeabsorption af lægemidler. Desuden kvantificerede vi serumprofilerne for Sild-farmakokinetik efter administration af per os FCT og sublingual ODT og ODF hos patienter med ED.
materialer og metoder
kemikalier og lægemiddelformuleringer
Hank ‘ s balance salts solution pH 7.4 (HBSS), HEPES–opløsning og Sildcitrat blev alle købt hos Sigma-Aldrich (Milano, Italien). For at undgå forvirrende resultater som følge af brugen af alternative bioækvivalente produkter, der er tilgængelige på markedet, blev følgende produkter anvendt: Cialis (Cialis, Italien), Cialis (Cialis, Italien), Cialis (Cialis, Italien) og Cialis (IBSA, Lodi, Italien). Narkotika blev ordineret til patienter under ambulant evaluering til deres private brug. Til in vitro-test og in vivo evaluering af farmakokinetik (se nedenfor) blev lægemidler specifikt købt af personale involveret i undersøgelsen på lokale apoteksfaciliteter og derefter håndteret/opbevaret under optimale forhold.
Disaggregationstest
in vitro disaggregationstestene blev udført i henhold til European Pharmacopoeia (2016) ved anvendelse af tablet Disintegrationstesteren (Sotaks dt 2, supplerende figur S1A) ved anvendelse af vand som nedsænkningsvæske ved 37 liter 0,5 liter C. disaggregeringstidspunktet blev kontrolleret ved fuldstændig opløsning af doseringsformen. Fuldstændig opløsning defineres som den tilstand, hvor enhver rest af enheden, der er tilbage på testapparatets skærm eller klæber til diskens nedre overflade, er en blød masse, der ikke har nogen håndgribelig fast kerne. Test blev udført i tre eksemplarer,og resultaterne blev rapporteret som middelværdi-standardafvigelse.
opløsningstest
in vitro-lægemiddelopløsningstest blev udført i henhold til European Pharmacopeia . Opløsningstestene blev udført ved hjælp af et padleapparat, padlehastighed 50 omdr. / min., og HBSS pH 7,4 blev anvendt som opløsningsmediumvolumen (900 ml ved 37 liter 0,5 liter C).
under frigivelsestestene, 2 ml opløsningsmediumprøve, ved 0, 2, 4, 6, 10, 20, 30, og 40 min, blev fjernet og filtreret gennem 0,45 liter celluloseestere filter og dermed fortyndet. Efterfølgende blev Sild-kvantificering udført ved højtydende væskekromatografi (HPLC)-UV. Det fjernede volumen blev udskiftet hver gang med frisk medium. Test blev udført i tre eksemplarer,og resultaterne blev rapporteret som middelværdi-standardafvigelse. Data blev normaliseret på lægemiddelindholdet i formuleringen.
Trans-mucosal Permeationstest
Trans-mucosal permeationsprofil af Sild blev evalueret in vitro ved anvendelse af en specifik enhed ifølge Delvadia et al. (2012) passende ændret. Kort sagt bestod enheden i et lodret diffusionssystem fremhævet af donor–modtagerkamre adskilt af en engangscellulose–acetatmembran (pore 0,45 liter). Donorcellen indeholdt 1,5 ml HBSS, hvorimod modtagerkammeret var en del af et lukket recirkulationskredsløb på 30 ml inklusive mængderne af rør og reservoir. Prøveudtagning blev udført fra modtagerkammerreservoir med tidsintervaller for 0, 5, 10, 20, 30, og 40 min og erstattet af et tilsvarende volumen frisk HBSS. Prøverne blev analyseret af HPLC-UV for lægemiddelindhold (fej Karts et al., 2014). Data blev normaliseret på den højeste gennemsyrede Sildkoncentration observeret for rent Sildcitrat. Test blev udført i tre eksemplarer,og resultaterne blev rapporteret som middelværdi-standardafvigelse.
farmakokinetisk undersøgelse af frivillige psykogene ED-patienter
undersøgelsen blev udført i enheden for Andrologi og Reproduktiv Medicin (Universitetshospital i Padova, Italien) mellem maj og September 2017 i henhold til Helsinki-erklæringen under godkendelse af Etikudvalget for Padova Universitetshospital (protokol nummer 3982/AO/16 og efterfølgende ændringer). For at undgå forvirrende resultater blev forsøgspersoner med psykogen ED indskrevet, fordi den lavere forekomst af organiske derangements associeres med ED (Ludvig og Phillips, 2014).
stikprøvestørrelsen blev beregnet for at opnå en effektstørrelse på mindst 0,5 med en statistisk effekt på 0,8 og et signifikansniveau på 0,05 for en sammenligning af tre grupper (se strømberegner – envejsuafhængig ANOVA).
tyve patienter (gennemsnitsalder 31, 4 i forhold til 5, 7 år) blev fortløbende tilmeldt ved frigivelse af underskrevet informeret samtykke. Patienter deltog i ambulant evaluering, der rapporterede om den konsekvente manglende evne til at opnå og opretholde en erektion til tilfredsstillende samleje i løbet af det foregående 6 måneder eller mere. Efterfølgende klinisk evaluering blev udført hos alle patienter for at fastslå fraværet af sygdomme relateret til ED, såsom diabetes mellitus, hypertension, neurologisk lidelse og brugen af antidepressiva. Diagnose af psykogen ED blev bekræftet ved opfyldelsen af en indeksscore <26 ved administrationen af det internationale indeks for erektil funktion-15 (IIEF-15) spørgeskema (Lotti et al., 2016) og vedligeholdelse af natlige spontane erektioner, vurderet ved natlig penile Tumescence og Stivhedsovervågning gennem RigiScan Plus Stivhedsvurderingssystem (Dacomed, USA) i to på hinanden følgende nætter som tidligere beskrevet., 1993; Caretta et al., 2005). Eksklusionskriterier var diagnose af maligniteter, unormale hormonplasmaniveauer (henholdsvis luteiniserende hormon > 8 UI/l, total testosteron <10, 4 nmol/l, thyrotropin >4, 5 mUI/l, prolactin >20 ng/ml) og øget intima-medietykkelse ved Supra-aortastammer (>0.9 mm) og/eller kavernøse arterier (>0,3 mm), vurderet ved farve Doppler-ultralyd som tidligere beskrevet (Caretta et al., 2005, 2009).
patienter blev enige om at overholde en enkeltdosis, trevejs crossover åben undersøgelse. Lægemiddeldoseringsskema er rapporteret i Figur 1. Doseringen af Sild blev valgt som 50 mg i overensstemmelse med tidligere rapporter om behandling af psykogen ED (Banner and Anderson, 2007). Patienter blev bedt om ikke at tage stoffer eller alkohol i 1 uge før og i løbet af undersøgelsen. Desuden blev patienter i løbet af dagen med lægemiddeldosering også bedt om at spise en ikke-fed morgenmad (ingen mælk eller anden fedt mad) mindst 2 timer før testen. FCT, betragtet som referenceformulering, blev klassisk administreret per os ved at sluge den orale tablet med et glas vand. For ODT og ODF blev patienterne instrueret om at holde formuleringen under tungen i 15 minutter uden antagelse af vand efterfulgt af indtagelse. Venøse blodprøver blev indsamlet i standardrør (Vacutainer, BD Biosciences, Milano, Italien) kl 0, 5, 10, 15, 30, 60, 90, 120, og 240 minutter efter lægemiddeladministration. Kompensation gennem kontinuerlig infusion af steril saltopløsning blev udført. Efter doseringen blev forsøgspersoner anbragt, indtil blodprøveudtagningen var afsluttet. En yderligere blodudtagning blev udført ved 24 timer fra dosering af kontrolårsager for at fastslå den komplette lægemiddelclearance. Som udvaskningsperioder blev der tilladt 7 dage mellem en dosering og følgende. Efter blodopsamling blev plasma straks isoleret og opbevaret ved -80 liter C indtil brug.
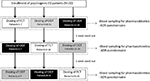
FIGUR 1. Doseringsskema og vurderinger til evaluering af farmakokinetiske parametre hos 20 patienter med psykogen erektil dysfunktion (ED), opdelt i tre grupper (henholdsvis patienter 1-7, patienter 8-14 og patienter 15-20). Hver patientgruppe fik alternativt per os Filmovertrukket tablet (FCT), sublingual oro-dispergerbar tablet (ODT) eller sublingual oro-dispergerbar film (ODF) med mindst 1 uges udvaskning fra hver dosering. Alle formuleringer indeholdt 50 mg sildenafil (Sild).
under huset blev patienter også anmodet om at registrere bivirkninger (ADR) i en specifikt udtænkt form, tilpasset fra ADR-rapporteringsformen for Agencia Italiana del Farmaco (aifa1). En oversat udgave af spørgeskemaet er tilgængelig som supplerende materiale (se supplerende datablad S1). Patienterne blev bedt om at specificere typen af bivirkninger, den samlede intensitet (i en subjektiv vurderingsskala fra 1, meget svag, til 5, meget intens), tidspunktet for indtræden og den samlede varighed.
kvantificering af Sildenafil i humant Serum
til kvantificering af serumniveauer af Sild blev der tilsat 400 liter serumprøve af 500 liter methanol suppleret med den interne standard (is). Derefter blev 5 ml ethylacetat tilsat til blandingen, prøverne blev virvlet for at udføre væske–væskeekstraktion, de to faser blev adskilt ved centrifugering. Den organiske del blev derefter fordampet under vakuumcentrifuge ved 40 liter C. Den opnåede rest blev opløst igen med 200 liter methanol og til sidst anvendt til højtydende væskekromatografi-tandem massespektrometri (HPLC-MS/MS) analyse.
højtydende væskekromatografi-MS/MS-analyse anvendte et system Agilent-Varian 1260, og den tredobbelte firdobbelt detektor Agilent-Varian 320 Ms. kromatografisk adskillelse blev udført på en søjlefænomeneks C-18 Evo 3 K100 og en mobil fase bestående af acetonitril med 0,1% myresyre i vand med en gradient beskrevet i supplerende figur S2A. En positiv detektionsmodus blev anvendt til overgangen 198 > 105 da af IS, opnået med en kapillærspænding på 40 V og en kollisionsenergi på 16 V, mens 475 > 100 Da for Sild med kapillærspænding på 40 V og en kollisionsenergi på henholdsvis 22,5 v. Repræsentative kromatogrammer af IS og Sild i reelle prøver er rapporteret i supplerende figur S2B.
statistisk analyse
farmakokinetiske parametre (PK), såsom maksimal serumkoncentration (Cmaks), tid til maksimal serumkoncentration (tmaks) og areal under kurven (AUC) på forskellige tidspunkter, blev beregnet med specifikke rutiner for applikationer med GraphPad-programmer (La Jolla, CA, USA). Statistisk analyse af data blev udført med SPSS 21.0 for vinduer (SPSS, Chicago, IL, USA). Kolmogorov-Smirnov-testen blev brugt til at kontrollere for normalitet i distributionen. Variabler, der ikke viser normalfordeling, blev logtransformeret. Baseline-karakteristika for patienter, PKs og data fra in vitro-eksperimenter blev sammenlignet med uparrede studerendes t–test med Bonferroni-Holm-korrektion for flere sammenligninger. Gentagne målinger ANOVA blev udført for at teste forskelle i lægemiddelfrigivelse og Sildserumkoncentration. Levenes test blev brugt til at teste homogeniteten af varians blandt grupper. Hvis homogeniteten af variansantagelsen blev overtrådt, blev der udført en test, og den respektive P-værdi blev rapporteret. Andelen af ADR blev sammenlignet med den nøjagtige stikprøve af prip2. P-værdier < 0.05 blev betragtet som statistisk signifikante.
resultater
in Vitro-analyse af frigivelse/gennemtrængning af Sildenafil fra de forskellige lægemiddelformuleringer
dynamikken i frigivelse og gennemtrængning af Sild fra de tre lægemiddelformuleringer blev tidligere undersøgt in vitro (figur 2). Tiden til fuldstændig opdeling for FCT, ODT og ODF blev evalueret ved hjælp af en standardtest beskrevet i European Pharmacopoeia (2016; figur 2a). ODF viste den højeste tid til disaggregering sammenlignet med både FCT og ODT (henholdsvis P = 0,017 og P = 0,008).
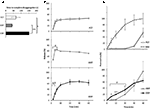
FIGUR 2. In vitro evaluering af bioteknologiske egenskaber hos FCT ‘er, ODT’ er og andodf ‘ er indeholdende 50 mg Sild. Resultaterne er repræsentative for tre uafhængige eksperimenter og rapporteres som middelværdier af standardafvigelsen. A) resultaterne af disaggregationstesten med angivelse af tiden (i sekunder) til den fuldstændige disaggregering af formuleringen. Betydning: p < 0,05 og p < 0,01 mellem de angivne formuleringer. (B) resultater af opløsningstesten, der rapporterer mængden af Sild frigivet af hver formulering som procentdel af lægemidlets dosering. Betydning: aP < 0,01 vs. FCT; bP < 0,001 vs. ODT. C) resultater af gennemtrængningsprøven (nærmere beskrevet i afsnittet “Materialer og metoder”), der rapporterer mængden af Sild, der er gennemtrængt gennem en celluloseacetatmembran, i procent af den højeste værdi opnået med 50 mg rent Sildpulver (diskontinuerlig linje i det øverste panel). Betydning: larp P < 0,05 vs. ODT; LARP P < 0,01 vs. ODT; ap < 0,01 vs. FCT.
for at evaluere indflydelsen af dette bevis på lægemiddelfrigivelsen fra formuleringen blev der udført en standardopløsningstest (European Pharmacopoeia, 2016; figur 2b). Sammenlignet med referenceformuleringen FCT viste ODT en hurtigere frigivelse af lægemidlet, hvis maksimale omfang blev opnået selv efter kun 2 minutter fra testens begyndelse (P = 0,006 vs. FCT). På den anden side var procentdelen af lægemidlet frigivet fra ODF inden for de første 4 minutter af analysen lavere sammenlignet med både FCT og ODT (henholdsvis P = 0,004 og P < 0,001). Især viste ODF en mere progressiv frigivelse af lægemidlet sammenlignet med FCT og opnåede det maksimale omfang efter 20 minutter fra testens begyndelse.
på dette grundlag blev trans-slimhindepermeationen af Sild fra hver formulering vurderet ved hjælp af en specifikt udviklet enhed (figur 2C). Til referenceformål blev ren Sildcitrat, anvendt i en vægt svarende til 50 mg Sild, vurderet for trans-slimhindepermeation og viste fri og hurtig diffusion mellem de to kamre. En næsten modsat profil blev observeret for FCT, der viste en ubetydelig gennemtrængning indtil 30 minutter fra testens begyndelse. Gennemtrængningsprofilerne for ODT og ODF viste en mellemadfærd sammenlignet med de to foregående betingelser. Inden for de første 20 minutter af analysen viste ODF en signifikant højere grad af permeation sammenlignet med ODT (henholdsvis P = 0,033 ved 5 min, P = 0,003 ved 10 min og P = 0,041 ved 20 min). Forskelligt fra FCT og ODT, der fuldstændigt blev opdelt i donorkammeret, fortsatte en resterende soft-jelly-masse af ODF på celluloseacetatmembran selv i slutningen af analysen (supplerende figur S2C).
differentiel farmakokinetik af Sildenafil
tyve mandlige forsøgspersoner påvirket af psykogen de accepteret at modtage alternativt FCT, ODT eller ODF, adskilt af en uges udvaskning. Som beskrevet i afsnittet” Materialer og metoder ” blev FCT klassisk slugt for at tillade den klassiske per os-administration, mens ODT og ODF blev opretholdt under tungen i 15 minutter for at fremme den sublinguale rute. Kliniske karakteristika hos patienter er rapporteret i tabel 1. Serumniveauer af Sild svarende til de tre doseringsbetingelser er rapporteret i figur 3. En betydelig variation indeholdt lægemiddelserumprofilen for de tre formuleringer. Sammenlignet med FCT viste ODT en tilsyneladende tidlig stigning i Sildserumniveauer; denne tendens var imidlertid ikke statistisk signifikant. På den anden side blev der observeret et hurtigere henfald af Sildniveauer ved 120 og 240 minutter fra dosering for ODT-formuleringen (henholdsvis P = 0,044 og P = 0,024 vs. FCT).
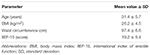
TABEL 1. Kliniske egenskaber hos undersøgelsesdeltagerne (N = 20).
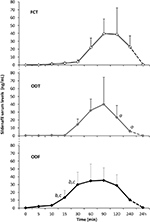
FIGUR 3. In vivo evaluering af serumniveauer af Sild hos 20 patienter, der er ramt af psykogen ED, modtager alternativt enten FCT per os eller den sublinguale ODT eller den sublinguale ODF som beskrevet i afsnittet “Materialer og metoder.”Data indberettes som middelværdier af en værdi af standardafvigelsen: ap < 0,05 vs. FCT; bP < 0,01 vs. FCT; cP < 0,05 vs. ODT.
LÆGEMIDDELSERUMPROFILEN for ODF-formuleringen viste en hurtigere stigning i Sildniveauer sammenlignet med både FCT (P = 0, 001 og P = 0, 003) og ODT (P = 0, 048 og P = 0, 041) henholdsvis 15 og 30 minutter fra dosering. I overensstemmelse med dens langsomme disaggregeringstid in vitro (figur 2b) var ODF ‘s gennemsnitlige koncentrations–tidskurve in vivo glattere end FCT og ODT’ s (figur 3).
farmakokinetiske parametre for de tre formuleringer opnået ved analysen af Sildserumniveauer er opsummeret i tabel 2. På trods af at der ikke blev observeret nogen signifikant forskel mellem de tre formuleringer med hensyn til Cmaks, TMAKS og AUC0-240 min, udviste ODF den laveste værdi af Cmaks (38,2 liter 23,7 ng/ml) og den korteste tmaks (70,0 liter 24,5 minutter). Især viste ODF en signifikant højere værdi af AUC0 – 60 min sammenlignet med både FCT og ODT (henholdsvis P = 0,005 og P = 0.043), hvilket resulterer i en øget relativ biotilgængelighed af Sild inden for den første time efter dosering af ODF gennem den sublinguale vej.

TABEL 2. Farmakokinetiske parametre for sildenafilformuleringer.
bivirkninger
resultater opnået fra det selvadministrerede spørgeskema om typen og træk ved ADR, som forsøgsdeltagerne oplever, er opsummeret i tabel 3. Blandt de kendte ADR rapporteret for Sild (Taylor et al., 2009), var de hyppigst registrerede hovedpine, rødmen og næsestop. En patient rapporterede muskelsmerter i lav grad (grad 1 på den subjektive vurderingsskala) efter dosering af FCT. Ingen af patienterne rapporterede ændret syn, takykardi, svaghed eller ændret hørelse.

TABEL 3. Bivirkninger registreret af undersøgelsesdeltagerne (N = 20).
sammenlignet med FCT som referenceformulering viste ODT uvarieret prævalens af ADR. Den personlige opfattelse af skylleintensitet var imidlertid signifikant lavere (P = 0,031). På den anden side viste ODF en reduceret forekomst af hovedpine sammenlignet med FCT (P = 0,043). Desuden blev varigheden og intensiteten af rødmen og næsestop opfattet på lavere niveauer sammenlignet med både FCT (henholdsvis P = 0,011 og P = 0,015) og ODT (henholdsvis P = 0,026 og P = 0,037).
Diskussion
i denne undersøgelse giver vi bevis for, at den sublinguale rute for Sildadministration associeres med en øget tidlig lægemiddel biotilgængelighed og forbedret tolerabilitetsprofil. Dette bevis understøttes af begge in vitro-undersøgelser, der viser, at Sildformuleringen er kendetegnet ved længere tid til opdeling, men signifikant favoriseret trans-slimhindeabsorption og in vivo-beviser.
phosphodiesterasehæmmere er den første valg terapeutiske mulighed til behandling af ED; bivirkninger, som patienter oplever, anerkendes dog som den mest udbredte årsag til seponering af behandlingen (Corona et al., 2016). Ændring af farmakokinetik gennem design af ny lægemiddelformulering kan repræsentere en attraktiv strategi til forbedring af sikkerhed/effektivitetsprofilen for selve lægemidlet (Mehrotra et al., 2007). I denne henseende tillod 2013-udløbet af patentet på Sildcitrat i flere europæiske lande muligheden for at frigive en række nye formuleringer af Sild. Det skal bemærkes, at de fleste af de Sildformuleringer, der findes på markedet i dag, faktisk er godkendt som bioækvivalente former for den originale FCT (Leoni et al., 2013). Interessant nok er der udviklet oralt desintegrerende formuleringer, der fremgår af hurtig opdeling i patientens mund uden behov for at sluge med vand (Goel et al., 2008). Disse nye formuleringer finder forbedret overensstemmelse i de populationer af patienter med vanskeligheder med at sluge konventionelle faste doser, såsom børn, geriatriske patienter og dysfagiske patienter. Derudover kan oralt desintegrerende formuleringer ved at tilvejebringe højere oral lægemiddeltilgængelighed repræsentere værdsatte systemer til fordel for trans-slimhinde, og især sub-lingual, absorption (Kathpalia og Gupte, 2013). Især i Italien er to oralt desintegrerende formuleringer af Sild officielt tilgængelige på apotekets faciliteter: ODTs og ODFs.
i denne undersøgelse havde vi til formål at evaluere de mulige farmakokinetiske variationer og det tilsvarende mønster af ADR, der stammer fra at favorisere trans-mucosal absorption af Sild gennem sub-lingual administration af de to tilgængelige oralt desintegrerende formuleringer af lægemidlet. Resultaterne blev sammenlignet med den oprindelige formulering af Sild, nemlig FCT ‘ erne. Interessant nok fandt vi en streng sammenhæng, både in vitro og in vitro, mellem de bioteknologiske egenskaber og PKs af de forskellige formuleringer. Især på trods af en lige lægemiddeldosis (50 mg) og let reduceret lægemiddelfrigivelse i opløsningstesten blev ODF karakteriseret ved en større tid til disaggregering og højere gennemtrængningshastighed i trans-slimhindemodellen på den ene side og ved en øget lægemiddelbiotilgængelighed inden for den første time fra dosering på den anden side. Vi kan så antage, at sub-lingual Sildabsorption er begunstiget af en langvarig lægemiddel-slimhindekontakt. Faktisk forfølges dette fænomen generelt for orale trans-mucosale lægemidler, hvor brugen af mucoadhesive polymerer anbefales for at sikre langvarig kontakt mellem formuleringen og mundslimhinden (Lam et al., 2014), især fra disse lægemidler, som Sild, påvirket af lav vandopløselighed (Sayed et al., 2012; Sun et al., 2014). Disse foreløbige resultater tyder også på en mulig forbedring af den kliniske effekt for denne klasse af lægemidler sammenlignet med originale formuleringer. Yderligere undersøgelser er berettiget til at afklare disse aspekter.
det mest slående bevis for denne undersøgelse er en signifikant reduktion i ADR’ erne for sublingual administration af ODF sammenlignet med ODT og FCT administreret i samme dosis, hvilket igen kan resultere i øget patienters overholdelse. Dette bevis kan fortolkes i lyset af princippet om, at forekomsten af en lægemiddelbivirkning øges ved at øge serumniveauerne og eksponeringstiden for selve lægemidlet (Gupta et al., 2005; Taylor et al., 2009). På trods af en uvarieret global biotilgængelighed sammenlignet med de andre analyserede formuleringer viste den sublinguale administration af ODF en lavere værdi af Cmaks og en kortere tmaks, hvilket resulterede i en signifikant højere andel Sild biotilgængelig inden for den første time efter dosering. Således kan vi spekulere i, at den sub-lingual administration af ODF kombinerer en effektiv absorption af lægemidlet med opnåelse af gennemsnitlige lavere serumniveauer af Sild og en deraf følgende lavere risiko for bivirkninger. Vi anerkender dog den lave stikprøvestørrelse som den største ulempe ved undersøgelsen. Yderligere undersøgelse af større kohorter og med forskellige doser er påkrævet for at bekræfte dette problem.
afslutningsvis rapporterer vi i denne undersøgelse, at sublingual administration af Sild ODF forbedrer lægemiddeltoleranceprofilen gennem den sandsynlige involvering af en modificeret farmakokinetik sammenlignet med generator FCT ‘ er. Selvom ODF ikke oprindeligt blev udtænkt til dette formål, repræsenterer dette en attraktiv strategi for at forbedre patientens overholdelse af terapi. Vi udvikler yderligere sammenlignende undersøgelser for at vurdere den kliniske effekt hos psykogene og organiske ED-patienter.
Forfatterbidrag
LDT og CF koordinerede studiet og udarbejdede manuskriptet. MDRP evaluerede og inkluderede patienterne. EF udførte in vitro-analyse. SDA udførte serumanalysen. RP udførte farmakokinetisk sammenligning. RP, nr og AG reviderede og færdiggjorde manuskriptet kritisk.
interessekonflikt Erklæring
forfatterne erklærer, at forskningen blev udført i mangel af kommercielle eller økonomiske forhold, der kunne fortolkes som en potentiel interessekonflikt.
anerkendelser
vi takker Dr. Alberto Barosso, Dr. Giuseppe Maggioni og Dr. Dimitri Portale for patientrådgivning, Dr. Flavia Rosano og Dr. Alice Passadore for patienter, der administrerer, og alt personale i enheden for Andrologi og Reproduktiv Medicin.
supplerende materiale
det supplerende materiale til denne artikel kan findes online på: https://www.frontiersin.org/articles/10.3389/fphar.2018.00059/full#supplementary-material
figur S1 / repræsentative billeder af tablet-Disintegrationstesteren (A) og Opløsningsapparatet (B), der anvendes til disaggregeringstest og opløsningstest.
figur S2 |(a) detaljer om den mobile fasegradient, der anvendes til højtydende væskekromatografi-tandem massespektrometri (HPLC-MS/MS) analyse af serumniveauer af sildenafil (Sild). Der rapporteres repræsentative kromatogrammer og massespektre for begge Sild ved den interne standard i reelle prøver (B). C) repræsentativt billede af resterende orodispersibel film (fremhævet med en diskontinuerlig linje), der vedvarer efter gennemtrængningstesten i det udstyr, der anvendes til in vitro-estimatet af trans-slimhindeabsorption gennem en celluloseacetatmembran.
datablad S1 | spørgeskema for bivirkninger.
fodnote
- ^http://www.aifa.gov.it/en/content/reporting-adverse-reaction
Banner, L. L. og Anderson, R. U. (2007). Integreret sildenafil og kognitiv adfærd køn terapi for psykogen erektil dysfunktion: en pilotundersøgelse. J. Køn. Middelhavs. 4, 1117–1125. doi: 10.1111 / j. 1743-6109.2007.00535.
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
Bischoff, E. (2004). Styrke, selektivitet og konsekvenser af ikke-selektivitet af PDE-hæmning. Int. J. Impot. Res. Suppl. 1, S11-S14. doi: 10.1038 / sj.ijir.3901208
PubMed abstrakt | CrossRef Fuld tekst | Google Scholar
Boolell, M., Allen, M. J., Ballard, S. A., Gepi-Attee, S., Muirhead, G. J., Naylor, A. M., et al. (1996). Sildenafil: en oralt aktiv type 5 cyklisk GMP-specifik phosphodiesterasehæmmer til behandling af erektil dysfunktion i penis. Int. J. Impot. 8, 47-52.
PubMed abstrakt / Google Scholar
Caretta, N., Palego, P., Ferlin, A., Garolla, A., Bettella, A., Selice, R., et al. (2005). Genoptagelse af spontane erektioner hos udvalgte patienter, der er ramt af erektil dysfunktion og forskellige grader af carotisvægsændring: tadalafils rolle. EUR. Urol. 48, 326–331. doi: 10.1016 / j. eururo.2005.01.013
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
Caretta, N., Palego, P., Schipilliti, M., Ferlin, A., Di Mambro, A. og Foresta, C. (2009). Cavernous arterie intima-medietykkelse: en ny parameter i diagnosen vaskulær erektil dysfunktion. J. Køn. Middelhavs. 6, 1117–1126. doi: 10.1111 / j. 1743-6109.2008. 01112.
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
Carvalheira, A. A., Pereira, N. M., Maroco, J. og Forjas, V. (2012). Frafald i behandlingen af erektil dysfunktion med PDE5: en undersøgelse af forudsigere og en kvalitativ analyse af årsagerne til seponering. J. Køn. Middelhavs. 9, 2361–2369. doi: 10.1111 / j. 1743-6109.2012. 02787.
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
Center for Lægemiddelvurdering og forskning (2003). Nda 021400 Levitra (Vardenafilhydrochlorid) tabletter: Klinisk Farmakologi / Biofarmaceutisk Gennemgang. Rockville, Md: Institut for sundhed og menneskelige tjenester. Silver Spring, MD: Food and Drug Administration.
Google Scholar
Corona, G., Rastrelli, G., Burri, A., Serra, E., Gianfrilli, D., Mannucci, E., Et Al. (2016). Første generation phosphodiesterase type 5 hæmmere frafald: en omfattende gennemgang og meta-analyse. Andrologi 4, 1002-1009. doi: 10.1111 / andr.12255
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
Delvadia, P. R., Barr, H. H. og Karnes, H. T. (2012). A biorelevant in vitro release/permeation system for oral transmucosal dosage forms. Int. J. Pharm. 430, 104–113. doi: 10.1016/j.ijpharm.2012.03.050
PubMed Abstract | CrossRef Full Text | Google Scholar
Eardley, I., Donatucci, C., Corbin, J., El-Meliegy, A., Hatzimouratidis, K., McVary, K., et al. (2010). Pharmacotherapy for erectile dysfunction. J. Sex. Med. 7, 524–540. doi: 10.1111/j.1743-6109.2009.01627.x
PubMed Abstract | CrossRef Full Text | Google Scholar
European Pharmacopoeia (2016). Det Europæiske Direktorat for lægemiddelkvalitet &sundhedspleje (EDM), 9.udgave. Strasbourg: Europarådet.
Google Scholar
fej kryss, I., Neumajer, G., B Krysni, S. og Jankovics, P. (2014). Kvalitativ og kvantitativ analyse af PDE-5-hæmmere i forfalskede lægemidler og kosttilskud af HPLC-UV ved anvendelse af sildenafil som eneste reference. J. Pharm. Biomed. Anal. 98, 327–333. doi: 10.1016 / j. jpba.2014.06.010
PubMed abstrakt | CrossRef Fuld tekst | Google Scholar
Rai, P., Rana, V. og Tivary, A. K. (2008). Mundtligt desintegrerende systemer: innovationer inden for formulering og teknologi. Seneste Pat. Drug Deliv. Formel. 2, 258–274. doi: 10.2174/187221108786241660
CrossRef fuldtekst / Google Scholar
Gupta, M., Kovar, A. og Meibohm, B. (2005). Den kliniske farmakokinetik af phosphodiesterase – 5-hæmmere til erektil dysfunktion. J. Clin. Pharmacol. 45, 987–1003. doi: 10.1177/0091270005276847
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
K., Amar, E., Eardley, I., Giuliano, F. D., Montorsi, F., et al. (2010). Den Europæiske Sammenslutning af urologi. Retningslinjer for mandlig seksuel dysfunktion: erektil dysfunktion og for tidlig sædafgang. EUR. Urol. 57, 804–814. doi: 10.1016 / j. eururo.2010.02.020
PubMed abstrakt | CrossRef Fuld tekst | Google Scholar
D. J. og Burnett, A. L. (2015). Farmakoterapeutisk behandling af erektil dysfunktion. Clin. Pharmacol. Ther. 98, 602–610. doi: 10.1002 / cpt.261
PubMed Abstrakt / CrossRef Fuld Tekst / Google Scholar
Heinig, R., Vimann, B., Dietrich, H., Og B. Krettcher, M. F. (2011). Farmakokinetikken for en ny smeltetabletformulering af vardenafil: resultater af tre kliniske forsøg. Clin. Drug Investig. 31, 27–41. doi: 10.2165/11584950-000000000-00000
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
Kathpalia, H. og Gupte, A. (2013). En introduktion til hurtig opløsning af orale tyndfilmslægemiddelafgivelsessystemer: en gennemgang. Curr. Drug Deliv. 10, 667–684. doi: 10.2174/156720181006131125150249
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
(2014). Oral transmucosal lægemiddelafgivelse til pædiatrisk brug. Adv. Drug Deliv. Åb 73, 50-62. doi: 10.1016 / j.addr.2013.08.011
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
Leoni, L. A., Leite, G. S., Vichi, R. B. og Rodrigues, B. (2013). Sildenafil: to årtiers fordele eller risici? Aldrende Mand 16, 85-91. doi: 10.3109 / 13685538.2013.801952
PubMed abstrakt | CrossRef Fuld tekst | Google Scholar
Lotti, F., Corona, G., Castellini, G., Maseroli, E., Fino, M. G., Cosolino, M., et al. (2016). Sædkvalitetsnedsættelse er forbundet med seksuel dysfunktion i henhold til dens sværhedsgrad. Hum. Reprod. 31, 2668–2680. doi: 10.1093 / humrep / dug 246
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
Phillips, M. (2014). Organiske årsager til erektil dysfunktion hos mænd Under 40 år. Urol. Int. 92, 1–6. doi: 10.1159/000354931
PubMed Abstrakt / CrossRef Fuldtekst / Google Scholar
Lugnier, C. (2006). Cyklisk nukleotidphosphodiesterase (PDE) superfamilie: et nyt mål for udvikling af specifikke terapeutiske midler. Pharmacol. Ther. 109, 366–398. doi: 10.1016 / j.pharmthera.2005.07.003
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
Mehrotra, N., Gupta, M., Kovar, A. og Meibohm, B. (2007). Farmakokinetikkens og farmakodynamikens rolle i phosphodiesterase-5-hæmmerbehandlingen. Int. J. Impot. Res. 19, 253-264. doi: 10.1038 / sj.ijir.3901522
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
Bancroft, J. Og Marshall, I. (1993). Udførelsen af Rigiscan i måling af penis tumescence og stivhed. Int. J. Impot. Res. 5, 69-76.
Google Scholar
Porst, H., Burnett, A., Brock, G., Ghanem, H., Giuliano, F., Glina, S., et al. (2013). ISSM Standards Committee for Seksuel Medicin. SOP konservativ (medicinsk og mekanisk) behandling af erektil dysfunktion. J. Køn. Middelhavs. 10, 130–171. doi: 10.1111 / jsm.12023
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
Fang, F., Ren, M., Lou, H., Et Al. (2014). Forbedret oral absorption og terapeutisk virkning af acetylpuerarin baseret på D-Kurt-Tocopheryl polyethylenglycol 1000 succinat nanoemulsioner. Int. J. Nanomedicin 9, 3413-3423. doi: 10.2147 / IJN.S63777
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
Taylor, J., Baldo, O. B., Storey, A., Cartledge, J. og Eardley, I. (2009). Forskelle i bivirkningsvarighed og relaterede generende niveauer mellem phosphodiesterase type 5-hæmmere. BJU Int. 103, 1392–1395. doi: 10.1111 / j. 1464-410H.2008. 08328.
PubMed abstrakt / CrossRef Fuld tekst / Google Scholar
A. O., Shukr, M. og El-Shamy, A. H. (2012). En in vitro og in vivo sammenlignende undersøgelse af direkte komprimerede faste dispersioner og frysetørrede sildenafilcitrat sublinguale tabletter til behandling af pulmonal arteriel hypertension. Acta Pharm. 62, 411–432. doi: 10.2478/v10007-012-0027-9
PubMed Abstract | CrossRef Full Text | Google Scholar