L’elemento chimico nihonium è classificato come un altro metallo. È stato scoperto nel 2012 dal team collaborativo RIKEN di Kosuke Morita.

Dati Zona
| Classificazione: | Nihonium è un ‘altra di metallo’ (presunta) |
| peso Atomico: | (286), no isotopi stabili |
| Stato: | > solido (presunta) |
| punto di Fusione: | |
| punto di Ebollizione: | |
| Elettroni: | 113 |
| Protoni: | 113 |
| Neutroni in isotopo più abbondante: | 173 |
| gusci di Elettroni: | 2, 8, 18, 32, 32, 18, 3 |
| configurazione elettronica: | 5f14 6d10 7s2 7p1 |
Mostra più, tra cui: Riscalda, Energie, Ossidazione,
Reazioni, Composti, Raggi, Conducibilità
| capacità termica Specifica | – |
| Calore di fusione | – |
| Calore di atomizzazione | – |
| Calore di vaporizzazione | – |
| 1 energia di ionizzazione | – |
| 2 energia di ionizzazione | – |
| 3 energia di ionizzazione | – |
| affinità elettronica | – |
| Minimum oxidation number | – |
| Min. common oxidation no. | – |
| Maximum oxidation number | – |
| Max. common oxidation no. | – |
| Elettronegatività (Pauling Scala) | – |
| Polarizability volume | – |
| Reazione con l’aria | – |
| Reazione con 15 M di HNO3 | – |
| Reazione con 6 M di HCl | – |
| Reazione con 6 M di NaOH | – |
| Ossido di(s) | – |
| Idruro(s) | – |
| Cloruro di(s) | – |
| Atomic radius | – |
| Ionic radius (1+ ion) | – |
| Ionic radius (2+ ion) | – |
| Ionic radius (3+ ion) | – |
| Ionic radius (1- ion) | – |
| Ionic radius (2- ion) | – |
| Ionic radius (3- ion) | – |
| Thermal conductivity | – |
| Electrical conductivity | – |
| Punto di congelamento / fusione: | – |

Nihonium è stato prodotto in un acceleratore di particelle. Immagine: LLNL.
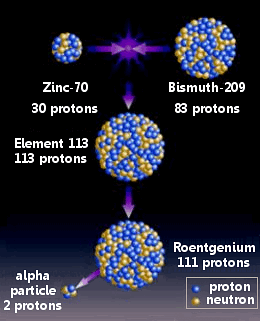
Nihonium è stato fatto combinando zinco-70 con bismuto-209 in un reation nucleare.
Scoperta di Nihonium
Nihonium è stato scoperto il 12 agosto 2012 dal team collaborativo RIKEN di Kosuke Morita in Giappone. E ‘ stato il primo elemento chimico mai scoperto in Asia.
La scoperta è stata formalmente accettata il 30 dicembre 2015 da IUPAC e IUPAP, e un nuovo elemento superpesante ha preso il suo posto nella settima riga della tavola periodica.
L’elemento prende il nome dal luogo in cui è stato sintetizzato per la prima volta; Nihon è uno dei due modi per dire Giappone in giapponese.
Nihonium è stato realizzato utilizzando l’acceleratore lineare di RIKEN e il separatore di ioni GARIS a Wako, in Giappone. L’isotopo prodotto era nihonium-278, che non si blocca a lungo: la sua emivita è inferiore a un millesimo di secondo.
Il team di Morita aveva iniziato il suo lavoro nel settembre 2003. Gli ioni di zinco (70Zn) sono stati formati in un fascio in un acceleratore di particelle e sparati su un sottile strato di bismuto (209Bi) in una reazione di fusione fredda.
Usando questo metodo gli scienziati credevano di aver creato un singolo atomo dell’elemento 113 nel luglio 2004 e di nuovo nell’aprile 2005. In ogni occasione l’atomo subì rapidamente quattro decadimenti alfa: prima a roentgenium-274, seguito da meitnerium-270, bohrium-266 e dubnium-262.
Alfa decade :
278Nh ==> 274Rg ==> 270Mt ==> 266Bh ==> 262Db
Questi risultati non erano sufficienti per soddisfare IUPAC e IUPAP. Nel 2011 il loro gruppo di lavoro congiunto ha rifiutato di accettare la scoperta dell’elemento 113, affermando che: “Il lavoro della collaborazione di Morita et al. è molto promettente ma non ha soddisfatto i criteri per la scoperta a causa della scarsità di eventi, dell’assenza di connessioni solide con nuclidi noti e delle incongruenze notate sopra.”
Gli scienziati in Giappone hanno poi colpito un vicolo cieco. Morita ha commentato: “Per oltre sette anni abbiamo continuato a cercare dati che identificassero definitivamente l’elemento 113, ma non abbiamo mai visto un altro evento. Non ero disposto ad arrendermi, tuttavia, poiché credevo che un giorno, se avessimo perseverato, la fortuna ci sarebbe caduta di nuovo addosso.”
Per aiutare a convalidare la loro scoperta del nihonium, il team ha effettuato un nuovo esperimento che avrebbe dato loro un’idea migliore della catena di decadimento oltre 266Bh. Un fascio di ioni di sodio è entrato in collisione con un bersaglio curium creando 266Bh che poi decaduto a 262Db.
Il 12 agosto 2012 gli scienziati hanno osservato un terzo e conclusivo evento di decadimento. Nihonium è stato creato nello stesso modo di prima e ha subito gli stessi quattro decadimenti alfa come in precedenza. Inoltre, 262Db ha continuato a subire decadimenti alfa, producendo 258Lr seguito da 254Md. Poiché la catena era stata completamente caratterizzata, questo è stato preso come una chiara dimostrazione che la fonte della catena di decadimento era davvero Nihonium, elemento 113.
Nel 2015 il Gruppo di lavoro congiunto IUPAC/IUPAP (JWP) ha esaminato i lavori e ha dichiarato che: “Il team di collaborazione RIKEN in Giappone ha soddisfatto i criteri per l’elemento Z = 113 e sarà invitato a proporre un nome e un simbolo permanenti.”
Aspetto e caratteristiche
Effetti nocivi:
Il Nihonium è nocivo a causa della sua radioattività.
Caratteristiche:
Il nihonium è un metallo radioattivo sintetico.
Usi di Nihonium
Nihonium è di interesse di ricerca soltanto.
Abbondanza e isotopi
Abbondanza crosta terrestre: nulla
Abbondanza sistema solare: parti per trilione in peso, parti per trilione di moli
Costo, puro: $ per 100g
Costo, massa: bulk per 100g
Fonte: L’elemento è stato creato utilizzando una reazione di fusione fredda tra un bersaglio bismuto-209 e ioni zinco-70.
Isotopi: il Nihonium ha un isotopo la cui emivita è nota, 278Nh.

- Esperimento sulla sintesi dell’elemento 113 nella reazione, Journal of the Physical Society of Japan, Vol. 73, n. 10, ottobre 2004, pp. 2593-2596
- Osservazione della seconda catena di decadimento da 278113, Journal of the Physical Society of Japan Vol. 76, No. 4, aprile 2007
- Robert Barber, Paul Karol, Hiromichi Nakahara, Emanuele Vardaci e Erich Vogt, Scoperta degli elementi con numeri atomici maggiori o uguali a 113,. 2011, IUPAC. (scarica pdf)
Citare questa pagina
Per il collegamento online, si prega di copiare e incollare uno dei seguenti:
<a href="https://www.chemicool.com/elements/ununtrium.html">Nihonium</a>
o
<a href="https://www.chemicool.com/elements/ununtrium.html">Nihonium Element Facts</a>
Per citare questa pagina in un documento accademico, si prega di utilizzare la seguente citazione conforme MLA:
"Nihonium." Chemicool Periodic Table. Chemicool.com. 11 Jun. 2016. Web. <https://www.chemicool.com/elements/ununtrium.html>.