蛍光分光法
蛍光分光法は、温度、pH、イオン強度、溶媒、配位子の変化による共役系、芳香族分子、剛性のある平面化合物の構造変化を研究するために日常的に使用されています。 単一の蛍光体は、繰り返し励起して検出することができる何千もの検出可能な光子を生成することができ、蛍光分光法は非常に敏感な技術である。
蛍光は、分子が遷移双極子モーメントを持つ波長でエネルギーを吸収するときに発生する放射放出の一種です。 基底状態で分子に供給される励起エネルギーは光子を励起一重項状態に促進し、光子はこの励起一重項状態の最も低い振動エネルギー準位に崩壊する。 このエネルギーはさらに分子の基底状態に戻り、その過程で光子を放出します(図1に示すように)。
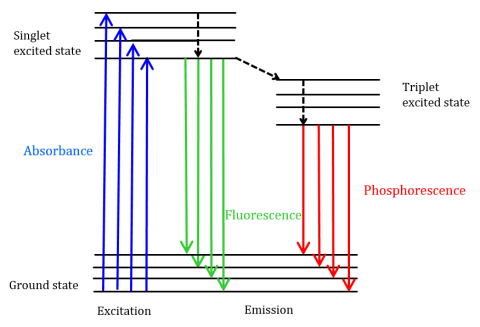
蛍光分子は、励起エネルギーが光子に変換されない非放射緩和の三つの方法、(1)内部変換、(2)外部変換、および(3)項間交差を受けることができる。 内部変換は、2つの電子状態の間に比較的小さなエネルギーギャップがあり、電子がより高い電子状態からより低いエネルギーの1つに遷移すると ここでエネルギーは電子状態の振動モードに伝達される。 振動プロセスは熱的に駆動されるため、温度の上昇は蛍光強度の低下をもたらす。 外部変換では、フルオロフォアの環境で溶質分子との衝突焼入れによってエネルギーが失われます。 一重項励起状態と三重項励起状態の振動準位がエネルギーで重なり合い,電子が最低一重項励起状態から第一励起三重項状態に遷移するときに項間交差が生じる。 基底状態に戻るときに放出される光子は、燐光として知られています(図1)。 三重項状態は一重項状態よりもエネルギーが低いので、蛍光よりも長い波長で燐光ピークが見られる。 これらの遷移も禁止されているため、燐光は蛍光(〜10–9〜10–6秒)と比較してより長い寿命(〜10-4〜102秒)を示す。 長寿命はまた、酸素消光、溶媒移動、および分子間衝突を介して熱的不活性化につながるので、燐光は通常室温では観察できず、したがってサンプルは液体窒素温度で冷却されなければならない。
ビールの法則と濃度効果
吸収は10-15秒未満のタイムスケールで起こるが、励起状態から基底状態への緩和過程ははるかに遅い。 したがって、蛍光は、吸収とは異なり、周囲の分子および溶媒との蛍光体の相互作用に関する情報を提供することができる。
蛍光強度は励起光強度に正比例します
F=2.303*K*I0*ebc
ここで、Kは機器の形状に基づく定数、I0は励起光の強度、eは蛍光体のモル吸収率、bは経路長、cは濃度です。 蛍光強度は吸収測定のように入射光強度に比されないので、蛍光感度は、入射強度と検出強度とを区別する機器の能力によって制限されないため、 その結果、より小さい集中は測定に要求される。
上記式は、サンプル吸光度が0.05AU未満の場合にのみ線形です。 サンプルが余りに集中すれば、放出ライトはより短い波長で蛍光性信号を減少させるfluorophoreによって再吸収することができます。 励起光はまた、高度に濃縮された試料の全幅を完全に透過しない可能性があり、これはまた、蛍光強度の低下をもたらす。
蛍光分光計
蛍光スペクトルの特性
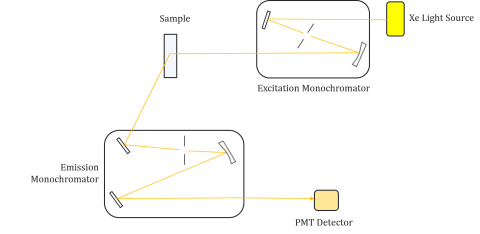
蛍光計は、励起と発光の両方のスペクトルを得ることができる励起と発光モノクロメータで構成されています。 蛍光光度計による測定は、個々の機器の励起および発光モノクロメータに固有のものです。 従って蛍光性は光源、モノクロメータの光学および光電子増倍管のような器械の設計そして部品に測定および依存の光束そして効率と直接関連して 各光源に源の寿命にわたって変わり、減る別の分光出力が(形および力両方)あります。
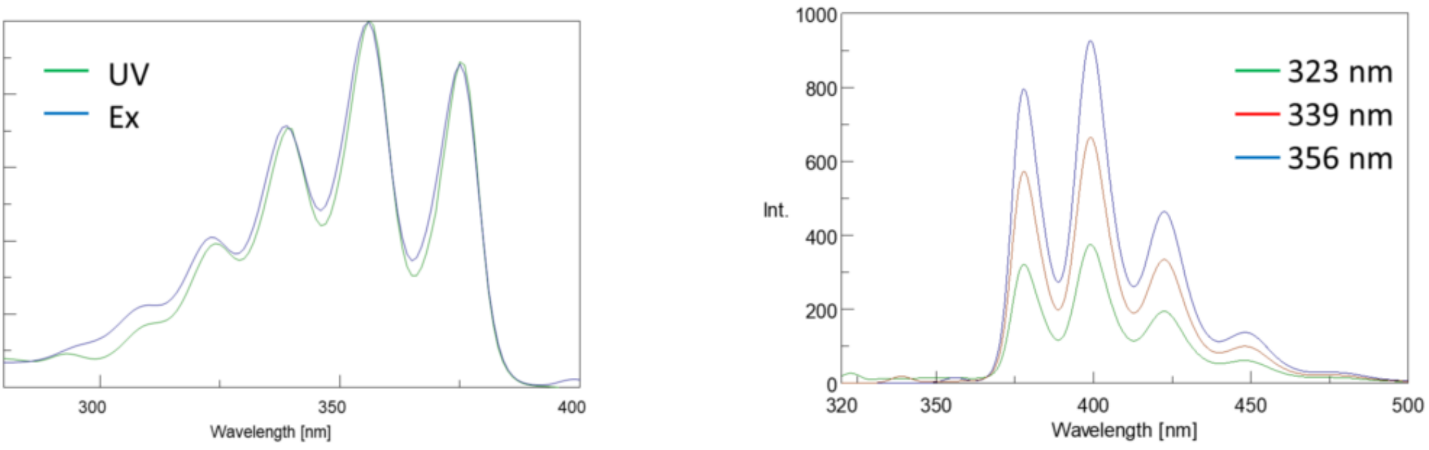
励起スペクトルは、励起波長を変化させながら、固定発光波長での強度をプロットします。 ほとんどの発光スペクトルは励起波長に依存しないので,励起スペクトルは蛍光体の吸収スペクトルの重複であることが多い。
逆に、発光スペクトルは、様々な発光波長を走査しながら、固定励起波長での強度をプロットする。 これらの発光スキャンは、フルオロフォアの分子構造とそれを取り巻く局所環境に関する情報を提供する。 蛍光発光は常に最低励起状態から基底状態に起こるので,発光スペクトルの形状は励起波長に依存しない。 分子を地面から励起状態に励起するためには、より多くのエネルギーが必要であり、その結果、対応する励起波長よりも長い波長(すなわちより小さいエネル 励起波長と発光波長の間のエネルギーのこの差は、ストークスシフトとして知られている。
また、励起状態と基底状態の振動エネルギー準位の分布が等しいため、吸収スペクトルと発光スペクトルは互いに鏡像であることが多い(図3)。 フランク=コンドンの原理は、原子核が比較的大きく、放出と吸収に関与する電子遷移がこのような速いタイムスケールで起こるため、原子核が動く時間と振動エネルギー準位がなく、したがって電子遷移を通してほぼ同じままであることを説明している。
スペクトル帯域幅
蛍光強度は入力光強度に比例するため、モノクロメータを通過する光の量は強度に大きく影響します。 励起帯域幅と放出帯域幅の合計は、すべてのピークが十分に分解されるように、監視対象のピークのスペクトル帯域幅(SBW)程度である必要があります。 この経験則に従う限り、帯域幅を開放して、蛍光性の低いサンプルの光スループットの量を増加させることができます。 SBWは、フルオロフォアのStokesシフトによっても影響を受けることができる。 ストークスシフトが狭いほど、使用できる許容可能なSbwの範囲が制限される可能性があります。
蛍光アーティファクト
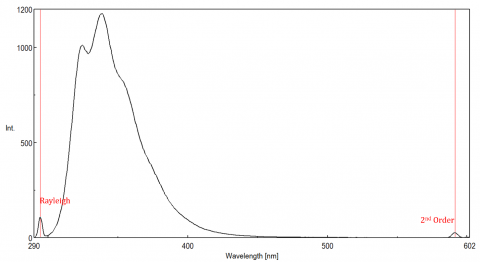
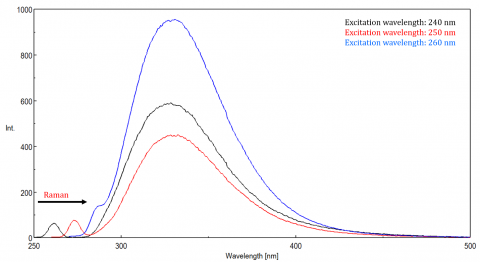
散乱光はアーティファクトを生じさせ、蛍光スペクトルを歪ませる可能性があります。 蛍光に見られる最も一般的な散乱の3つのタイプは、レイリー散乱、2次散乱、およびラマン散乱です(図3)。 レイリー散乱は散乱された励起光であり、したがって励起波長でピークを迎える。 2次散乱は励起波長の2倍で観測される高次散乱である。 ラマン散乱は、励起波長からの一定のエネルギーでの溶媒とピークによる非弾性散乱である。 蛍光ピークからラマン散乱を区別するために、励起波長は5〜10nmの増分で変化させることができ、問題のピークが励起波長とともにシフトし、強度が減少 また、ピークが空白の溶媒スペクトルにあるかどうかを確認することもできます。 もしそうであれば、それはラマンピークである可能性があります。 蛍光ピークが、Raman散乱またはRayleigh散乱のいずれかと近すぎるか、または重複する場合、帯域幅および/または励起波長を調整して、散乱を蛍光ピークからシフトさ これらの効果は非常に低いfluorophoreの集中および特に非常に分散の解決のために、蛋白質、microsphere、nanoparticles、また固体のような最も顕著です。
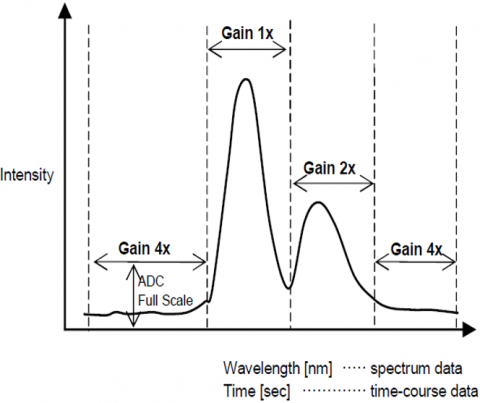
ダイナミックレンジ
自動ゲイン制御機能は、蛍光強度に基づいて検出器からの信号のゲインを自動的に調整します。 これはs/Nを改善し、結果の正確さを保証するために異なった強度のピークが自動的に調節されるように分光または時間のコースの測定のための全
自動感度制御システム(SCS)
自動感度制御システム(SCS)は、蛍光強度に応じて検出器電圧を自動的に調整することにより、検出された蛍光信号のダイナ これはmicromolar集中にsub-picomolarの固定波長か定量分析の測定を手動で器械を変えないで可能にする。

図5. 自動SCS機能を使用して5·10-13からの1.5·10-6Mへのフルオレセインの解決の検量線。
蛍光分光法の応用
異方性
蛍光異方性は、蛍光体が偏光軸に応じて異なる強度の光を放出するときに観察され、次の式で記述されます
r=Ivv-GIvh/Ivv+2givh
ここで、励起面に平行な発光強度であり、励起面に垂直な発光強度である。励起面。 GはG因子または計器格子因子と呼ばれ、発光モノクロメータの偏光依存性を説明します。
すべての蛍光体は、分子軸に沿って特定の方向に沿って起こる遷移モーメントを持っています。 偏光に曝されると,入射光の角度の周りに配向した吸収遷移モーメントを有するランダムに配向した蛍光体が励起され,この励起状態集団は部分的に配向する。 分子が励起状態から基底状態に戻ると、電子電荷が再分配され、双極子モーメントの配向の変化が励起分極と放出分極に影響を与える。 例えば、分子が回転する前に蛍光が放出されると、蛍光光は励起光の偏光の方向に向かって強く偏光される。 分子を完全にランダムな方向に回転させた後に光が放出されると、蛍光はもはや偏光されなくなる。
蛍光異方性を測定する場合、(1)分子サイズ、(2)分子の環境の粘度、(3)結合した分子の強度と自由度など、分子の動きに影響を与えます。 異方性の測定は光子の吸収と放出の間に起こるfluorophoreの平均角変位を定めます。 角変位は励起状態の寿命の間の回転拡散の速度と程度に依存する。 フルオロフォアが無制限で、光子を再放出する前に自由に回転することができる場合、拡散速度は一般に放出速度よりも速く、異方性はほぼゼロに等しい。 回転拡散は放出を脱分極する遷移モーメントの方向を変化させる。 フルオロフォアが制限されるほど、柔軟性の減少が全体の回転速度を減少させるので、異方性値が大きくなります。<6027><4726>FRET<1893><8283>蛍光共鳴エネルギー移動(FRET)は、隣接する2つの分子間のエネルギー移動を支配する機構である。 ドナーは、最初にその励起状態にあり、非放射電子共鳴を介してアクセプター分子にエネルギーを伝達することができる。
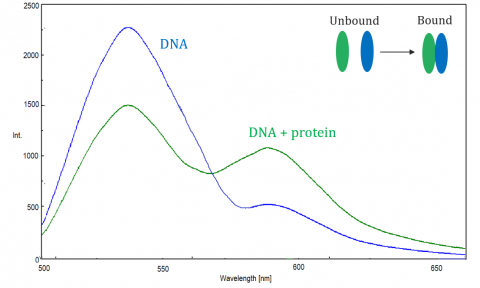
FRETは、アクセプターまたは励起ドナーの蛍光/消光を測定する分光蛍光計によって監視されます。 フレット効率は、以下の要因に依存します: ドナーとアクセプタの間の距離、ドナーとアクセプタの間のスペクトル重複、およびそれらの双極子モーメントのアライメント。 効率はドナーとアクセプタの間の距離の第六乗に反比例し、この技術は距離の小さな変化に非常に敏感である。 ドナー蛍光スペクトルとアクセプター吸収スペクトルの重複領域が大きいと,FRET効率が高くなる。 FRET効率は,二つの双極子モーメントが互いに平行または反平行であるときにも最大であり,双極子モーメントが互いに垂直であるときにはエネルギー移動は起こらない。 典型的には、ドナーとアクセプターとの間の距離が1nmと10nmの間である場合、フレットが生じる。
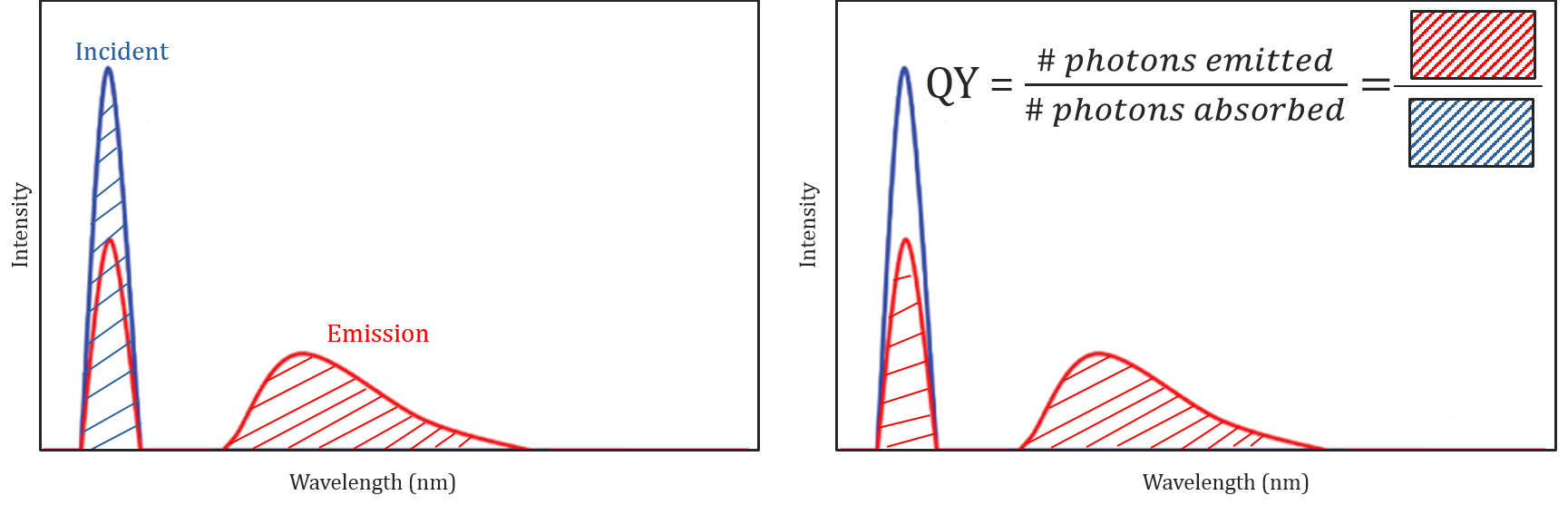
量子収率とスペクトル補正
異なる分子および環境条件は、分子が蛍光を発するかどうかに影響を与えるだけでなく、放出された蛍光放射の強 蛍光を発する分子の効率は、その量子収率によって記述され、サンプルによって放出される光子の数に吸収された光子の数の比として定義される。
場合によっては、正確なスペクトル測定を決定する必要があります。 これは、既知の較正された材料への参照を使用して行われます。 使用される目盛りを付けられた源は知られていた器械の絶対分光出力があるように点検され、顧客に供給される個々の器械を訂正するために参照ス スペクトル補正が効果的に機能するためには、5nmのスペクトル帯域幅でのスペクトル補正を10nmのSBWを使用した測定に適用できないように、各 これは、偏光子が使用されている場合の位置、および高次フィルタの使用に適用されます。 お客様が使用するスペクトル帯域幅の組み合わせごとに、高次フィルタの選択の包含または除外、および偏光子の位置が取り付けられている場合には、分光補正を行う必要があります。 サンプル励起波長と発光波長は、校正に使用される溶液/光源を決定します。
近赤外線
スペクトルの近赤外線領域をプローブするアプリケーションでは、PMT検出器のスペクトル応答がデータを取得するために重要です。 可視領域の赤色端では、近赤外線では、PMTの量子効率が大幅に低下し、サンプル測定中に信号強度がほとんどまたはまったく得られません。 FRET実験およびNIR染料およびプローブは、5 0 0nm以上の波長で頻繁に監視され、多くの場合、蛍光のようなそのような敏感な技術であっても、小さな信号を有 図8は、標準PMTを使用したローダミンBの蛍光強度の違いを、スペクトルの赤色端の波長により敏感なPMTと比較して示しています。
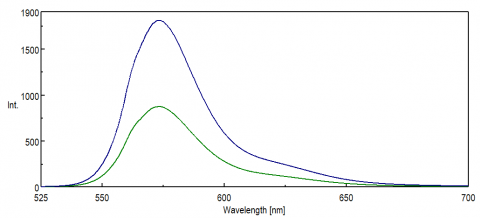
:
円二色性分光法
円二色性分光法(CD)は、分子の光学活性を介してキラリティを分析するために使用される不可欠な分析技術です。 CDは、分子構造の多種多様に適用することができますが、高分子構造、特にタンパク質や核酸の解明のための科学界で好意を発見しました。