Fluorescentiespectroscopie
Fluorescentiespectroscopie wordt routinematig gebruikt voor het bestuderen van structurele veranderingen in geconjugeerde systemen, aromatische moleculen en stijve, vlakke verbindingen als gevolg van veranderingen in temperatuur, pH, Ionische sterkte, oplosmiddel en liganden. Een enige fluorophore kan duizenden detecteerbare fotonen produceren die herhaaldelijk kunnen worden opgewekt en gedetecteerd, makend fluorescentiespectroscopie is een hoogst gevoelige techniek.
fluorescentie is een soort stralingsemissie die optreedt wanneer een molecuul energie absorbeert op een golflengte waar het een overgangs-dipoolmoment heeft. De opwindingsenergie die aan de molecule bij de grondstaat wordt verstrekt bevordert fotonen aan een opgewekte singletstaat, waar zij dan tot het laagste trillingsenergieniveau van deze opgewekte singletstaat vervallen. Deze energie ontspant zich verder terug naar de grondtoestand van het molecuul, waardoor fotonen vrijkomen, zoals weergegeven in Figuur 1.
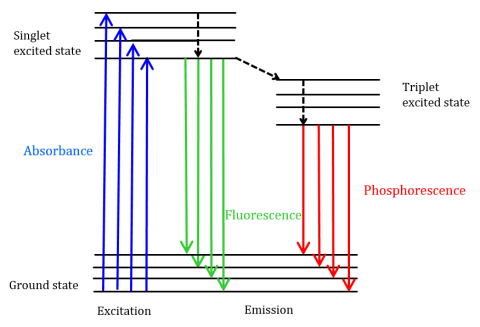
Fluorescerende moleculen kunnen ook worden onderworpen aan drie methoden van niet-radiatieve relaxatie waarbij de excitatie-energie niet wordt omgezet in fotonen: (1) Interne conversie, (2) externe conversie, en (3) intersystem crossing. De interne omzetting komt voor wanneer er een relatief kleine energiekloof tussen twee elektronische Staten en de elektronenovergang van een hogere elektronische staat aan één van lagere energie is. Hier wordt de energie overgebracht naar de trillingsmodi van de elektronische staat. Aangezien trillingsprocessen thermisch worden aangedreven, leidt de stijgende temperatuur tot dalingen van fluorescentieintensiteit. In externe omzetting, wordt de energie verloren door collisional het doven met opgeloste molecules in het milieu van fluorophore. Intersystem crossing ontstaat wanneer trillingsniveaus van de singlet en triplet opgewekte toestanden elkaar overlappen in energie en elektronen overgang van de laagste singlet opgewekte toestand naar de eerste opgewekte triplet toestand. De fotonen die vrijkomen als ze terugkeren naar de grond staat bekend als fosforescentie (figuur 1). De tripletstaat is lager in energie dan de singletstaat zodat worden de fosforescentiepieken gevonden bij langere golflengten dan fluorescentie. Aangezien deze overgangen ook verboden zijn, vertoont fosforescentie een langere levensduur (~10-4 – 102 seconden) vergeleken met fluorescentie (~10-9 – 10-6 seconden). De langere levensduur ook leiden tot thermische deactivering via zuurstof doven, oplosmiddel beweging, en intermoleculaire botsing zodat fosforescentie typisch niet kan worden waargenomen bij kamertemperatuur en monsters moeten daarom worden gekoeld bij vloeibare stikstof temperatuur.
wet-en concentratie-effecten van bier
terwijl absorptie plaatsvindt op een tijdschaal van minder dan 10-15 seconden, is het relaxatieproces van de opgewekte toestand naar de grond veel langzamer. Daarom kan de fluorescentie informatie over de interactie van fluorophores met omringende molecules en oplosmiddelen verstrekken, in tegenstelling tot absorptie.
Fluorescentieintensiteit is recht evenredig met de intensiteit van het opwindingslicht
F = 2,303 * K * I0 * ebc
waar K een constante is gebaseerd op de geometrie van het instrument, I0 is de intensiteit van het opwindingslicht, e is de molaire absorptievermogen van de fluorofoor, b is de pathlengte en c is de concentratie. Aangezien de fluorescentieintensiteit niet aan de incidentele lichte intensiteit zoals met absorptiemetingen wordt ratioed, is de fluorescentiegevoeligheid veel groter omdat het niet door de instrumentencapaciteit wordt beperkt om tussen het incident en gedetecteerde intensiteiten te onderscheiden. Daarom zijn kleinere concentraties nodig voor metingen.
bovenstaande vergelijking is alleen lineair wanneer de monsterabsorptie kleiner is dan 0,05 ae. Als een steekproef te geconcentreerd is, kan het emissielicht door fluorophore opnieuw worden geabsorbeerd, die het fluorescentiesignaal bij kortere golflengten verzwakken. Het opwindingslicht kan ook niet volledig de volledige breedte van een hoogst geconcentreerde steekproef doordringen, wat ook tot verminderde fluorescentieintensiteiten zal leiden.
instrumentatie van Fluorescentiespectroscopie
karakteristieken van een Fluorescentiespectrum
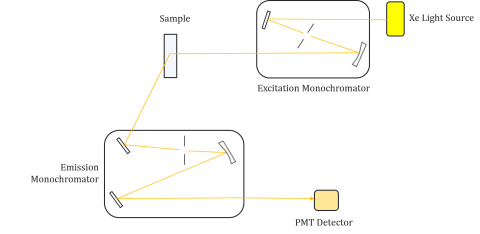
Fluorometers zijn samengesteld uit een excitatie-en emissiemonochromator, waardoor gebruikers zowel excitatie-als emissiespectra kunnen verkrijgen. Een meting met een fluorometer is uniek voor de excitatie-en emissiemonochromatoren van het individuele instrument. Fluorescentie is direct gerelateerd aan de lichtstroom en de efficiëntie van de meting en daarom afhankelijk van het instrumentontwerp en componenten zoals de lichtbron, monochromator optica en fotomultiplicatorbuis. Elke lichtbron zal een andere spectrale output hebben (zowel vorm als vermogen) die zal variëren en afnemen gedurende de levensduur van de bron.
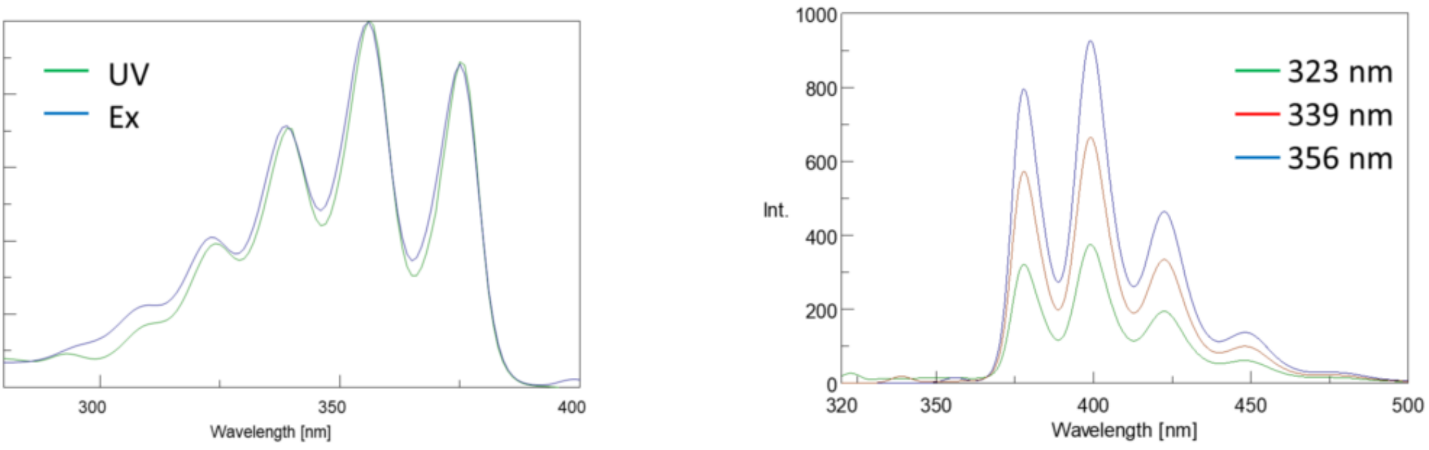
Excitatiespectra plotten de intensiteit bij een vaste emissiegolflengte, waarbij de excitatiegolflengten worden gevarieerd. Aangezien de meeste emissiespectra onafhankelijk van de opwindingsgolflengte zijn, zijn de opwindingsspectra vaak duplicaten van het absorptiespectrum van fluorophore.
omgekeerd zet een emissiespectrum de intensiteit uit bij een vaste excitatiegolflengte terwijl het door wisselende emissiegolflengten scant. Deze emissieaftasten verstrekken informatie over de moleculaire structuur van fluorophore en het lokale milieu die het omringen. Aangezien de fluorescentieemissie altijd van de laagste opgewekte staat aan de grondstaat voorkomt, is de vorm van het emissiespectrum onafhankelijk van de opwindingsgolflengte. Meer energie wordt ook vereist om een molecuul van de grond aan de opgewekte staat op te wekken, resulterend in emissiepieken bij langere golflengten (dwz kleinere energieën) dan hun overeenkomstige opwindingsgolflengten. Dit verschil in energie tussen de opwinding en de emissiegolflengten staat bekend als de Stokes-verschuiving.
bovendien zijn absorptie-en emissiespectra vaak spiegelbeelden van elkaar vanwege de gelijke verdeling tussen de trillingsenergieniveaus van de aangeslagen en de grondtoestanden (Figuur 3). Het Franck-Condon Principe legt uit dat omdat de kernen relatief groot zijn en de elektronische overgang die betrokken is bij emissie en absorptie plaatsvindt op zulke snelle tijdschalen, er geen tijd is voor kernen om te bewegen en de trillingsenergie niveaus en daarom ongeveer hetzelfde blijven gedurende de elektronische overgang.
spectrale bandbreedte
aangezien de fluorescentieintensiteit evenredig is met de lichtintensiteit van de input, zal de hoeveelheid licht die door de monochromator wordt gevoerd, de intensiteit sterk beïnvloeden. De som van de excitatie-en emissiebandbreedtes moet ongeveer gelijk zijn aan de spectrale bandbreedte (SBW) van de piek die wordt gemonitord, zodat alle pieken goed worden opgelost. Zolang deze vuistregel wordt gevolgd, kunnen de bandbreedtes worden geopend om de hoeveelheid lichtdoorvoer voor steekproeven met lage fluorescentie te verhogen. SBW kan ook door de Stokesverschuiving van fluorophore worden beà nvloed. Smallere Stokes shifts kunnen het bereik van aanvaardbare SBWs dat kan worden gebruikt beperken.
fluorescentie artefacten
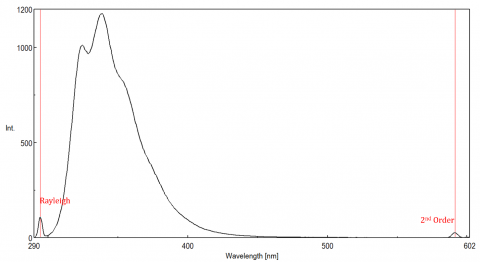
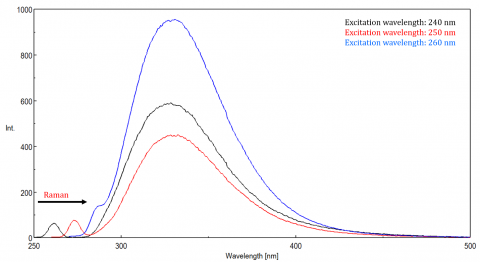
verstrooid licht kan artefacten veroorzaken, waardoor het fluorescentiespectrum wordt verstoord. De drie meest voorkomende vormen van verstrooiing gezien in fluorescentie zijn Rayleigh, 2nd order, en Raman scatter (Figuur 3). Rayleigh het verspreiden is het verspreide opwindingslicht en daarom pieken bij de opwindingsgolflengte. 2nd order scatter is hogere-orde scatter waargenomen bij twee keer de excitatie golflengte. Het verspreiden van Raman is inelastic verspreiding toe te schrijven aan oplosmiddelen en pieken bij een vaste energie van de opwindingsgolflengte. Om Raman te onderscheiden die zich van een fluorescentiepiek verspreiden, kan de opwindingsgolflengte in 5 tot 10 nm-verhogingen worden gevarieerd en als de piek in kwestie met de opwindingsgolflengte en dalingen in intensiteit verschuift, dan is die piek, toe te schrijven aan ramanverspreiding. U kunt ook controleren of de piek zich in het spectrum van het lege oplosmiddel bevindt. Als dat zo is, is er een kans dat het een Raman peak is. Als de fluorescentiepiek te dicht of overlappend met of de Raman of Rayleighverspreiding is, kunnen de bandbreedtes en/of opwindingsgolflengte worden aangepast om de verspreiding van de fluorescentiepiek te verschuiven. Deze gevolgen zijn het meest prominent voor zeer lage fluorophore concentraties en vooral hoogst het verspreiden van oplossingen, zoals proteã nen, microsphere, nanoparticles, evenals vaste stoffen.
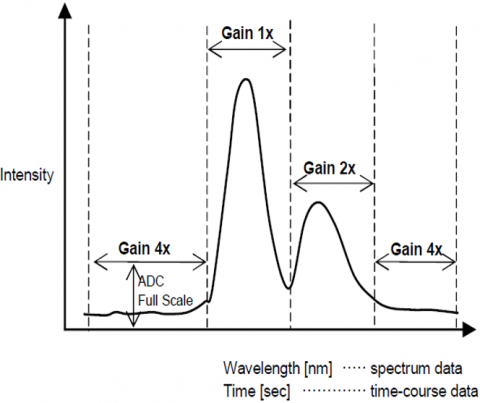
dynamisch bereik
de automatische versterkingsregeling past automatisch de versterkingssterkte van een signaal van de detector aan op basis van de fluorescentieintensiteit. Dit optimaliseert het signaal naar ruis over het gehele gescande bereik voor spectrale of tijdsverloop metingen, zodat pieken met verschillende intensiteiten automatisch worden aangepast om de S/N te verbeteren en de nauwkeurigheid van het resultaat te verzekeren.
Automatic Sensitivity Control System (SCS)
het Automatic Sensitivity Control System(SCS) breidt het dynamische bereik van het gedetecteerde fluorescentiesignaal uit door de spanning van de detector automatisch aan te passen aan de fluorescentie-intensiteit. Dit maakt metingen van subpicomolaire tot micromolaire concentraties mogelijk zonder het instrument handmatig te veranderen.

Figuur 5. Kalibratiecurve van fluoresceïneoplossingen van 5 * 10-13 tot 1,5 * 10-6 M met behulp van de auto-SCS-functie.
toepassingen van Fluorescentiespectroscopie
anisotropie
fluorescentie anisotropie wordt waargenomen wanneer een fluorofoor licht van verschillende intensiteiten uitzendt, afhankelijk van de polarisatieassen en wordt beschreven met de volgende vergelijking
r=Ivv-GIvh/Ivv+2GIvh
waarbij de emissieintensiteit evenwijdig is aan het excitatievlak en de emissieintensiteit loodrecht is naar het excitatie vliegtuig. G wordt de G-factor of instrument rooster factor genoemd en is verantwoordelijk voor de polarisatie afhankelijkheid van de emissie monochromator.
alle fluoroforen hebben overgangsmomenten die langs specifieke richtingen langs de moleculaire as voorkomen. Wanneer blootgesteld aan gepolariseerd licht, willekeurig georiënteerde fluorophores die hun absorptieovergangsmomenten hebben die rond de hoek van het invallende licht worden georiënteerd zullen worden opgewekt en deze opgewekte staatspopulatie is gedeeltelijk georiënteerd. Aangezien een molecuul van een opgewekte staat terug aan zijn grondstaat terugkeert, wordt de elektronenlading herverdeeld en de verandering in de oriëntatie van de dipoolmomenten effect de opwinding en emissiepolarisaties. Bijvoorbeeld, wanneer de fluorescentie wordt uitgezonden alvorens een molecule roteert, zal het fluorescentielicht sterk naar de richting van de polarisatie van het opwindingslicht worden gepolariseerd. Als het licht na de omwenteling van de molecule in een volledig willekeurige richting wordt uitgezonden, zal de fluorescentie niet meer gepolariseerd zijn.
bij het meten van fluorescentieanisotropie zullen de volgende factoren de moleculaire beweging beïnvloeden: (1) moleculaire grootte, (2) viscositeit van de omgeving van het molecuul, en (3) sterkte en vrijheidsgraden van een gebonden molecuul. De anisotropiemetingen bepalen de gemiddelde hoekverplaatsing van fluorophore die tussen de absorptie en de emissie van een foton voorkomt. De hoekverplaatsing is afhankelijk van de snelheid en omvang van de rotatiediffusie tijdens de levensduur van de opgewekte toestand. Wanneer fluorophore onbeperkt is en toegestaan om vrij te roteren alvorens een foton opnieuw uit te zenden, is het tarief van verspreiding over het algemeen sneller dan het tarief van de emissie en anisotropy is ruwweg gelijk aan nul. Rotatieverspreiding verandert de richting van het overgangsmoment waardoor de emissie wordt gedepolariseerd. Beperkter fluorophore, groter zal de anisotropiewaarde aangezien de daling van flexibiliteit het algemene tarief van omwenteling zal verminderen zijn.
FRET
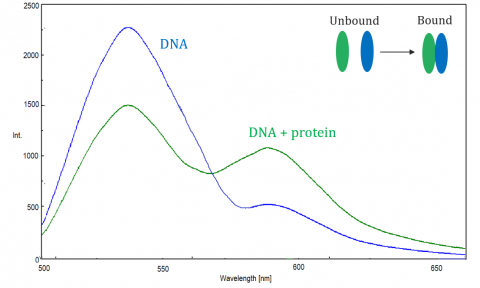
fluorescentie resonantie-energieoverdracht (fret) is een mechanisme dat de energieoverdracht tussen twee naburige moleculen regelt. Een donor, aanvankelijk in zijn opgewekte staat, kan energie aan een acceptormolecule door niet-radiatieve elektronresonantie overbrengen.
FRET wordt gecontroleerd door de spectrofluorometer, die de fluorescentie/demping van de acceptor of de aangeslagen donor meet. FRET efficiëntie hangt af van de volgende factoren: de afstand tussen donor en acceptor, de spectrale overlap tussen donor en acceptor, en de uitlijning van hun dipoolmomenten. De efficiëntie is omgekeerd evenredig met de zesde macht van de afstand tussen donor en acceptor, waardoor de techniek extreem gevoelig is voor kleine veranderingen in afstand. Wanneer het overlapgebied van het spectrum van de donorfluorescentie en het spectrum van de acceptorabsorptie groter is, is de efficiency van het lijstwerk hoger. De efficiëntie van het FRET is ook op een maximum wanneer de twee dipoolmomenten parallel of anti-parallel aan elkaar zijn, en geen energieoverdracht optreedt wanneer de dipoolmomenten loodrecht op elkaar staan. Typisch wanneer de afstand tussen donor en acceptor tussen 1 en 10 nm is, komt het lijstwerk voor.
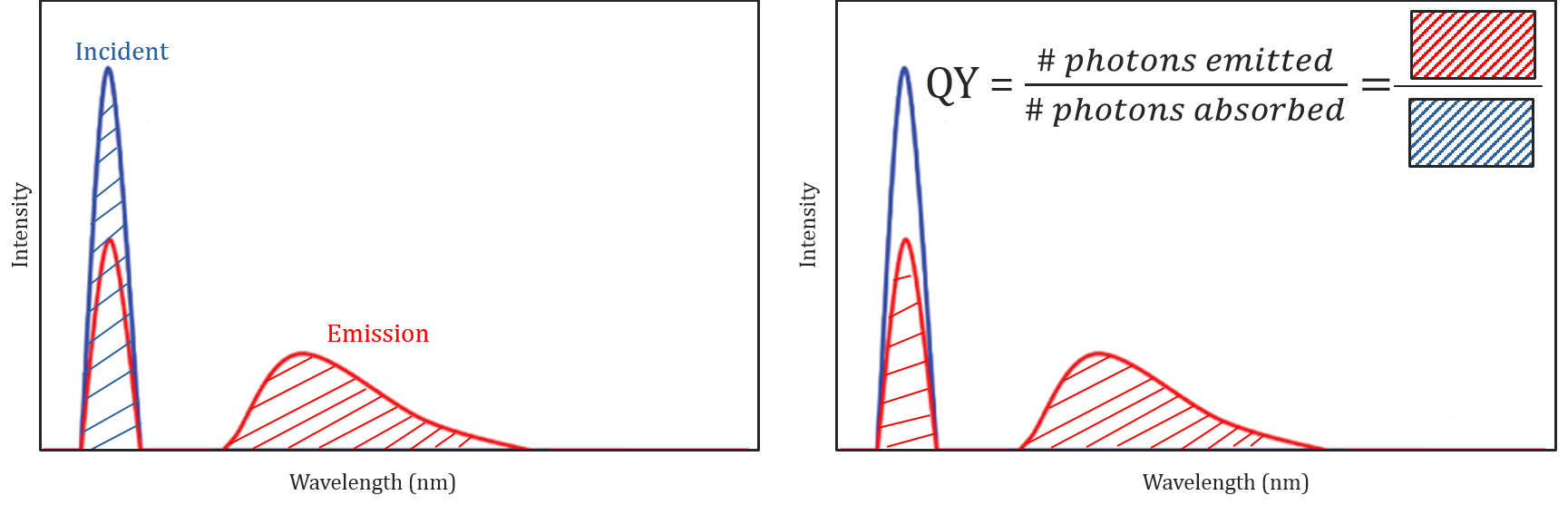
Kwantumopbrengst en spectrale correctie
verschillende moleculaire en omgevingsomstandigheden beïnvloeden niet alleen of een molecuul fluoresceert of niet, maar kunnen ook de intensiteit of kwantumopbrengst van de uitgezonden fluorescentiestraling bepalen. De efficiëntie van een molecule om te fluoresceren wordt beschreven door zijn kwantumopbrengst en wordt gedefinieerd als de verhouding van het aantal fotonen geabsorbeerd aan het aantal fotonen uitgezonden door de steekproef.
in sommige gevallen is het noodzakelijk nauwkeurige spectrale metingen te bepalen. Dit wordt gemaakt met behulp van verwijzingen naar bekende gekalibreerde materialen. De gekalibreerde bronnen die worden gebruikt, worden gecontroleerd op absolute spectrale output op een bekend instrument en er wordt een referentiespectrum geleverd om het individuele instrument dat aan de klant wordt geleverd te corrigeren. Om de spectrale correctie effectief te laten werken, moet deze worden uitgevoerd bij elke parameter en bandbreedtecombinatie van het instrument, zodat de spectrale correctie bij een spectrale bandbreedte van 5 nm niet kan worden toegepast op metingen met een SBW van 10 nm. Dit geldt voor de positie van polarisatoren als ze worden gebruikt, evenals het gebruik van hogere orde filters. Het is noodzakelijk om de spectrale correctie uit te voeren voor elke combinatie van spectrale bandbreedtes die door de klant moet worden gebruikt, voor het al dan niet opnemen van de hogere volgorde filterselectie en voor de posities van polarisatoren indien gemonteerd. De monster excitatie en emissie golflengten zullen bepalen welke oplossing / lichtbron wordt gebruikt voor kalibratie.
nabij-infrarood
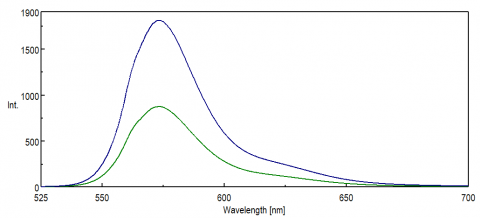
voor toepassingen die het NIR-gebied van het spectrum onderzoeken, is de spectrale respons van de PMT-detector van cruciaal belang voor het verkrijgen van gegevens. In het rode uiteinde van het zichtbare gebied, in het NIR, neemt de kwantumefficiëntie van de PMT aanzienlijk af, wat resulteert in weinig tot geen signaalintensiteit tijdens monstermetingen. FRET experimenten en Nir kleurstoffen en sondes worden vaak gecontroleerd bij golflengten boven 500 nm en in veel gevallen hebben kleine signalen, zelfs voor een dergelijke gevoelige techniek zoals fluorescentie. Figuur 8 illustreert het verschil in fluorescentie intensiteit van rhodamine B met behulp van een standaard PMT vergeleken met een PMT die gevoeliger is voor golflengten op het Rode einde van het spectrum.
Complementaire Techniek:
circulaire dichroism spectroscopie
circulaire dichroism spectroscopie (CD) is een essentiële analytische techniek die wordt gebruikt om chiraliteit in moleculen te analyseren door middel van hun optische activiteit. CD kan op een grote verscheidenheid van moleculaire structuren worden toegepast maar heeft gunst in de wetenschappelijke gemeenschap voor de opheldering van macromoleculaire structuur, vooral proteã NEN EN nucleic zuren gevonden.