Brom trifluoride je toxický interhalogen sloučeniny. Je známý pro své použití jako silné fluorační činidlo.
Brom trifluoride Identifikace
Číslo CAS: 7787-71-5
Číslo UN: UN1746
PubChem Compound ID: 24594
ChemSpider Referenční Číslo: 20474213
MDL číslo: MFCD00042533
Číslo ES: 232-132-1
Číslo RTECS: ED2275000
Identifikátor InChI: InChI=1S/BrF3/c2-1(3)4
InChI Klíč: InChIKey=FQFKTKUFHWNTBN-UHFFFAOYSA-N
Chemický Vzorec pro Brom trifluoride
chemický vzorec pro tento interhalogen sloučenina je BrF3.
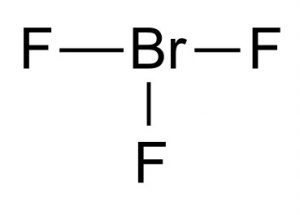
Obrázek 1 – Brom trifluoride
Výroba Bromu trifluoride
V roce 1906, Paul Lebeau syntetizovány tuto sloučeninu poprvé tím, že reakce bromu s fluorem při teplotě 20°C. reakce je reprezentována následující rovnicí:
Br2 + 3F2 → 2BrF3
Další způsob, jak produkovat Brom trifluoride je současně redukovat a oxidovat Brom monofluoride. Tato reakce produkuje fluorid bromu a brom.
3BrF → BrF3 + Br2
Brom trifluoride Složení
Brom trifluoride se skládá z 58.367% bromu a 41.632% fluoru.
Vlastnosti Bromu trifluoride
fyzikální a chemické vlastnosti této látky jsou popsány níže:
Vzhled
To je slámově zbarvenou tekutinu.
zápach
chemická látka má štiplavý zápach.
hygroskopie
je to hygroskopická kapalina.
molární hmotnost
molární hmotnost fluoridu bromu je 136,90 g / mol.
Monoisotopická Hmotnost
monoisotopická hmotnost této látky je 135.913547 u (unifikované atomové hmotnostní jednotky).
Hustota
hustota látky je 2.803 g/cm3.
Bod Tání
bod tání Brom trifluoride je 8.77°C.
Bod Varu
bod varu této látky je 125.72°C.
vodivost
díky autoionizaci je kapalina dobrým vodičem elektřiny.
Žíravost
je to žíravá kapalina.
hustotě
specifická hmotnost Bromu trifluoride je 2.81 při teplotě 68.0°F.
Dipólový moment
molekulární dipólový moment této látky je 1.19 Debye.
rozpustnost
fluorid brom je rozpustný v kyselině sírové. Rozkládá se a exploduje, když přichází do styku s organickými sloučeninami a vodou. Reakce se sloučeninami obsahujícími vodík mohou způsobit násilné reakce. Mnoho iontových fluoridů se snadno rozpouští v fluoridu bromu a tvoří solvobázy.
KF + BrF3 → KBrF4
Kromě výše uvedených vlastností, Brom trifluoride je také silný fluoraci z agenta.
struktura fluoridu bromu
Lewisova struktura fluoridu bromu ukazuje, že má molekulární strukturu ve tvaru T. Podle VSEPR teorie molekulární tvorby je centrální brom spojen se dvěma elektronovými páry. Vzdálenost mezi brom centrum a rovníkové fluoru je 1.72 Å a pro každý axiální fluoru je 1.81 Å. Úhel mezi rovníkovým fluorem a axiálním fluorem je 86,2°. Úhel je udržován o něco méně než 90°, protože síla odpuzování z vazeb Br-F je nižší než síla elektronových párů.
reakce fluoridu bromu
fluorid bromu při reakci s oxidy kovů uvolňuje kyslík. Když fluorid bromu reaguje s oxidem křemičitým, produkuje plynný tetrafluorid křemíku a brom.
při reakci mezi fluoridem bromem a oxidem titaničitým(IV) se vyrábí fluorid titaničitý(IV) a brom.
fluorid bromu používá
fluorid bromu je silné ionizující anorganické rozpouštědlo a fluorační činidlo. Používá se také pro výrobu hexafluoridu uranu (UF6) při zpracování a přepracování jaderného paliva.
Brom trifluoride MSDS
Zdravotní Rizika
lidská bytost vystavena Brom trifluoride může trpět z následujících zdravotních problémů:
Pokožkou: Kontakt s touto chemikálií může vést k pálení a dráždivým pocitům.
oční kontakt: pokud se oči dostanou do kontaktu s chemickými výpary nebo samotnou chemickou látkou, může to vést k silnému pálení očí, vředům a dokonce i slepotě.
požití: požití vede k silnému spálení sliznic.
inhalace: inhalace může vést k silnému podráždění horních cest dýchacích.
První Pomoc
Oči: oči Je třeba důkladně omýt velkým množstvím vody po dobu nejméně 15 minut. Lékař musí být okamžitě konzultován.
kůže: pokud se kůže dostane do kontaktu s chemickou látkou, infikované oblasti by měly být dobře omyty vodou a mýdlem po dobu nejméně 15 minut. Je nutná okamžitá lékařská péče. Kontaminovaný oděv je třeba rychle odstranit. Oblečení by mělo být před opětovným použitím důkladně vyčištěno a vysušeno. Kontaminované boty by měly být zničeny.
požití: v případě náhodného požití by oběť měla vypít velké množství vody. Vyvolání zvracení se nedoporučuje.
inhalace: V případě jakýchkoli nežádoucích účinků by měla být oběť odvezena do nekontaminované oblasti. Umělé dýchání musí být aplikováno v případě, že oběť nedýchá. Pokud je dýchání a dýchání stále obtížné, měl by být podán kyslík. K zajištění bezpečnosti oběti je nutná další lékařská pomoc.
Reaktivita Profil
Brom trifluoride je vysoce reaktivní oxidační činidlo. Reaguje prudce, když přichází do styku s vodou. Může urychlit spalování hořlavé látky. Při kontaktu s látkami obsahujícími vodík, jako je kyselina octová, amoniak a metan, může způsobit výbuch a požár. Také prudce reaguje s kyselinami, halogeny, halogenidy kovů, kovy a oxidy kovů při pokojové teplotě. Konkrétně způsobuje nebezpečné reakce s kyselinou dusičnou, kyselinou sírovou, jodem a selenem.
Protipožární Opatření
Brom trifluoride je oxidační činidlo, a tak se může vznítit nebo explodovat, když přijde do kontaktu s hořlavými materiály.
v případě velkých požárů by měla být oblast izolována a zaplavena vodou z bezpečné vzdálenosti. Pokud jsou nádoby skladující fluorid Bromitý blízko ohně, měly by být odstraněny, pokud by to mohlo být provedeno bezpečně. Nádoby by měly být chlazeny tekoucí vodou i dlouho po uhašení požáru.
hasicí prostředky: při hašení požáru je třeba používat vhodné hasicí prostředky. Pro hašení požáru se doporučuje použití vody, suchého chemického nebo sodného popela.
opatření k náhodnému uvolnění
hořlavé materiály by měly být izolovány a mělo by se zabránit jakémukoli spojení s nimi. Rozlitý materiál by se neměl dotýkat. Únik chemikálií by měl být zastaven, pokud je to možné bez osobního rizika. Prevalence chemických par by měla být snížena postřikem vodou. Je třeba dbát na to, aby se voda nedostala do chemických nádob. U velkých úniků by chemikálie měly být umístěny do karantény pro pozdější likvidaci. Oblast by měla být řádně větrána.
manipulace s fluoridem bromem
manipulace s tímto materiálem podléhá manipulačním předpisům podle US OSHA 29 CFR 1910.119.
Skladování Brom trifluoride
chemické látky by měly být skladovány a zpracovány podle aktuální normy a předpisy NFPA 430 Kód pro skladování Kapalných a Pevných Oxidační Materiály. Chemické nádoby by měly být chráněny před jakýmkoli fyzickým poškozením. Měly by být také chráněny před neslučitelnými látkami.
Osobní Ochrana
Při zpracování této chemické látky, odpovídající ochrana musí být přijata. Mělo by být použito správné ochranné zařízení. Ty by měly v ideálním případě obsahovat:
- MSHA/NIOSH (schválen nebo ekvivalent) dýchací přístroj s tlakem-poptávky kyslíkové masky je nutné pro správné dýchání.
- k ochraně očí jsou vyžadovány ochranné brýle nebo ochranné brýle schválené OSHA.
- k ochraně pokožky před škodlivými infekcemi způsobenými chemickým kontaktem je třeba používat ochranný oděv a rukavice.
kromě výše uvedeného ochranného zařízení by měla být oblast také dobře větrána. Ventilační mechanismus by měl být odolný vůči výbuchům v případě, že jsou přítomny výbušné koncentrace chemické látky. Měl by být také zajištěn místní výfukový systém.