El trifluoruro de bromo es un compuesto interhalógeno tóxico. Es conocido por sus usos como un agente fluorante fuerte.
Identificación del trifluoruro de bromo
Número CAS: 7787-71-5
Número ONU: UN1746
Identificación del compuesto PubChem: 24594
Número de referencia de ChemSpider: 20474213
Número MDL: MFCD00042533
Número EC: 232-132-1
Número RTECS: ED2275000
InChI Identificador: InChI = 1S / BrF3 / c2-1(3)4
Clave InChI: InChIKey = FQFKTKUFHWNTBN-UHFFFAOYSA-N
Fórmula química para trifluoruro de bromo
La fórmula química para este compuesto interhalógeno es BrF3.
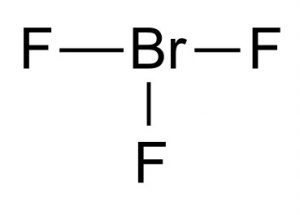
Imagen 1-Trifluoruro de bromo
Producción de trifluoruro de bromo
En el año 1906, Paul Lebeau sintetizó este compuesto por primera vez reaccionando bromo con flúor a una temperatura de 20°C. La reacción está representada por la siguiente ecuación:
Br2 + 3F2 → 2BrF3
Otra forma de producir trifluoruro de bromo es reducir y oxidar simultáneamente el monofluoruro de bromo. Esta reacción produce trifluoruro de bromo y bromo.
3BrF → BrF3 + Br2
Composición de trifluoruro de bromo
El trifluoruro de bromo se compone de 58,367% de bromo y 41,632% de flúor.
Propiedades del trifluoruro de bromo
Las propiedades físicas y químicas de esta sustancia se discuten a continuación:
Apariencia
Es un líquido de color pajizo.
Olor
El producto químico tiene un olor acre.
Higroscopia
Es un líquido higroscópico.
Masa molar
La masa molar del trifluoruro de bromo es de 136,90 g / mol.
Masa monoisotópica
La masa monoisotópica de esta sustancia es de 135,913547 u (unidades de masa atómica unificadas).
Densidad
La densidad de la sustancia es de 2,803 g / cm3.
Punto de Fusión
El punto de fusión de trifluoruro de Bromo es 8.77°C.
Punto de Ebullición
El punto de ebullición de esta sustancia es 125.72°C.
Conductividad
Debido a la autoionización, el líquido es un buen conductor de electricidad.
Corrosividad
es un líquido corrosivo.
Gravedad específica
La gravedad específica del trifluoruro de bromo es de 2,81 a una temperatura de 68,0°F.
Momento dipolar
El momento dipolar molecular de esta sustancia es de 1,19 Debye.
Solubilidad
El trifluoruro de bromo es soluble en ácido sulfúrico. Se descompone y explota cuando entra en contacto con compuestos orgánicos y agua. Las reacciones con compuestos que contienen hidrógeno pueden causar reacciones violentas. Muchos fluoruros iónicos se disuelven fácilmente en trifluoruro de bromo y forman solvobasas.
KF + BrF3 → KBrF4
Además de las propiedades mencionadas anteriormente, el trifluoruro de bromo también es un potente agente fluorante.
Estructura del trifluoruro de bromo
La estructura de Lewis del trifluoruro de bromo muestra que tiene una estructura molecular en forma de T. De acuerdo con la teoría de la formación molecular VSEPR, el bromo central está conectado con dos pares de electrones. La distancia entre el centro del bromo y el flúor ecuatorial es de 1,72 Å y a cada uno de los flúor axial es de 1,81 Å. El ángulo entre el flúor ecuatorial y un flúor axial es de 86,2°. El ángulo se mantiene ligeramente por debajo de 90°, ya que la fuerza de repulsión de los enlaces Br-F es menor que la fuerza de los pares de electrones.
Reacciones de trifluoruro de bromo
El trifluoruro de bromo en reacción con óxidos metálicos emite oxígeno. Cuando el trifluoruro de bromo reacciona con el dióxido de silicio, produce tetrafluoruro de silicio gaseoso y bromo.
En una reacción entre trifluoruro de bromo y óxido de titanio (IV), se producen fluoruro de titanio(IV) y bromo.
Usos de trifluoruro de bromo
El trifluoruro de bromo es un fuerte disolvente inorgánico ionizante y un agente fluorante. También se utiliza para fabricar hexafluoruro de uranio (UF6) mientras se procesa y reprocesa combustible nuclear.
Trifluoruro de bromo MSDS
Riesgos para la salud
Un ser humano expuesto al trifluoruro de bromo puede sufrir los siguientes problemas de salud:
Contacto con la piel: El contacto de la piel con esta sustancia química puede provocar sensaciones de ardor e irritación.
Contacto visual: Si los ojos entran en contacto con los vapores químicos o el producto químico en sí, puede provocar ardor grave en los ojos, úlceras e incluso ceguera.Ingestión
: La ingestión provoca quemaduras graves en las membranas mucosas.
Inhalación: La inhalación puede provocar irritación grave del sistema respiratorio superior.
Medidas de primeros auxilios
Ojos: Los ojos deben lavarse a fondo con abundante agua durante al menos 15 minutos. Es necesario consultar a un médico de inmediato.
Piel: Si la piel entra en contacto con el producto químico, las áreas infectadas deben lavarse bien con agua y jabón durante un mínimo de 15 minutos. Se requiere atención médica inmediata. La ropa contaminada debe quitarse rápidamente. La ropa debe limpiarse y secarse a fondo antes de reutilizarla. Los zapatos contaminados deben ser destruidos.Ingestión
: En caso de ingestión accidental, la víctima debe beber mucha agua. No se recomienda inducir el vómito.
Inhalación: En caso de cualquier efecto adverso, la víctima debe ser llevada a un área no contaminada. La respiración artificial debe aplicarse en caso de que la víctima no esté respirando. Si la respiración y la respiración siguen siendo difíciles, se debe administrar oxígeno. Se necesita más asistencia médica para garantizar la seguridad de la víctima.
Perfil de reactividad
El trifluoruro de bromo es un agente oxidante altamente reactivo. Reacciona violentamente cuando entra en contacto con el agua. Puede acelerar la quema de una sustancia combustible. Cuando entra en contacto con sustancias que contienen hidrógeno, como el ácido acético, el amoníaco y el metano, puede causar una explosión e incendio. También reacciona violentamente con ácidos, halógenos, haluros metálicos, metales y óxidos metálicos a temperatura ambiente. Causa específicamente reacciones peligrosas con ácido nítrico, ácido sulfúrico, yodo y selenio.
Medidas de lucha contra incendios
El trifluoruro de bromo es un agente oxidante, por lo que puede inflamarse o explotar cuando entra en contacto con combustibles.
En caso de grandes incendios, el área debe estar aislada e inundada con agua desde una distancia segura. Si los recipientes que almacenan trifluoruro de bromo están cerca del fuego, deben retirarse si es posible hacerlo de forma segura. Los recipientes deben enfriarse con agua corriente incluso mucho después de que se haya extinguido el fuego.
Medios de extinción de incendios: Se deben usar medios de extinción de incendios adecuados mientras se apaga el fuego. Se recomienda el uso de agua, productos químicos secos o ceniza de sosa para extinguir incendios.
Medidas de liberación accidental
Los materiales combustibles deben aislarse y debe evitarse cualquier conexión con ellos. El material derramado no debe tocarse. Las fugas de productos químicos deben detenerse si es posible hacerlo sin riesgo personal. La prevalencia de vapores químicos debe reducirse con rociado de agua. Se debe tener cuidado de no introducir agua en los recipientes de productos químicos. En el caso de derrames grandes, los productos químicos deben ponerse en cuarentena para ser desechados posteriormente. El área debe ventilarse adecuadamente.
Manejo de trifluoruro de bromo
El manejo de este material está sujeto a las regulaciones de manejo bajo la OSHA 29 CFR 1910.119 de los Estados Unidos.
Almacenamiento de trifluoruro de bromo
El producto químico debe almacenarse y manipularse de acuerdo con las normas y regulaciones actuales del Código NFPA 430 para el almacenamiento de Materiales Oxidantes Líquidos y Sólidos. Los contenedores químicos deben protegerse de cualquier tipo de daño físico. También deben mantenerse alejados de sustancias incompatibles.
Protección personal
Durante la manipulación de este producto químico, se debe tomar una protección adecuada. Se debe utilizar equipo de protección adecuado. Lo ideal sería que incluyeran::
- Se requiere un aparato de respiración autónomo MSHA/NIOSH (aprobado o equivalente) que tenga máscaras de oxígeno de presión y demanda para una respiración adecuada.
- Se requieren gafas protectoras o gafas de seguridad aprobadas por OSHA para proteger los ojos.
- Para proteger la piel de las infecciones dañinas resultantes del contacto con productos químicos, se deben usar ropa y guantes protectores.
Aparte del equipo de protección mencionado anteriormente, el área también debe estar bien ventilada. El mecanismo de ventilación debe ser resistente a las explosiones en caso de que haya concentraciones explosivas del producto químico. También debe proporcionarse un sistema de escape local.