L’élément chimique nihonium est classé comme un autre métal. Il a été découvert en 2012 par l’équipe collaborative RIKEN de Kosuke Morita.

Zone de Données
| Classification : | Le nihonium est un » autre métal » (présumé) |
| Poids atomique: | (286), pas d’isotopes stables |
| État : | solide (présumé) |
| Point de fusion: | |
| Point d’ébullition: | |
| Électrons: | 113 |
| Protons: | 113 |
| Neutrons dans l’isotope le plus abondant: | 173 |
| Coquilles d’électrons: | 2, 8, 18, 32, 32, 18, 3 |
| Configuration électronique: | 5f14 6d10 7s2 7p1 |
Afficher plus, y compris: Chaleurs, Énergies, Oxydation, Réactions
, Composés, Rayons, Conductivités
| Capacité thermique spécifique | – |
| Chaleur de fusion | – |
| Chaleur d’atomisation | – |
| Chaleur de vaporisation | – |
| 1ère énergie d’ionisation | – |
| 2ème énergie d’ionisation | – |
| 3ème énergie d’ionisation | – |
| Affinité électronique | – |
| Minimum oxidation number | – |
| Min. common oxidation no. | – |
| Maximum oxidation number | – |
| Max. common oxidation no. | – |
| Électronégativité (Échelle de Pauling) | – |
| Volume de polarisabilité | – |
| Réaction avec l’air | – |
| Réaction avec 15 M HNO3 | – |
| Réaction avec HCl 6 M | – |
| Réaction avec 6 M de NaOH | – |
| Oxyde (s) | – |
| Hydrure(s) | – |
| Chlorure(s) | – |
| Atomic radius | – |
| Ionic radius (1+ ion) | – |
| Ionic radius (2+ ion) | – |
| Ionic radius (3+ ion) | – |
| Ionic radius (1- ion) | – |
| Ionic radius (2- ion) | – |
| Ionic radius (3- ion) | – |
| Thermal conductivity | – |
| Electrical conductivity | – |
| Point de congélation/fusion: | – |

Le nihonium a été produit dans un accélérateur de particules. Image: LLNL.
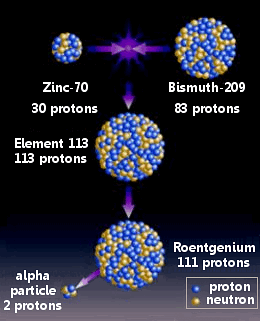
Du nihonium a été obtenue en combinant le zinc-70 avec le bismuth-209 dans une réation nucléaire.
Découverte du Nihonium
Le Nihonium a été découvert le 12 août 2012 par l’équipe collaborative RIKEN de Kosuke Morita au Japon. C’était le premier élément chimique jamais découvert en Asie.
La découverte a été officiellement acceptée le 30 décembre 2015 par l’IUPAC et l’IUPAP, et un nouvel élément super lourd a pris sa place dans la septième rangée du tableau périodique.
L’élément est nommé d’après l’endroit où il a été synthétisé pour la première fois; Nihon est l’une des deux façons de dire Japon en japonais.
Le nihonium a été fabriqué à l’aide de l’accélérateur linéaire de RIKEN et du séparateur d’ions GARIS à Wako, au Japon. L’isotope produit était le nihonium-278, qui ne traîne pas longtemps: sa demi-vie est inférieure à un millième de seconde.
L’équipe de Morita avait commencé ses travaux en septembre 2003. Des ions zinc (70Zn) ont été formés en un faisceau dans un accélérateur de particules et mis à feu sur une fine couche de bismuth (209Bi) dans une réaction de fusion à froid.
En utilisant cette méthode, les scientifiques pensaient avoir fabriqué un seul atome de l’élément 113 en juillet 2004 et à nouveau en avril 2005. À chaque fois, l’atome subit rapidement quatre désintégrations alpha : d’abord en roentgenium-274, suivi du meitnerium-270, du bohrium-266 et du dubnium-262.
Désintégrations alpha :
278Nh == > 274Rg == > 270Mt == > 266Bh == > 262Db
Ces résultats n’étaient pas suffisants pour satisfaire l’IUPAC et l’IUPAP. En 2011, leur Groupe de travail conjoint a refusé d’accepter la découverte de l’élément 113, déclarant que: « Le travail de la collaboration de Morita et al. est très prometteur mais n’a pas satisfait aux critères de découverte en raison de la rareté des événements, de l’absence de connexion ferme avec des nucléides connus et des incohérences notées ci-dessus. »
Les scientifiques au Japon ont alors fait une impasse. Morita a commenté: « Pendant plus de sept ans, nous avons continué à rechercher des données identifiant de manière concluante l’élément 113, mais nous n’avons tout simplement jamais vu d’autre événement. Je n’étais pas prêt à abandonner, cependant, car je croyais qu’un jour, si nous persévérions, la chance retomberait sur nous. »
Pour valider leur découverte du nihonium, l’équipe a réalisé une nouvelle expérience qui leur donnerait une meilleure idée de la chaîne de désintégration au-delà de 266Bh. Un faisceau d’ions sodium est entré en collision avec une cible de curium créant 266Bh qui s’est ensuite désintégré à 262Db.
Le 12 août 2012, les scientifiques ont observé un troisième événement de désintégration concluant. Le nihonium a été créé de la même manière qu’auparavant et a subi les mêmes quatre désintégrations alpha qu’auparavant. De plus, 262Db a continué à subir des désintégrations alpha, donnant 258Lr suivi de 254Md. Comme la chaîne avait été entièrement caractérisée, cela a été considéré comme une démonstration claire que la source de la chaîne de désintégration était bien le Nihonium, l’élément 113.
En 2015, le Groupe de travail mixte UICPA/UICPA a examiné les travaux et a déclaré que: « L’équipe de collaboration RIKEN au Japon a rempli les critères pour l’élément Z = 113 et sera invitée à proposer un nom et un symbole permanents. »
Apparence et caractéristiques
Effets nocifs:
Le nihonium est nocif en raison de sa radioactivité.
Caractéristiques:
Le nihonium est un métal radioactif synthétique.
Utilisations du nihonium
Le nihonium ne présente qu’un intérêt pour la recherche.
Abondance et Isotopes
Abondance croûte terrestre : néant
Abondance système solaire: parties par billion en poids, parties par billion en moles
Coût, pur: $ par 100g
Coût, en vrac: per par 100g
Source: L’élément a été créé à l’aide d’une réaction de fusion à froid entre une cible de bismuth-209 et des ions zinc-70.
Isotopes : Le nihonium a un isotope dont la demi-vie est connue, 278Nh.

- Expérience sur la Synthèse de l’élément 113 dans la Réaction, Journal de la Société de Physique du Japon, Vol. 73, No 10, octobre 2004, pp. 2593-2596
- Observation de la Deuxième chaîne de désintégration de 278113, Journal of the Physical Society of Japan Vol. 76, No 4, Avril 2007
- Robert Barber, Paul Karol, Hiromichi Nakahara, Emanuele Vardaci et Erich Vogt, Découverte des éléments de numéros atomiques supérieurs ou égaux à 113,. 2011, UICPA. (téléchargement pdf)
Citez cette Page
Pour les liens en ligne, veuillez copier et coller l’un des éléments suivants:
<a href="https://www.chemicool.com/elements/ununtrium.html">Nihonium</a>
ou
<a href="https://www.chemicool.com/elements/ununtrium.html">Nihonium Element Facts</a>
Pour citer cette page dans un document académique, veuillez utiliser la citation conforme à la MLA suivante :
"Nihonium." Chemicool Periodic Table. Chemicool.com. 11 Jun. 2016. Web. <https://www.chemicool.com/elements/ununtrium.html>.