Broomtrifluoride is een toxische interhalogeenverbinding. Het staat bekend om zijn gebruik als een sterk fluorerend middel.
Broom trifluoride Identificatie
CAS-Nummer: 7787-71-5
UN-Nummer: UN1746
PubChem Compound-ID: 24594
ChemSpider Referentie Nummer: 20474213
MDL-nummer: MFCD00042533
EG-Nummer: 232-132-1
SUPERTHERM-Nummer: ED2275000
InChI-Id: InChI=1S / BrF3 / c2-1(3)4
InChI-sleutel: InChIKey = FQFKTKUFHWNTBN-UHFFFAOYSA-N
chemische formule voor Broomtrifluoride
de chemische formule voor deze interhalogeenverbinding is BrF3.
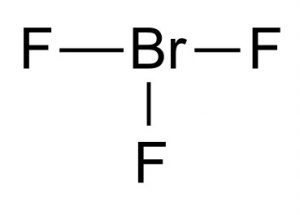
Afbeelding 1-Broomtrifluoride
productie van Broomtrifluoride
in het jaar 1906 synthetiseerde Paul Lebeau deze verbinding voor het eerst door Broom met Fluor te reageren bij een temperatuur van 20°C. De reactie wordt weergegeven door de volgende vergelijking::
Br2 + 3F2 → 2BrF3
een andere manier om Broomtrifluoride te produceren is het gelijktijdig verminderen en oxideren van Broommonofluoride. Deze reactie produceert Broomtrifluoride en broom.
3BrF → BrF3 + Br2
Broomtrifluoride samenstelling
Broomtrifluoride bestaat uit 58,367% broom en 41,632% fluor.
eigenschappen van Broomtrifluoride
de fysische en chemische eigenschappen van deze stof worden hieronder besproken:
voorkomen
het is een strokleurige vloeistof.
geur
de chemische stof heeft een scherpe geur.
Hygroscopie
het is een hygroscopische vloeistof.
Molaire massa
de molaire massa van Broomtrifluoride bedraagt 136,90 g / mol.
Mono-isotopische massa
de mono-isotopische massa van deze stof is 135,913547 u (unified atomic mass units).
dichtheid
de dichtheid van de stof is 2,803 g/cm3.
smeltpunt
het smeltpunt van Broomtrifluoride is 8,77°C.
kookpunt
het kookpunt van deze stof is 125,72°C.
geleidbaarheid
door auto-ionisatie is de vloeistof een goede geleider van elektriciteit.
corrosiviteit
het is een corrosieve vloeistof.
soortelijk gewicht
het soortelijk gewicht van Broomtrifluoride is 2,81 bij een temperatuur van 68,0°F.
dipoolmoment
het moleculaire dipoolmoment van deze stof is 1,19 Debye.
Oplosbaarheid
Broomtrifluoride is oplosbaar in zwavelzuur. Het ontleedt en explodeert wanneer het in contact komt met organische verbindingen en water. Reacties met waterstofhoudende verbindingen kunnen gewelddadige reacties veroorzaken. Veel Ionische fluoriden lossen gemakkelijk op in Broomtrifluoride en vormen solvobases.
KF + BrF3 → KBrF4
afgezien van de bovengenoemde eigenschappen is Broomtrifluoride ook een krachtig fluorerend middel.
structuur van Broomtrifluoride
De Lewis-structuur van Broomtrifluoride toont aan dat het een T-vormige moleculaire structuur heeft. Volgens de VSEPR-theorie van moleculaire vorming is het centrale Broom verbonden met twee elektronenparen. De afstand tussen het centrum van broom en het equatoriale fluor is 1,72 Å en tot elk van de axiale fluor is 1,81 Å. De hoek tussen Equatoriaal fluor en axiaal fluor is 86,2°. De hoek wordt iets minder dan 90° gehouden omdat de afstotingskracht van de BR-F-bindingen lager is dan de kracht van de elektronenparen.
Broomtrifluoridereacties
Broomtrifluoride als reactie met metaaloxiden geeft zuurstof af. Wanneer Broomtrifluoride reageert met siliciumdioxide, produceert het gasvormige siliciumtetrafluoride en broom.
in een reactie tussen Broomtrifluoride en titaan(IV) oxide worden titaan(IV) fluoride en broom geproduceerd.
Broomtrifluoride gebruikt
Broomtrifluoride is een sterk ioniserend anorganisch oplosmiddel en een fluoriserende stof. Het wordt ook gebruikt voor de vervaardiging van uraanhexafluoride (UF6) bij de verwerking en opwerking van splijtstof.
Broomtrifluoride MSDS
gezondheidsrisico ‘ s
een mens die wordt blootgesteld aan Broomtrifluoride kan de volgende gezondheidsproblemen hebben:
huidcontact: Huidcontact met deze chemische stof kan leiden tot branderig en irriterend gevoel.
oogcontact: als de ogen in contact komen met de chemische dampen of de chemische stof zelf, kan dit leiden tot ernstige verbranding van de ogen, zweren en zelfs blindheid.
inslikken: inslikken leidt tot ernstige verbranding van de slijmvliezen.Inhalatie: inhalatie kan leiden tot ernstige irritatie van de bovenste luchtwegen.
eerste hulpmaatregelen
Ogen: de ogen moeten gedurende ten minste 15 minuten grondig met veel water worden gewassen. Een arts moet onmiddellijk worden geraadpleegd.
huid: als de huid in contact komt met de chemische stof, moeten de besmette gebieden gedurende minimaal 15 minuten goed worden gewassen met water en zeep. Onmiddellijke medische zorg is vereist. De verontreinigde kleding moet snel worden verwijderd. De kleding moet grondig worden gereinigd en gedroogd voor hergebruik. De besmette schoenen moeten worden vernietigd.
inslikken: in geval van accidentele inname dient het slachtoffer voldoende water te drinken. Induceren van braken wordt niet aanbevolen.
inhalatie: In geval van nadelige effecten moet het slachtoffer naar een niet-verontreinigd gebied worden gebracht. Kunstmatige ademhaling moet worden toegepast in het geval het slachtoffer niet ademt. Als de ademhaling en ademhaling nog steeds moeilijk is, moet zuurstof worden toegediend. Verdere medische hulp is nodig om de veiligheid van het slachtoffer te waarborgen.
Reactiviteitsprofiel
Broomtrifluoride is een sterk reactieve oxiderende stof. Het reageert heftig als het in contact komt met water. Het kan de verbranding van een brandbare stof versnellen. Wanneer het in contact komt met waterstofhoudende stoffen zoals azijnzuur, ammoniak en methaan, kan het een explosie en brand veroorzaken. Het reageert ook heftig met zuren, halogenen, metaalhalogeniden, metalen en metaaloxiden bij kamertemperatuur. Het veroorzaakt vooral gevaarlijke reacties met salpeterzuur, zwavelzuur, jodium en selenium.
brandbestrijdingsmaatregelen
Broomtrifluoride is een oxiderende stof en kan daarom ontbranden of exploderen wanneer het in contact komt met brandbare stoffen.
bij grote branden moet het gebied worden geïsoleerd en van een veilige afstand met water worden overspoeld. Als de containers waarin Broomtrifluoride wordt opgeslagen in de buurt van vuur liggen, moeten ze worden verwijderd als dit veilig kan worden gedaan. De containers moeten worden gekoeld met stromend water, zelfs lang nadat de brand is gedoofd.
Brandblusmedia: geschikte brandblusmedia moeten worden gebruikt tijdens het blussen van brand. Gebruik van water, droog chemisch product of natriumcarbonaat wordt aanbevolen voor het blussen van brand.
maatregelen voor het per ongeluk vrijkomen
de brandbare materialen moeten worden geïsoleerd en elke verbinding ermee moet worden vermeden. Het gemorste materiaal mag niet worden aangeraakt. Chemische lekkage moet worden gestopt als dit mogelijk is zonder persoonlijk risico. De prevalentie van chemische dampen moet worden verminderd met waternevel. Er moet op worden gelet dat er geen water in de chemische containers komt. Bij grote morsen moeten de chemicaliën in quarantaine worden geplaatst om later te worden verwijderd. Het gebied moet goed worden geventileerd.
hantering van Broomtrifluoride
hantering van dit materiaal is onderworpen aan de hanteringsvoorschriften van U. S. OSHA 29 CFR 1910.119.
opslag van Broomtrifluoride
de chemische stof moet worden opgeslagen en behandeld volgens de huidige normen en voorschriften van de NFPA 430-Code voor de opslag van vloeibare en vaste Oxiderende materialen. De chemische containers moeten worden beschermd tegen elke vorm van fysieke schade. Ze moeten ook uit de buurt van onverenigbare stoffen worden gehouden.
persoonlijke bescherming
bij het hanteren van deze chemische stof moet voldoende bescherming worden genomen. De juiste beschermingsuitrusting moet worden gebruikt. Deze moeten idealiter omvatten:
- MSHA / NIOSH (goedgekeurd of gelijkwaardig) zelfstandige ademhalingsapparatuur met druk-Vraag zuurstofmaskers is vereist voor een goede ademhaling.
- door OSHA goedgekeurde beschermende brillen of veiligheidsbrillen zijn vereist om de ogen te beschermen.
- om de huid te beschermen tegen schadelijke infecties als gevolg van chemisch contact, dienen beschermende kleding en handschoenen te worden gebruikt.
behalve de bovengenoemde beschermingsuitrusting moet het gebied ook goed geventileerd zijn. Het ventilatiemechanisme moet bestand zijn tegen explosies wanneer er explosieve concentraties van de chemische stof aanwezig zijn. Er moet ook een lokaal uitlaatsysteem aanwezig zijn.