elementul chimic nihoniu este clasificat ca un alt metal. A fost descoperit în 2012 de echipa de colaborare Riken a lui Kosuke Morita.

zona de date
| clasificare: | Nihoniul este un ‘ alt metal ‘(presupus) |
| greutate atomică: | (286), fără izotopi stabili |
| stare: | solid (presupus) |
| punct de topire: | |
| punct de fierbere: | |
| electroni: | 113 |
| protoni: | 113 |
| neutronii din izotopul cel mai abundent: | 173 |
| cochilii de electroni: | 2, 8, 18, 32, 32, 18, 3 |
| configurația electronică: | 5f14 6d10 7s2 7p1 |
arată mai mult, inclusiv: Incalziri, energii, oxidare,
reactii, compusi, raze, Conductivitati
| capacitate specifică de căldură | – |
| căldură de fuziune | – |
| căldură de atomizare | – |
| căldură de vaporizare | – |
| 1 energie de ionizare | – |
| a 2-a energie de ionizare | – |
| a 3-a energie de ionizare | – |
| afinitate Electronică | – |
| Minimum oxidation number | – |
| Min. common oxidation no. | – |
| Maximum oxidation number | – |
| Max. common oxidation no. | – |
| electronegativitate (scara Pauling) | – |
| Polarizabilitate volum | – |
| reacția cu aerul | – |
| reacție cu 15 m HNO3 | – |
| reacție cu HCl de 6 M | – |
| reacție cu 6 m NaOH | – |
| oxid(e) | – |
| hidrură(s) | – |
| clorură(cloruri) | – |
| Atomic radius | – |
| Ionic radius (1+ ion) | – |
| Ionic radius (2+ ion) | – |
| Ionic radius (3+ ion) | – |
| Ionic radius (1- ion) | – |
| Ionic radius (2- ion) | – |
| Ionic radius (3- ion) | – |
| Thermal conductivity | – |
| Electrical conductivity | – |
| punctul de congelare/topire: | – |

Nihonium a fost produs într-un accelerator de particule. Imagine: LLNL.
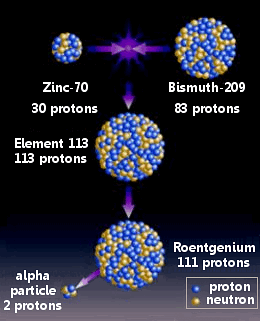
Nihoniul a fost realizat prin combinarea zincului-70 cu bismutul-209 într-o reație nucleară.
descoperirea Nihoniului
Nihoniul a fost descoperit pe 12 August 2012 de echipa de colaborare Riken a lui Kosuke Morita din Japonia. A fost primul element chimic descoperit vreodată în Asia.
descoperirea a fost acceptată oficial la 30 decembrie 2015 de către IUPAC și IUPAP, iar un nou element super-greu și-a luat locul în al șaptelea rând al tabelului periodic.
elementul este numit după locul în care a fost sintetizat pentru prima dată; Nihon este unul dintre cele două moduri de a spune Japonia în Japoneză.
Nihonium a fost fabricat folosind instalația de accelerare liniară RIKEN și separatorul de ioni GARIS din Wako, Japonia. Izotopul produs a fost nihonium-278, care nu atârnă mult timp: timpul său de înjumătățire este mai mic de o mie de secundă.
echipa lui Morita își începuse activitatea în septembrie 2003. Ionii de Zinc (70Zn) s-au format într-un fascicul într-un accelerator de particule și au tras într-un strat subțire de bismut (209bi) într-o reacție de fuziune la rece.
folosind această metodă, oamenii de știință au crezut că au făcut un singur atom al elementului 113 în iulie 2004 și din nou în aprilie 2005. Cu fiecare ocazie, atomul a suferit rapid patru dezintegrări Alfa: mai întâi la roentgenium-274, urmat de meitnerium-270, bohrium-266 și dubnium-262.
alfa se descompune :
278nh ==> 274rg ==> 270mt ==> 266bh = = > 262db
aceste rezultate nu au fost suficiente pentru a satisface IUPAC și IUPAP. În 2011, grupul lor comun de lucru a refuzat să accepte descoperirea elementului 113, afirmând că: „lucrarea colaborării lui Morita și colab. este foarte promițătoare, dar nu a îndeplinit criteriile de descoperire din cauza numărului redus de evenimente, a absenței unei legături ferme cu nuclizii cunoscuți și a inconsecvențelor menționate mai sus.”
oamenii de știință din Japonia au lovit apoi o fundătură. Morita a comentat: „Timp de peste șapte ani am continuat să căutăm date care să identifice în mod concludent elementul 113, dar nu am văzut niciodată un alt eveniment. Cu toate acestea, nu eram pregătit să renunț, deoarece credeam că într-o zi, dacă perseverăm, norocul va cădea din nou asupra noastră.”
pentru a ajuta la validarea descoperirii nihoniului, echipa a efectuat un nou experiment care le-ar oferi o idee mai bună despre lanțul de dezintegrare dincolo de 266Bh. Un fascicul de ioni de sodiu a fost ciocnit cu o țintă curium creând 266Bh care apoi s-a descompus la 262db.
la 12 August 2012, oamenii de știință au observat un al treilea eveniment concludent de dezintegrare. Nihoniul a fost creat în același mod ca înainte și a suferit aceleași patru dezintegrări alfa ca anterior. În plus, 262Db a continuat să sufere dezintegrări alfa, producând 258Lr urmat de 254md. Deoarece lanțul fusese pe deplin caracterizat, acest lucru a fost luat ca o demonstrație clară că sursa lanțului de descompunere era într-adevăr nihoniu, elementul 113.
în 2015, Grupul de lucru comun IUPAC/IUPAP (JWP) a revizuit activitatea și a declarat că: „Echipa de colaborare Riken din Japonia a îndeplinit criteriile pentru elementul Z=113 și va fi invitată să propună un nume și un simbol permanent.”
aspect și caracteristici
efecte nocive:
Nihoniul este dăunător datorită radioactivității sale.
caracteristici:
Nihoniul este un metal radioactiv sintetic.
utilizări ale Nihoniului
Nihoniul este doar de interes pentru cercetare.
abundență și izotopi
abundență scoarța pământului: zero
abundență sistem solar: părți pe trilion în greutate, părți pe trilion de moli
Cost, pur: $ pe 100g
Cost, vrac: $ pe 100g
Sursa: elementul a fost creat folosind o reacție de fuziune la rece între un bismut-209 țintă și zinc-70 ioni.
izotopi: Nihoniul are un izotop al cărui timp de înjumătățire este cunoscut, 278Nh.

- Experiment privind sinteza elementului 113 în reacția, Jurnalul Societății fizice din Japonia, Vol. 73, nr. 10, octombrie, 2004, pp. 2593-2596
- observarea celui de-al doilea lanț de dezintegrare din 278113, Journal of the Physical Society of Japan Vol. 76, nr. 4, aprilie, 2007
- Robert Barber, Paul Karol, Hiromichi Nakahara, Emanuele Vardaci, și Erich Vogt, descoperirea elementelor cu numere atomice mai mari sau egale cu 113,. 2011, IUPAC. (Descărcare pdf)
citați Această pagină
pentru conectarea online, copiați și lipiți una dintre următoarele:
<a href="https://www.chemicool.com/elements/ununtrium.html">Nihonium</a>
sau
<a href="https://www.chemicool.com/elements/ununtrium.html">Nihonium Element Facts</a>
pentru a cita această pagină într-un document academic, vă rugăm să folosiți următoarea citare conformă MLA:
"Nihonium." Chemicool Periodic Table. Chemicool.com. 11 Jun. 2016. Web. <https://www.chemicool.com/elements/ununtrium.html>.