Im Allgemeinen können Amide entweder in saurer oder basischer Lösung hydrolysiert werden. Die Mechanismen ähneln denen der Esterhydrolyse (Abschnitt 18-7A), aber die Reaktionen sind sehr viel langsamer, eine Eigenschaft von großer biologischer Bedeutung (auf die wir später eingehen werden):
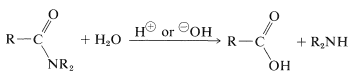
Wie wir in Abschnitt 23-12 angedeutet haben, kann die Amidhydrolyse ein wichtiger Weg zu Aminen sein. Die Hydrolyse unter sauren Bedingungen erfordert starke Säuren wie Schwefel- oder Salzsäure und Temperaturen von etwa \ (100 ^ \ text {o} \) für mehrere Stunden. Der Mechanismus beinhaltet die Protonierung des Amids an Sauerstoff, gefolgt von einem Angriff von Wasser auf den Carbonylkohlenstoff. Das gebildete tetraedrische Zwischenprodukt dissoziiert schließlich zur Carbonsäure und zum Ammoniumsalz:
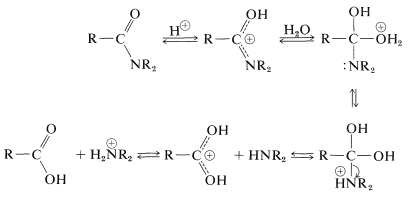
Bei der alkalischen Hydrolyse wird das Amid mit siedendem wässrigem Natrium- oder Kaliumhydroxid erhitzt. Das nukleophile Hydroxidion addiert sich zum Carbonylkohlenstoff zu einem tetraedrischen Zwischenprodukt, das mit Hilfe des wässrigen Lösungsmittels den Stickstoff als freies Amin ausstößt:
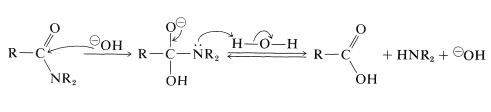
Die biologische Amidhydrolyse, wie bei der Hydrolyse von Peptiden und Proteinen, wird durch die proteolytischen Enzyme katalysiert. Diese Reaktionen werden in Kapitel 25 diskutiert.
Eine indirekte Methode zur Hydrolyse einiger Amide verwendet salpetrige Säure. Primäre Amide werden durch Behandlung mit salpetriger Säure leicht in Carbonsäuren umgewandelt. Diese Reaktionen sind denen sehr ähnlich, die zwischen einem primären Amin und salpetriger Säure auftreten (Abschnitt 23-10):
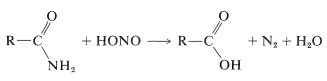
Sekundäre Amide ergeben \(\ce{N}\)-Nitrosoverbindungen mit salpetriger Säure, während tertiäre Amide nicht reagieren:
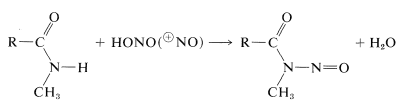
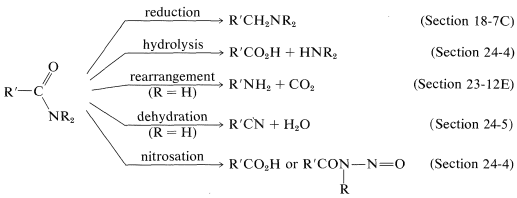
Es folgt eine kurze Zusammenfassung wichtiger Amidreaktionen:
Von den vielen anderen bekannten Arten von Organonitrogenverbindungen umfassen die wichtigeren

Obwohl es unpraktisch ist, alle diese Verbindungen im Detail zu diskutieren, werden wir nun kurz einige diskutieren, denen bisher nicht viel Aufmerksamkeit geschenkt wurde.
Mitwirkende und Zuschreibungen
- John D. Robert und Marjorie C. Caserio (1977) Grundprinzipien der organischen Chemie, zweite Ausgabe. W. A. Benjamin, Inc. In : Menlo Park, CA. ISBN 0-8053-8329-8. Dieser Inhalt ist unter den folgenden Bedingungen urheberrechtlich geschützt: „Sie erhalten die Erlaubnis zur individuellen, pädagogischen, forschungsbezogenen und nichtkommerziellen Reproduktion, Verbreitung, Anzeige und Aufführung dieser Arbeit in jedem Format.“