Vergleich von Säureanhydriden mit Säurechloriden (Säurechloride)
Sie sind mit ziemlicher Sicherheit zum ersten Mal auf Säureanhydride gestoßen, nachdem Sie sich die Säurechloride angesehen haben, oder Sie untersuchen sie möglicherweise gleichzeitig mit den Säurechloriden. Es ist viel, viel einfacher, an Säureanhydride zu denken, als wären sie eine Art modifiziertes Acylchlorid, als zu versuchen, sie von Grund auf neu kennenzulernen. Das ist die Linie, die ich in diesem ganzen Abschnitt vertreten werde. Vergleichen Sie die Struktur eines Säureanhydrids mit der eines Acylchlorids – schauen Sie sich genau an, wie es im Diagramm dargestellt ist.
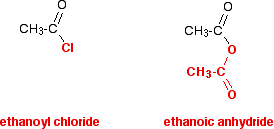
Bei den Reaktionen von Ethananhydrid bleibt die rote Gruppe am Boden immer intakt. Es verhält sich in vielerlei Hinsicht so, als wäre es ein einzelnes Atom – genau wie das Chloratom im Acylchlorid. Die übliche Reaktion eines Acylchlorids ist der Ersatz des Chlors durch etwas anderes.
Unter Verwendung von Ethanoylchlorid als typisch ist die anfängliche Reaktion dieser Art:

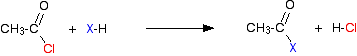
Chlorwasserstoffgas wird abgegeben, obwohl dies mit anderen Komponenten des Gemisches reagieren könnte. Bei einem Säureanhydrid ist die Reaktion langsamer, aber der einzige wesentliche Unterschied besteht darin, dass anstelle von Chlorwasserstoff als anderes Produkt Ethansäure erhalten wird.

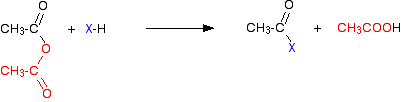
Genau wie der Chlorwasserstoff kann dieser anschließend mit anderen vorhandenen Dingen reagieren. Die Reaktionen (sowohl von Acylchloriden als auch von Säureanhydriden) beinhalten Dinge wie Wasser, Alkohole und Phenole oder Ammoniak und Amine. Alle diese speziellen Fälle enthalten ein sehr elektronegatives Element mit einem aktiven einsamen Elektronenpaar – entweder Sauerstoff oder Stickstoff.