zuuranhydriden vergelijken met acylchloriden (zuurchloriden)
u bent vrijwel zeker zuuranhydriden voor het eerst tegengekomen net na het bekijken van acylchloriden, of u bestudeert ze mogelijk tegelijk met acylchloriden. Het is veel, veel gemakkelijker om aan zuuranhydriden te denken alsof ze een soort gemodificeerd acylchloride zijn dan om er vanaf nul over te leren. Dat is de lijn die ik in dit hele hoofdstuk wil volgen. Vergelijk de structuur van een zuuranhydride met die van een acylchloride – zorgvuldig kijken naar de manier waarop het kleur in het diagram.
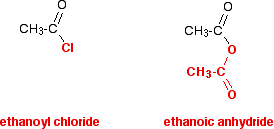
in de reacties van ethaanzuuranhydride blijft de rode groep onderaan altijd intact. Het gedraagt zich op vele manieren alsof het een enkel atoom is – net als het chlooratoom in het acylchloride. De gebruikelijke reactie van een acylchloride is het vervangen van het chloor door iets anders.
wanneer ethanoylchloride als typisch wordt gebruikt, is de initiële reactie van deze aard:

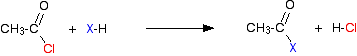
Waterstofchloridegas wordt afgegeven, hoewel dat kan gaan reageren met andere componenten van het mengsel. Met een zuuranhydride is de reactie langzamer, maar het enige essentiële verschil is dat in plaats van waterstofchloride wordt geproduceerd als het andere product, je ethaanzuur krijgt.

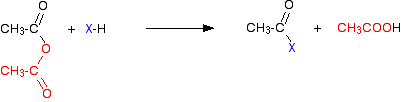
net als het Waterstofchloride, kan dit later gaan reageren met andere dingen aanwezig. De reacties (van zowel acylchloriden als zuuranhydriden) betreffen zaken als water, alcoholen en fenolen, of ammoniak en aminen. Al deze specifieke gevallen bevatten een zeer elektronegatief element met een actief eenzame paar elektronen – ofwel zuurstof of stikstof.