a savas anhidridek összehasonlítása Acil-kloridokkal (savas kloridok)
szinte biztos, hogy először találkozott savas anhidridekkel, miután megvizsgálta az acil-kloridokat, vagy esetleg az acil-kloridokkal egyidejűleg tanulmányozza őket. Sokkal, sokkal könnyebb úgy gondolni a savas anhidridekre, mintha egyfajta módosított Acil-klorid lennének, mint megpróbálni megismerni őket a semmiből. Ezt a vonalat szándékozom végigvinni ebben a szakaszban. Hasonlítsa össze a savas anhidrid szerkezetét az acil-klorid szerkezetével-gondosan nézze meg a diagram színét.
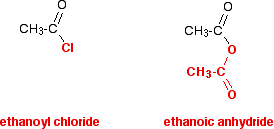
az etánsav-anhidrid reakcióiban az alján lévő vörös csoport mindig érintetlen marad. Sok szempontból úgy viselkedik, mintha egyetlen atom lenne – akárcsak az acil-kloridban lévő klóratom. Az acil-klorid szokásos reakciója a klór helyettesítése valami mással.
az etanoil-kloridot tipikusnak tekintve a kezdeti reakció ilyen:

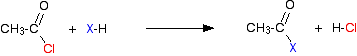
hidrogén-klorid gázt bocsátanak ki, bár ez tovább reagálhat a keverék más komponenseivel. Savas anhidrid esetén a reakció lassabb, de az egyetlen lényeges különbség az, hogy a másik termékként hidrogén-klorid előállítása helyett etánsavat kapunk.

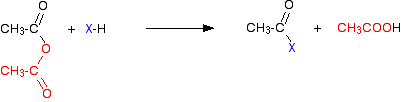
csakúgy, mint a hidrogén-klorid, ez később reakcióba léphet más jelenlévő dolgokkal. A reakciók (mind az acil-kloridok, mind a savas anhidridek) olyan dolgokat tartalmaznak, mint a víz, az alkoholok és a fenolok, vagy az ammónia és az aminok. Mindezek a különleges esetek nagyon elektronegatív elemet tartalmaznak, aktív magányos elektronpárral-akár oxigénnel, akár nitrogénnel.