van Der Vaals ligning blev foreslået i år 1873. Det var et første skridt i retning af at tage hensyn til interaktionskræfter, der virker mellem virkelige gasmolekyler.
tilstandsligningen for den perfekte gas henviser til en gas bestående af punktlignende genstande, der ikke interagerer med hinanden.
i stedet for denne van Der Vaals foreslået en ligning
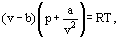
hvor a og b er de såkaldte Van Der Vaals konstanter, og som har forskellige værdier for hver gas.
B-korrektionen tager højde for det faktum, at ifølge van Der Vaals. de virkelige gasmolekyler kan ikke bevæge sig i det samlede volumen, der optages af gassen, men kun i en del af dette volumen, der defineres ved at trække det, han kaldte molekylernes eget volumen. Korrektionen a / kr2 —proportional med kvadratet af densitet-tager højde for de tiltrækningskræfter, der findes mellem gasmolekyler. I henhold til antagelsen om van Der Vaals mindsker disse kræfter trykket mod karvæggene, fordi molekylerne, der er tæt på væggen, udsættes for tiltrækning af andre molekyler.
A-og b-konstanterne skal betragtes som empiriske; de skal udledes af eksperimentelle data om indbyrdes afhængighed af densitet, temperatur og tryk. For en række teknisk vigtige gasser er varevognskonstanterne tabuleret.
ifølge metoden til at tillade afvigelse af en reel gas fra en perfekt gas, ville van Der-ligningen angiveligt kun være gyldig for små afvigelser, dvs.for moderate tryk. Men det viste sig, at denne ligning kvalitativt tilfredsstillende beskriver den virkelige gasadfærd i en lang række parametre, herunder den kritiske region.
Van Der Vaals-ligningen er en kubisk ligning med hensyn til det specifikke volumen. Dette betyder, at hver trykværdi generelt ved en given temperatur svarer til tre specifikke volumenværdier—kr1, kr2, kr2. Værdierne LR1 og LR2 svarer til fysisk eksisterende tilstande af væske og damp. Værdien kurr, hvor (kurr p / kurr v) t > 0, svarer til en ustabil tilstand og eksisterer ikke fysisk. Efterhånden som temperaturen stiger, kommer værdierne prit1 og prit2 tættere på, og til sidst på det kritiske punkt falder alle tre rødder sammen ved det kritiske volumen vc. Ved højere temperaturer forbliver kun en rod af Van Der-ligningen reel, de to andre er imaginære. Disse superkritiske isotermer afslører infleksioner ved Kris = vc, som er tæt på opførelsen af virkelige stoffer.
for så vidt angår det kritiske punkt er følgende betingelser gyldige:

og det er muligt ved hjælp af Van Der Vaals ligning at udlede sammenkoblinger mellem Van Der Vaals konstanter og kritiske parametre for et stof.

derfor vil den kritiske kompressibilitetsfaktor være identisk for alle stoffer og lig med

i virkeligheden passer de kritiske kompressibilitetsfaktorer for de fleste stoffer ind i området 0,21-0,31.
Van Der Vaals-ligningen kan omarrangeres til en ikke-dimensionel form ved hjælp af de reducerede parametre:

i dette koordinater bliver van Der-ligningen:

dette betyder, at med reducerede parametre beskrives alle stoffer, der adlyder Van Der-ligningen, ved en identisk tilstandsligning. Herfra følger det, at alle disse stoffer kan behandles på samme måde. F. eks.har alle stoffer de samme værdier på samme kr. og kr. Denne generaliserede tilgang bruges også med mere sofistikerede tilstandsligninger, der beskriver den virkelige stoffers adfærd bedre end van Der-ligningen.